
 ,
, ;HNO3;Cu;
;HNO3;Cu;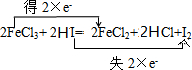 ,
,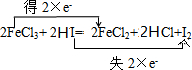 ;FeCl3;HI.
;FeCl3;HI.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
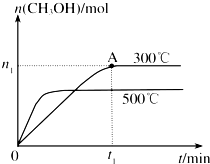 甲醇是一种可再生燃料.在容积为2L的密闭容器中进行反应:CO(g)
甲醇是一种可再生燃料.在容积为2L的密闭容器中进行反应:CO(g)查看答案和解析>>
科目:高中化学 来源: 题型:
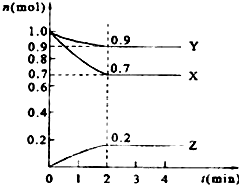 某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示. 查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D为短周期元素,A元素的原子价电子排布为ns2np2,B元素原子的最外层子数是其电子层数的3倍,C元素原子的M能层的p能级有3个未成对电子,D元素原子核外的M能层中只有2对成对电子.请回答下列问题:
A、B、C、D为短周期元素,A元素的原子价电子排布为ns2np2,B元素原子的最外层子数是其电子层数的3倍,C元素原子的M能层的p能级有3个未成对电子,D元素原子核外的M能层中只有2对成对电子.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
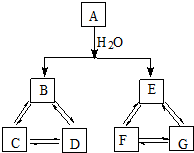 有A、B、C、D、E、F、G七种常见物质,它们满足下图所示转化关系.已知:
有A、B、C、D、E、F、G七种常见物质,它们满足下图所示转化关系.已知:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原电池是化学能转变为电能的装置 |
| B、构成原电池的正极和负极必须是两种不同的金属 |
| C、在原电池中,电子流出的一极是负极,该电极被还原 |
| D、原电池放电时,电流的方向是从负极到正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
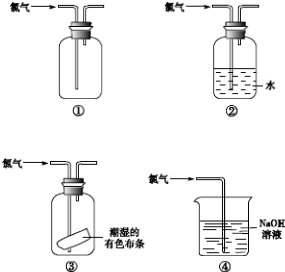
| A、①② | B、①③ | C、②③ | D、①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com