
【题目】常温下,向20mL 0.2mol/LH2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如图(其中I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)所示。根据图示判断,下列说法正确的是
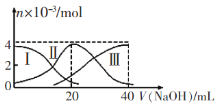
A.当V(NaOH)=20 mL时,溶液中离子浓度大小关系: c(Na+)>c(HA-)>c(A2-)>c(H+)>c(OH-)
B.等浓度的NaOH溶液与H2A溶液按体积2:1混合后,其溶液中水的电离程度比纯水大
C.NaHA溶液中:c(OH-)=c(H+)+c(HA-)+2c(H2A)
D.向上述加入20 mL NaOH溶液后所得溶液中再加入水的过程中,pH可能减少
【答案】B
【解析】
试题分析:A.根据图象知,当V(NaOH)=20 mL时,发生反应为NaOH+H2A═NaHA+H2O,溶质主要为NaHA,HA-电离程度大于水解程度,溶液显酸性,水和HA-都电离出氢离子,只有HA-电离出A2-,所以离子浓度大小顺序是c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-),故A错误;B.等浓度的NaOH溶液与H2A溶液按体积2:1混合后,二者恰好反应生成Na2A和水,Na2A是强碱弱酸盐促进水电离,故B正确;C.根据电荷守恒得c(OH-)+2c(A2-)+c(HA-)=c(H+)+c(Na+),根据物料守恒得c(Na+)=c(HA-)+c(H2A)+c(A2-),所以得c(OH-)+c(A2-)=c(H+)+c(H2A),故C错误;D.二者恰好反应生成NaHA,加水稀释HA-电离和水解,但氢氧根离子浓度减小,但水解程度大于电离程度,所以pH增大,故D错误;故选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】I.20mL0.1mol/LBaCl2溶液中Cl-的物质的量浓度为________,Ba2+的物质的量为_______。
II.把5.1g镁铝合金的粉末放入过量的盐酸中,得到5.6 LH2(标准状况下)。
(1)合金中镁的物质的量_________。
(2)写出该合金溶于足量NaOH溶液的化学方程式_________。同时产生H2的体积(标准状况下)为____________ 。
III.在一定质量的AlCl3和MgCl2混合溶液中逐渐滴入一定溶质质量分数的NaOH溶液,生成沉淀的物质的量与加入NaOH的物质的量的关系如图所示,则:

①生成Mg(OH)2的质量为__________;
②X=_______;Y=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氯水中滴入紫色石蕊试液、硝酸银溶液,将依次观察到紫色石蕊试液先变红后退色、有白色沉淀产生等现象。这些现象与氯水所含的下列哪种微粒无直接关系?
A.HClO
B.H2O
C.Cl-
D.H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】侯德榜是我国制碱丁业的先驱,他根据氨碱法制碱的缺点提出用饱和的NaCl溶液、CO2、NH3反应制取纯碱的联合制碱法。某学校课外活动小组根据侯氏制碱法的原理在实验室模拟制碱。请同答下列问题:
(1)写出实验室制取NH3的化学方程式:_______________。
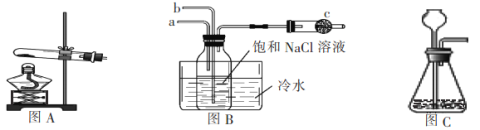
(2)上图B中的a接装置图_________(填图A或图C)
(3)用离子方程式表示装有饱和食盐水的集气瓶中的现象:______________________。
(4)水槽中的冷水的作用除了可以增加气体物质在溶液中的溶解度外还有一个重要作用是:_____________。
(5)图B中c的作用是:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KCl中有少量的KI,为了除去杂质,可选用以下操作中的( )
①加入碘水 ②通入Cl2 ③用CCl4萃取 ④过滤
A.①③
B.①④
C.②③
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下2CO(g) + O2(g) = 2CO2(g) △H=-566 kJ·mol—1;CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890 kJ·mol—1,则1molCO和3molCH4组成的混合气体在上述条件下完全燃烧放出的热量为
A.2912 kJ B.2953 kJ C.3236 kJ D.3836 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个恒压的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应![]()
![]()
![]() ,经一段时间后,甲、乙两容器反应都达到平衡,下列说法中正确的是
,经一段时间后,甲、乙两容器反应都达到平衡,下列说法中正确的是
A. 平均反应速度:![]() B. 平衡时C的物质的量甲>乙
B. 平衡时C的物质的量甲>乙
C. 平衡时C的转化率:乙<甲 D. 平衡时A的物质的量甲>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中含有Mg2+、Al3+、Fe3+、Cu2+、NH4+、 Na+中的一种或几种, 取100mL该溶液,向其中不断滴加某浓度的NaOH溶液,产生的沉淀随着NaOH体积变化的关系如图所示, 则下列叙述不正确的是( )

A. 该溶液中一定不含Fe3+、Cu2+
B. a点到b点,没有发生化学反应
C. 所加NaOH溶液物质的量浓度为1mol/L
D. 该溶液中一定含有Mg2+、Al3+、NH4+,且三者物质的量浓度之比为1:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】宝鸡被誉为“青铜器之乡”,出土了大盂鼎、毛公鼎、散氏盘等五万余件青铜器。研究青铜器(含Cu、Sn等)在潮湿环境中发生的腐蚀对于文物保护和修复有重要意义。下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图,下列说法不正确的是

A. 青铜器发生电化学腐蚀,图中c作负极,被氧化
B. 正极发生的电极反应为O2+ 4e-+2H2O=4OH-
C. 环境中的Cl- 与正、负两极反应的产物作用生成a的离子方程式为2Cu2++3OH-+Cl-=Cu2 (OH)3Cl↓
D. 若生成0.2 mol Cu2(OH)3Cl,则理论上消耗的O2体积为4.48L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com