
| A、氯水的颜色呈浅黄绿色,说明氯水中含有Cl2 |
| B、向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- |
| C、向氯水中加入紫色石蕊试液,先变红后褪色,说明氯水中含有H+及HClO |
| D、向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中只含有HClO |


科目:高中化学 来源: 题型:
| A、少量过氧化钠投入AlCl3溶液 |
| B、向饱和碳酸钠溶液通入CO2气体 |
| C、向Fe(NO3)2溶液中滴加稀硫酸 |
| D、向碳酸氢钠溶液中滴加氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
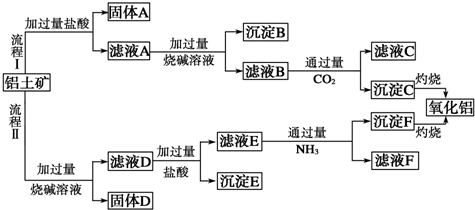
查看答案和解析>>
科目:高中化学 来源: 题型:
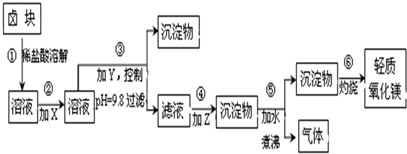
| 表1:生成氢氧化物沉淀的pH | 表2:原料价格表 | |||
| 物质 | 开始沉淀 | 沉淀完全 | 物质 | 价格(元/吨) |
| Fe(OH)3 | 2.7 | 3.7 | a.漂液(含25.2%NaClO) | 450 |
| Fe(OH)2 | 7.6 | 9.6﹡ | b.双氧水(含30%H2O2) | 2400 |
| Mn(OH)2 | 8.3 | 9.8 | c.烧碱(含98%NaOH) | 2100 |
| Mg(OH)2 | 9.6 | 11.1 | d.纯碱(含99.5%Na2CO3) | 600 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加水振荡,静置分层后,用分液漏斗分离去水层 |
| B、加入氢溴酸并加热,使乙醇转化为溴乙烷 |
| C、加入金属钠,使乙醇发生反应而除去 |
| D、加入浓硫酸并加热到170℃,使乙醇变成乙烯而逸出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、MnO4-、Mg2+、Cl- |
| B、Na+、Ba2+、HCO3-、NO3- |
| C、Na+、NO3-、CO32-、Cl- |
| D、K+、H+、Cl-、S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com