
【题目】二氧化氯是高效、低毒的消毒剂。已知:ClO2 是一种黄绿色易溶于水的气体,具有强氧化性, 回答下列问题:
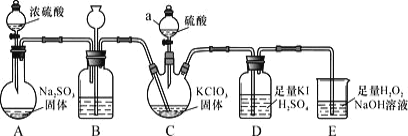
(1)ClO2 的制备及性质探究(如图所示)
①仪器 C 的名称为_________,装置 B 的作用是________。
②装置C 用于制备ClO2,同时还生成一种酸式盐,该反应的化学方程式为_____,装置 D 中滴有几滴淀粉溶液,其作用是_______。
③装置E 用于吸收尾气,反应生成NaClO2,则该反应中氧化剂与还原剂的物质的量之比为___,氧化产物是___。
(2)粗略测定生成 ClO2 的量实验步骤如下:
a、取下装置 D,将其中的溶液转入 250mL 容量瓶,用蒸馏水洗涤 D 瓶 2~3 次,并将洗涤液一并转移到容量瓶中,再用蒸馏水稀释至刻度。
b、从容量瓶中取出 25.00mL 溶液于锥形瓶中,用 0.1000mol/L 硫代硫酸钠标准溶液滴定(I2+2S2O32-=2I-+S4O62-),指示剂显示终点时共用去 24.00 mL 硫代硫酸钠溶液。
①滴定至终点的现象是___。
②进入装置 D 中的 ClO2 质量为___,与 C 中 ClO2 的理论产量相比,测定值偏低, 可能的原因是_____。
【答案】三颈烧瓶 防倒吸、防堵塞(或平衡气压、安全瓶均可) ![]() 检验有无I2生成,从而证明二氧化氯是否具有氧化性 2:1 O2 溶液由蓝色变为无色,且半分钟内溶液颜色不再改变 0.324g
检验有无I2生成,从而证明二氧化氯是否具有氧化性 2:1 O2 溶液由蓝色变为无色,且半分钟内溶液颜色不再改变 0.324g ![]() 部分没有被吸收、未完全进入D中都导致测定值偏低
部分没有被吸收、未完全进入D中都导致测定值偏低
【解析】
(1)浓硫酸和亚硫酸钠反应生成二氧化硫,A制备二氧化硫,B装置有缓冲作用,能防止倒吸、堵塞;装置C用于制备ClO2,同时还生成一种酸式盐,则C中发生反应![]() ,ClO2是一种黄绿色易溶于水的气体,具有强氧化性,所以D中发生氧化还原反应生成碘,装置D中滴有几滴淀粉溶液,碘遇淀粉变蓝色;装置E用于吸收尾气,反应生成
,ClO2是一种黄绿色易溶于水的气体,具有强氧化性,所以D中发生氧化还原反应生成碘,装置D中滴有几滴淀粉溶液,碘遇淀粉变蓝色;装置E用于吸收尾气,反应生成![]() ,双氧水作还原剂生成氧气,从而防止尾气污染环境;
,双氧水作还原剂生成氧气,从而防止尾气污染环境;
(2)①碘遇淀粉变蓝色,当碘完全反应后溶液变为无色;
②ClO2溶液与碘化钾反应的离子方程式:![]() ,滴定方程:
,滴定方程:![]() ,计算ClO2 质量,ClO2部分没有被吸收、未完全进入D中都导致测定值偏低。
,计算ClO2 质量,ClO2部分没有被吸收、未完全进入D中都导致测定值偏低。
(1)①仪器C的名称为三颈烧瓶,装置B有缓冲作用,所以能防倒吸、防堵塞(或平衡气压、安全瓶均可)。
故答案为:三颈烧瓶;防倒吸、防堵塞(或平衡气压、安全瓶均可);
②装置C用于制备ClO2,同时还生成一种酸式盐,根据元素守恒知,生成的酸式盐为硫酸氢钠,该反应的化学方程式为![]() ;装置D中滴有几滴淀粉溶液,淀粉遇碘变蓝色,根据淀粉是否变色来判断是否有碘生成,从而证明二氧化氯是否具有氧化性,
;装置D中滴有几滴淀粉溶液,淀粉遇碘变蓝色,根据淀粉是否变色来判断是否有碘生成,从而证明二氧化氯是否具有氧化性,
故答案为:![]() ;检验有无I2生成,从而证明二氧化氯是否具有氧化性;
;检验有无I2生成,从而证明二氧化氯是否具有氧化性;
③装置E用于吸收尾气,反应生成![]() ,反应方程式为
,反应方程式为![]() ,该反应中二氧化氯是氧化剂、双氧水是还原剂,则该反应中氧化剂与还原剂的物质的量之比为2:1,氧化产物是氧气,
,该反应中二氧化氯是氧化剂、双氧水是还原剂,则该反应中氧化剂与还原剂的物质的量之比为2:1,氧化产物是氧气,
故答案为:2:1;O2;
(2)①碘遇淀粉变蓝色,当碘完全反应后溶液变为无色,其滴定终点为溶液由蓝色变为无色,且半分钟内溶液颜色不再改变,
故答案为:溶液由蓝色变为无色,且半分钟内溶液颜色不再改变;
②![]() 溶液与碘化钾反应的离子方程式:
溶液与碘化钾反应的离子方程式:![]() ,由
,由![]() ,可得
,可得![]() ,则
,则![]() ,由于滴定待测液只取了
,由于滴定待测液只取了![]() 则生成 ClO2物质的量
则生成 ClO2物质的量 ![]() ,
,![]() ,
,![]() 部分没有被吸收、未完全进入D中都导致测定值偏低,
部分没有被吸收、未完全进入D中都导致测定值偏低,
故答案为:0.324g;![]() 部分没有被吸收、未完全进入D中都导致测定值偏低。
部分没有被吸收、未完全进入D中都导致测定值偏低。


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】5﹣二甲氧基苯酚是重要的有机合成中间体,可用于天然物质白柠檬素的合成,一种以间苯三酚为原料的合成反应如下:

甲醇、乙醚和3,5﹣二甲氧基苯酚的部分物理性质见下表:
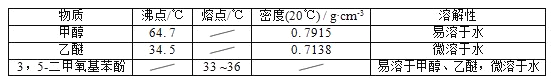
(1)反应结束后,先分离出甲醇,再加入乙醚进行萃取,①分离出甲醇的操作是的______;②萃取用到的分液漏斗使用前需__________________并洗净,分液时有机层在分液漏斗的________填(“上”或“下”)层;
(2)分离得到的有机层依次用饱和NaHCO3溶液、饱和食盐水、少量蒸馏水进行洗涤.用饱和NaHCO3溶液洗涤的目的是__,用饱和食盐水洗涤的目的是______;
(3)洗涤完成后,通过以下操作分离、提纯产物,正确的操作顺序是__(填字母);
a.蒸馏除去乙醚 b.重结晶 c.过滤除去干燥剂 d.加入无水CaCl2干燥
(4)固液分离常采用减压过滤.为了防止倒吸,减压过滤完成后应先________________,再______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
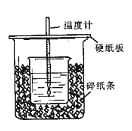
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 ;(填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列溶液均为0.1mol·L-1,有关叙述正确的是( )
A.碳酸钠溶液中c(OH-)=c(H+)+c(H2CO3)+c(CO32-)
B.碳酸钠溶液中滴加盐酸至pH=7,所得溶液的溶质只有NaCl
C.碳酸钠溶液比碳酸氢钠溶液的pH小
D.碳酸氢钠溶液中c(H2CO3)>c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于水的电离平衡H2O![]() H++OH-,下列叙述正确的是
H++OH-,下列叙述正确的是
A.加热,Kw增大,pH不变
B.向水中加入少量盐酸,c(H+)增大,Kw不变
C.向水中加入少量CH3COONa固体,平衡逆向移动,c(H+)降低
D.向水中加入NaOH固体,平衡逆向移动,c(OH-)降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用碳纳米管能够吸附氢气,设计一种新型二次电池,其装置如图所示。关于该电池的叙述不正确的是( )
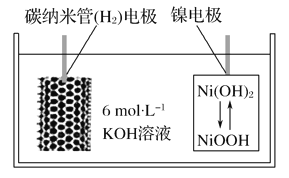
A. 电池放电时K+移向正极
B. 电池放电时负极反应为:H2-2e-+2OH-===2H2O
C. 电池充电时镍电极上NiOOH转化为Ni(OH)2
D. 电池充电时碳纳米管电极与电源的负极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯、苯乙烯均是重要的化工原料。
![]() 工业上可用乙苯催化脱氢方法制备苯乙烯
工业上可用乙苯催化脱氢方法制备苯乙烯
①已知部分化学键的键能如下:
化学键 | C-H | C-C |
| H-H |
键能/(kJ/mol) | 412 | 348 | 612 | 436 |
则![]() +H2(g)的
+H2(g)的![]() ________kJ/mol。
________kJ/mol。
②实际生产中常在恒压条件下掺入高温水蒸气作为反应体系的稀释剂![]() 水蒸气不参加反应
水蒸气不参加反应![]() 。在一定压强、900 K的条件下,乙苯的平衡转化率随着
。在一定压强、900 K的条件下,乙苯的平衡转化率随着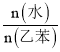 的增大而________
的增大而________![]() 填“增大”“减小”或“不变”
填“增大”“减小”或“不变”![]() 。随着反应的进行,少量积碳会使催化剂活性减弱,水蒸气还有利于恢复催化剂活性,原因是____________
。随着反应的进行,少量积碳会使催化剂活性减弱,水蒸气还有利于恢复催化剂活性,原因是____________![]() 用化学方程式表示
用化学方程式表示![]() 。
。
![]() 苯乙烯可由乙苯和
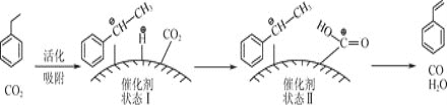
苯乙烯可由乙苯和![]() 催化脱氢制得。其反应历程如下:
催化脱氢制得。其反应历程如下:
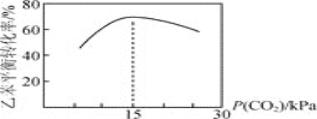
乙苯平衡转化率与![]() 的关系如图所示,当P(CO2)< 15 kPa时,乙苯平衡转化率随着
的关系如图所示,当P(CO2)< 15 kPa时,乙苯平衡转化率随着![]() 增大而增大,其原因是__________,当P(CO2)> 15 kPa时,乙苯平衡转化率随着
增大而增大,其原因是__________,当P(CO2)> 15 kPa时,乙苯平衡转化率随着![]() 增大反而减小,其原因是____________。
增大反而减小,其原因是____________。
![]() 研究表明金属次卟啉二甲酯能够顺利地选择性催化氧化苯乙烯生成苯甲醛,以该反应原理设计成酸性燃料电池,则电池负极的电极反应式为 ________。若该电池消耗标准状况下22.4L的
研究表明金属次卟啉二甲酯能够顺利地选择性催化氧化苯乙烯生成苯甲醛,以该反应原理设计成酸性燃料电池,则电池负极的电极反应式为 ________。若该电池消耗标准状况下22.4L的![]() ,则外电路中理论上转移电子的物质的量为________。
,则外电路中理论上转移电子的物质的量为________。
(4)上海交通大学仇毅翔等研究了不同含金化合物催化乙烯加氢![]() 的反应历程如下图所示:
的反应历程如下图所示:

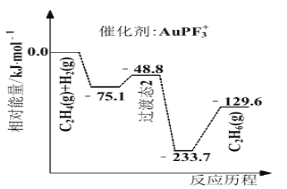
则![]() ____________,催化乙烯加氢效果较好的催化剂是________(选填“
____________,催化乙烯加氢效果较好的催化剂是________(选填“![]() ”或“
”或“![]() ”)。
”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在固定容积的密闭容器中,A和B发生下列反应:A(s)+2B(g)![]() 2C(g) △H>0,在一定条件下达到平衡,若升高温度则达平衡后混合气体的
2C(g) △H>0,在一定条件下达到平衡,若升高温度则达平衡后混合气体的
A.气体的分子数减少B.A的物质的量浓度减小
C.气体的密度减小D.气体的平均相对分子质量增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】扁桃酸衍生物是重要的医药中间体,以物质a为原料合成扁桃酸衍生物b的过程如下:下列说法正确的是( )
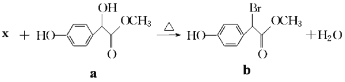
A.物质X是Br2, 物质a转化为b属于取代反应
B.lmol物质a能与3molH2反应,且能在浓硫酸中发生消去反应
C.物质b具有多种能与NaHCO3反应的同分异构体
D.物质b的核磁共振氢谱有四组峰
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com