
【题目】下列物质的制备,不符合工业生产实际的是( )
A.工业上用电解熔融氯化镁制备单质镁
B.工业上用电解饱和食盐水制备氯气
C.工业上用二氧化硅在高温下与焦炭反应制得高纯硅
D.工业上炼铁时,常用石灰石除去铁矿石中的二氧化硅
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案科目:高中化学 来源: 题型:
【题目】汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:
N2(g)+O2(g)![]() 2NO(g),△H>0,已知该反应在240℃,平衡常数K=64×10-4。请回答:
2NO(g),△H>0,已知该反应在240℃,平衡常数K=64×10-4。请回答:
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟后O2的物质的量为0.5mol,则N2的反应速率为______。
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志______.
A.消耗1molN2同时生成1molO2![]() 混合气体密度不变
混合气体密度不变
C.混合气体平均相对分子质量不变D.2v正(N2)=v逆(NO)
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,如图变化趋势正确的是______(填字母序号)。

(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态![]() 与原平衡状态相比,此时平衡混合气中NO的体积分数______
与原平衡状态相比,此时平衡混合气中NO的体积分数______![]() 填“变大”、“变小”或“不变”
填“变大”、“变小”或“不变”![]()
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应______(填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】茉莉花香气的成分有多种,乙酸苯甲酯(![]() )是其中的一种,它可以从茉莉花中提取,也可以用乙醇和甲苯为原料进行人工合成,其合成路线如图:
)是其中的一种,它可以从茉莉花中提取,也可以用乙醇和甲苯为原料进行人工合成,其合成路线如图:
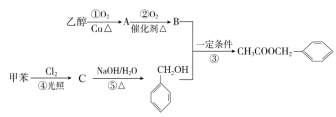
(1)C的结构简式是___,⑤的反应类型:___。
(2)A中所含官能团名称是___,以下化合物在一定条件下,能生成与A中物质相同官能团的是___(填序号),能发生消去反应生成两种烯烃的是___(填序号)
a.![]() b.
b.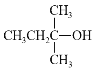 c.
c. d.
d.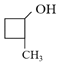
(3)①的化学方程式为___;③的化学方程式为___。
(4)乙酸苯甲酯![]() 有多种同分异构体,其中在苯环上只有一个支链,属于酯类化合物的同分异构体还有___种,其中在酸性条件下水解生成甲酸的同分异构体是:___。
有多种同分异构体,其中在苯环上只有一个支链,属于酯类化合物的同分异构体还有___种,其中在酸性条件下水解生成甲酸的同分异构体是:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】复合氢化物可作为储氢和固体电解质材料,在能源与材料领域得到了深入的研究。
如:①Mg(NH2)2 ②NaNH2 ③ H3N-BH3 ④NaAlH4 ⑤Li3AlH6
(1)复合氢化物升温加热可逐步分解放出氢气,理论上单位质量的上述复合氢化物其储氢能力最低的是__________(填标号)。
(2)在Mg(NH2)2和NaNH2中均存在NH2-,NH2-的空间构型为_________,中心原子的杂化方式为____________。
(3)H3N-BH3与水反应生成一种盐和H2的化学方程式:_____________________。写出基态B原子的价电子轨道表达式:__________________________。
(4)Li3AlH6晶体的晶胞参数为a=b=801.7 pm,c=945.5 pm,α=β=90°、γ=120°,结构如图所示:
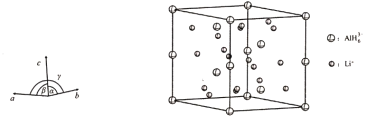
①已知AlH63-的分数坐标为(0,0,0)、(0,0,![]() ),(
),(![]() ,
,![]() ,
,![]() ),(
),(![]() ,
,![]() ,
,![]() ),(
),(![]() ,
,![]() ,
,![]() )和(
)和(![]() ,
,![]() ,
,![]() ),晶胞中Li+的个数为____________。
),晶胞中Li+的个数为____________。
②如图是上述Li3AlH6晶胞的某个截面,共含有10个AlH63-,其中6个已经画出(图中的○),请在图中用○将剩余的AlH63-画出____________。
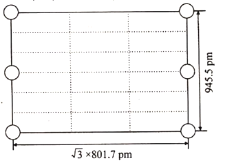
③此晶体的密度为____g·cm-3(列出计算式,已知阿伏加德罗常数约为6.02×1023mol-1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是药物合成的一种中间体,可通过以下方法合成:
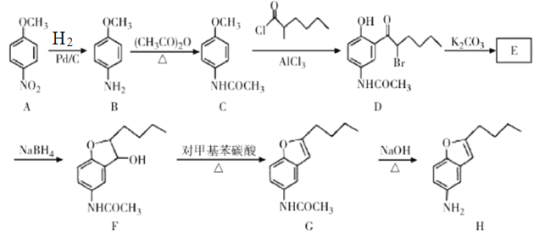
(1)B中官能团名称为____________。
(2)G→H的反应类型为____________。
(3)已知C的一种同分异构体为: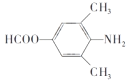 ,下列说法正确的是________。
,下列说法正确的是________。
a.能发生酯化反应
b.能发生银镜反应
c.l mol该物质完全水解产物能消耗3 mol NaOH
d.该分子的核磁共振氢谱中峰面积之比为1:2:6:2
e.其水解产物之一能与FeCl3溶液发生显色反应
(4)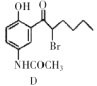 中手性碳原子个数为____________。
中手性碳原子个数为____________。
(5)E的分子是为C14H17O3N,E经还原得到F,写出E→F的反应方程式______________。
(6)已知:①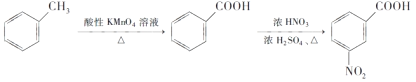
②苯胺(![]() )易被氧化
)易被氧化
请以甲苯和(CH3CO)2O为原料制备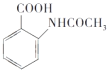 ,写出制备的合成路线流程图(无机试剂任选)______________。
,写出制备的合成路线流程图(无机试剂任选)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀氨水中存在着下列平衡:NH3·H2O![]() NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是( )
NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是( )
①NH4Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤加热 ⑥少量MgSO4固体
A. ①②③⑤B. ③C. ③④⑥D. ③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中A~H均为中学化学中常见的物质,A、B、H为气体,反应①是重要的工业反应,它们之间有如下转化关系(反应中生成的水已略去)。

请回答以下问题:
(1)B是_____,D是_____,G是_____,H是_____(填化学式)。
(2)工业上常利用反应①制取漂白粉,该反应的化学方程式:__________,漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为_________。
(3)A中元素的原子结构示意图为________。
(4)F在溶液中的电离方程式为_________。
(5)上述反应中属于氧化还原反应的是_______(填写序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬铁矿的成分主要为 FeCr2O4 ,另含有少量 Al2O3 和 SiO2 。从铬铁矿中提取铁、铬的化合物,并获得副产物的工艺流程如下:
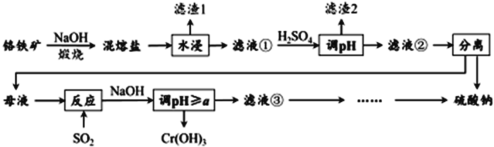
已知:铬铁矿FeCr2O4 中Cr元素在化合价为+3,“ 混熔盐 ” 中含有 Na2CrO4 和 NaFeO2 等成分,其中 NaFeO2 极易水解。试回答下列问题:
(1) “滤渣 1 ”为红褐色沉淀,其化学式为 _________________ ;
(2) 向滤液①中加 H2SO4 “调“ pH ”的目的:一是使 CrO![]() 转化为 Cr2O
转化为 Cr2O![]() ,离子方程式为 __________________ ;二是______________ 。
,离子方程式为 __________________ ;二是______________ 。
(3) “煅烧”铬铁矿时,主要成分反应的化学方程式为 _____________________ 。
(4) 根据下图溶解度(S)~温度(T) 曲线判断,
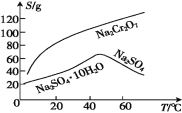
对滤液②进行的最佳“分离”方法为 ________( 填序号 ) 。
A. 蒸发结晶 B. 蒸发浓缩,趁热过滤 C. 蒸发浓缩,冷却结晶,过滤
(5) “反应”的离子方程式为 ____________________________ 。
(6) 已知 25 ℃时,Cr(OH) 3 的溶度积常数 Ksp [Cr(OH) 3 ]= 1.0 × 10 -32 。则使 Cr 3+恰好完全沉淀,即溶液中c(Cr 3+ )=1.0 × 10 -5 mol/L 时,应调节pH 的最小值a为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,浓度均为0.100 mol/L的HA溶液和BOH溶液各20.00 mL,分别用0.100 mol/L NaOH溶液、0.100 mol/L 盐酸进行滴定,滴定过程中pH随滴加溶液体积变化关系如图,两图像关于pH=7呈上下对称。下列说法错误的是
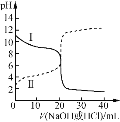
A.曲线Ⅰ表示盐酸滴加到BOH溶液的过程,可用甲基橙作指示剂
B.Ka(HA) =Kb(BOH),交点对应横坐标V< 20.00 mL
C.曲线Ⅰ,滴加溶液到10.00 mL时:c(BOH) > c(Cl-) > c(OH-) >c(H+)
D.曲线Ⅱ,滴加溶液到5.00~10.00 mL时:c(A-) +c(OH-) =c(H+) +c(Na+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com