
【题目】铬铁矿的成分主要为 FeCr2O4 ,另含有少量 Al2O3 和 SiO2 。从铬铁矿中提取铁、铬的化合物,并获得副产物的工艺流程如下:
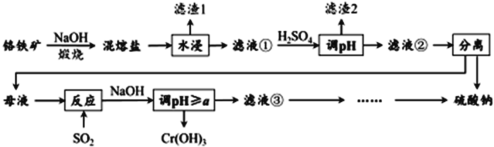
已知:铬铁矿FeCr2O4 中Cr元素在化合价为+3,“ 混熔盐 ” 中含有 Na2CrO4 和 NaFeO2 等成分,其中 NaFeO2 极易水解。试回答下列问题:
(1) “滤渣 1 ”为红褐色沉淀,其化学式为 _________________ ;
(2) 向滤液①中加 H2SO4 “调“ pH ”的目的:一是使 CrO![]() 转化为 Cr2O
转化为 Cr2O![]() ,离子方程式为 __________________ ;二是______________ 。
,离子方程式为 __________________ ;二是______________ 。
(3) “煅烧”铬铁矿时,主要成分反应的化学方程式为 _____________________ 。
(4) 根据下图溶解度(S)~温度(T) 曲线判断,
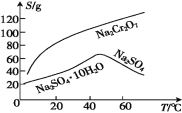
对滤液②进行的最佳“分离”方法为 ________( 填序号 ) 。
A. 蒸发结晶 B. 蒸发浓缩,趁热过滤 C. 蒸发浓缩,冷却结晶,过滤
(5) “反应”的离子方程式为 ____________________________ 。
(6) 已知 25 ℃时,Cr(OH) 3 的溶度积常数 Ksp [Cr(OH) 3 ]= 1.0 × 10 -32 。则使 Cr 3+恰好完全沉淀,即溶液中c(Cr 3+ )=1.0 × 10 -5 mol/L 时,应调节pH 的最小值a为________。
【答案】Fe(OH) 3 2CrO![]() +2H + = Cr2O
+2H + = Cr2O![]() +H2O 使 Al O
+H2O 使 Al O![]() 、 SiO
、 SiO![]() 转化为沉淀,便于过滤分离 4FeCr2O 4 +20NaOH + 7O2
转化为沉淀,便于过滤分离 4FeCr2O 4 +20NaOH + 7O2 ![]() 8Na2CrO4+ 4NaFeO2+10H2O B 3SO2 + Cr2O
8Na2CrO4+ 4NaFeO2+10H2O B 3SO2 + Cr2O![]() + 2H + ===2Cr3 ++ 3SO
+ 2H + ===2Cr3 ++ 3SO![]() + H2O 5
+ H2O 5
【解析】
FeCr2O4、Al2O3、SiO2和氢氧化钠煅烧生成Na2CrO4和NaFeO2、NaAlO2、Na2SiO3;Na2CrO4和NaFeO2、NaAlO2、Na2SiO3中加水,Na2CrO4、NaAlO2、Na2SiO3溶于水,NaFeO2水解为Fe(OH)3沉淀和氢氧化钠,过滤出Fe(OH)3沉淀,滤液中加入硫酸调节pH,使 CrO![]() 转化为Cr2O
转化为Cr2O![]() ,使 Al O
,使 Al O![]() 、SiO
、SiO![]() 转化为沉淀氢氧化铝、硅酸沉淀;根据溶解度(S)~温度(T) 曲线,蒸发浓缩,趁热过滤可分离出硫酸钠,向母液中通入SO2把Cr2O
转化为沉淀氢氧化铝、硅酸沉淀;根据溶解度(S)~温度(T) 曲线,蒸发浓缩,趁热过滤可分离出硫酸钠,向母液中通入SO2把Cr2O![]() 还原为Cr3 +,加入氢氧化钠生成Cr(OH) 3沉淀。
还原为Cr3 +,加入氢氧化钠生成Cr(OH) 3沉淀。
(1) NaFeO2水解为Fe(OH)3沉淀和氢氧化钠,所以“滤渣 1 ”为红褐色沉淀,其化学式为Fe(OH)3;
(2) 向滤液①中加H2SO4调“ pH ”的目的:一是使 CrO![]() 转化为Cr2O
转化为Cr2O![]() ,根据电荷守恒,离子方程式为2CrO
,根据电荷守恒,离子方程式为2CrO![]() +2H += Cr2O
+2H += Cr2O![]() +H2O;二是使 Al O
+H2O;二是使 Al O![]() 、SiO
、SiO![]() 转化为氢氧化铝、硅酸沉淀,便于过滤分离;
转化为氢氧化铝、硅酸沉淀,便于过滤分离;
(3) “煅烧”铬铁矿时,FeCr![]() 8Na2CrO4+ 4NaFeO2+10H2O;
8Na2CrO4+ 4NaFeO2+10H2O;
(4) 根据溶解度(S)~温度(T) 曲线,在较高温度下析出硫酸钠沉淀,对滤液②分离出硫酸钠的最佳“分离”方法为蒸发浓缩,趁热过滤,选B;
(5) “反应”过程是向母液中通入SO2把Cr2O![]() 还原为Cr3 +,反应的离子方程式是3SO2 + Cr2O
还原为Cr3 +,反应的离子方程式是3SO2 + Cr2O![]() + 2H +===2Cr3 ++ 3SO
+ 2H +===2Cr3 ++ 3SO![]() + H2O;
+ H2O;
(6)使Cr 3+恰好完全沉淀,即溶液中c(Cr 3+)=1.0 × 10-5mol/L时,c(OH-)=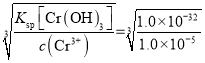 =1.0 × 10-9mol/L,应调节pH 的最小值a为5。
=1.0 × 10-9mol/L,应调节pH 的最小值a为5。


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】金属钼(Mo)在工业和国防建设中有重要的作用。钼的常见化合价为+4、+5、+6。由钼精矿(主要成分是MoS2)制备单质钼和钼酸钠晶体(![]() ),部分流程如下图所示:
),部分流程如下图所示:
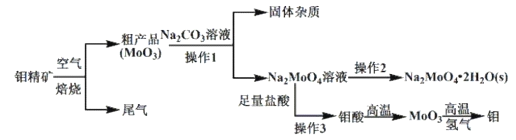
已知:钼酸微溶于水,可溶于碱溶液。
回答下列问题:
(1)钼精矿在空气中焙烧时,发生的主要方程式为_______________________。
(2)钼精矿焙烧时排放的尾气对环境会产生危害,请你提出一种实验室除去该尾气的方法________________________。
(3)操作2的名称为_____________________ 、过滤、洗涤、干燥。
(4)实验室由钼酸经高温制MoO3,所用到的硅酸盐材料仪器的名称是_________。
(5)操作1中,加入碳酸钠溶液充分反应后,碱浸液中c(![]() )=0.80 molL1、c(
)=0.80 molL1、c(![]() )=0.05 molL1,在结晶前需加入Ba(OH)2固体以除去溶液中的
)=0.05 molL1,在结晶前需加入Ba(OH)2固体以除去溶液中的![]() 。当BaMoO4开始沉淀时,SO42的去除率是_________。[Ksp(BaSO4)=1.1
。当BaMoO4开始沉淀时,SO42的去除率是_________。[Ksp(BaSO4)=1.1![]() 1010、Ksp(BaMoO4)=4.0
1010、Ksp(BaMoO4)=4.0![]() 108,溶液体积变化可忽略不计。]
108,溶液体积变化可忽略不计。]
(6)焙烧钼精矿所用装置是多层焙烧炉,下图为各炉层固体物料的物质的量的百分数(![]() )。
)。
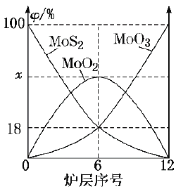
①x=___________。
②焙烧炉中也会发生MoS2与MoO3反应生成MoO2和SO2,还原剂为_________。若反应中转移3mole-,则消耗的还原剂的物质的量为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的制备,不符合工业生产实际的是( )
A.工业上用电解熔融氯化镁制备单质镁
B.工业上用电解饱和食盐水制备氯气
C.工业上用二氧化硅在高温下与焦炭反应制得高纯硅
D.工业上炼铁时,常用石灰石除去铁矿石中的二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)![]() CH3OH(g) △H
CH3OH(g) △H
(1)该反应的ΔH___0(填“>”、“<”或“=”)。
(2)若将等物质的量的CO和H2混合气体充入恒温恒容密闭容器中进行上述反应,下列事实能说明此反应已达到平衡状态的是___。
A.容器内气体密度保持不变
B.混合气体的平均相对分子质量不变
C.生成CH3OH的速率与生成H2的速率相等
D.CO的体积分数保持不变
(3)当按投料比![]() =2,分别在P1、P2、P3压强下,测得不同温度下平衡时CO的平衡转化率如图1。
=2,分别在P1、P2、P3压强下,测得不同温度下平衡时CO的平衡转化率如图1。
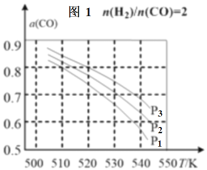
520K时,投料比![]() =2(总物质的量为3mol),维持反应过程中压强P3不变,达到平衡时测得容器体积为0.1L,则平衡常数K=___。
=2(总物质的量为3mol),维持反应过程中压强P3不变,达到平衡时测得容器体积为0.1L,则平衡常数K=___。
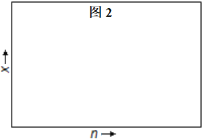
若H2和CO的物质的量之比为n∶1(维持反应过程中压强P3不变),相应平衡体系中CH3OH的物质的量分数为x,请在图2中绘制x随n变化的示意图___。
(4)甲醇合成甲醚的反应为:
Ⅰ.2CH3OH(g)![]() CH3OCH3(g)+H2O(g)(主反应)
CH3OCH3(g)+H2O(g)(主反应)
Ⅱ.2CH3OH(g)![]() C2H4(g)+2H2O(g)(副反应)
C2H4(g)+2H2O(g)(副反应)
反应过程中的能量变化如图3所示。
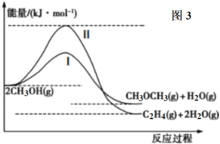
①在一定温度下,在恒容容器中进行合成甲醚的反应,测得CH3OCH3含量随着时间的推移,先增大后减小,请结合碰撞理论说明原因:___。
②在不改变温度的前提下,说出其中一个能增大CH3OCH3选择性的措施:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究某无结晶水的正盐X(仅含有两种短周期元素)的组成和性质,设计并完成下列实验。(气体体积已转化为标准状况下的体积)
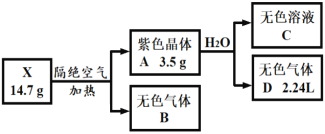
已知:B是空气的主要成分之一;C是一种强碱,且微溶于水,载人宇宙飞船内常用含C的过滤网吸收宇航员呼出的CO2,以净化空气;D遇湿润的红色石蕊试纸变蓝。
(1)B的组成元素在元素周期表中的位置是___。
(2)D分子的空间构型为___。
(3)X受热分解转变成A和B的化学反应方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业中用过量的FeCl3溶液溶解电路板中的铜箔时,会产生大量废液。由该废液回收铜并得到净水剂(FeCl36H2O)的步骤如下:
I.在废液中加入过量铁粉,过滤;
II.向I的滤渣中加入过量试剂A,充分反应后,过滤,得到铜;
III.合并I和II中的滤液,通入足量氯气;
IV.……,得到FeCl36H2O晶体。
(1)用FeCl3溶液腐蚀铜箔的离子方程式是_____________;
(2)试剂A是______;
(3)取少量步骤III所得的溶液于试管中,能够证明通入氯气足量的是______;
a. 检验Cl2的存在 b. 检验Fe3+的存在 c. 检验Fe2+的不存在
(4)完成步骤IV需要用到的实验装置是______(填字母)。
a b
b c
c d
d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取碳酸钠和碳酸氢钠的混合物8.22g,加热到质量不再发生变化,冷却后称其质量为6.36g。回答下列问题:
(1)若取等质量的原混合物溶于水,配成80mL溶液,则c(Na+) = ______mol·L-1;
(2)向(1)所配溶液中逐滴滴加1mol·L-1的稀盐酸至过量,生成的CO2体积(标准状况下)与加入的盐酸体积有如下图关系(不考虑CO2在水中的溶解),则a点消耗盐酸的体积为_______mL。
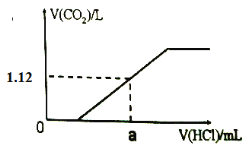
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制480 mL 1 mol· L-1的稀硫酸。可供选用的仪器有:① 胶头滴管② 烧瓶③ 烧杯④ 玻璃棒⑤ 药匙⑥ 量筒⑦ 托盘天平。请回答下列问题:

(1)在容量瓶的使用方法中,下列操作不正确的是________
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,配制溶液不需要干燥
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1~2cm处,用滴管加蒸馏水到标线
D.定容后盖好瓶塞用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶颠倒摇匀多次
(2)该浓硫酸的物质的量浓度为_________mol· L-1。
(3)配制稀硫酸时,还缺少的仪器有________________。
(4)配制480mL 1mol· L-1的稀硫酸需要用量筒量取上述浓硫酸的体积为_______mL。所需量筒的规格为________。(可供选择的量筒有5mL、10mL、20mL、50mL、100mL)
(5)过程中的部分步骤,其中有错误的是(填写序号)____________。

(6)对所配制的稀硫酸进行测定,发现其浓度大于1 mol· L-1,配制过程中下列各项操作可能引起该浓度偏高的原因有___________。
A.定容时,仰视容量瓶刻度线进行定容。
B.将稀释后的硫酸立即转入容量瓶后,紧接着就进行以后的实验操作。
C.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水。
D.转移溶液时,不慎有少量溶液洒到容量瓶外面。
E.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。
(1)把与下面元素有关性质相符的曲线标号填入相应的空格中:
a. 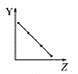 b.
b. 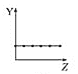 c.
c. 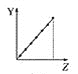 d.
d. 
①第ⅡA族元素的价电子数________。
②第三周期元素的最高化合价________。
③F-、Na+、Mg2+、Al3+的离子半径________。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。据此回答:
①X为___________(名称),Y为____________(元素符号),Z原子结构示意图为________________。
②N的最高价氧化物的水化物的化学式为________________。
③M的最高价氧化物的化学式为________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com