
【题目】盐酸埃洛替尼(I)是一种抑制癌细胞增殖的药物,其合成路线如图:

已知:

(l)下列说法不正确的是___。
A.上述流程中的反应中,D到E为取代反应,E到F为还原反应
B.一定条件下I最多可以和9molH2反应
C.D的氢核磁共振谱图中有7组峰
D.G可以发生水解反应
(2)写出H的结构简式:___。
(3)写出F生成G的化学方程式:___。
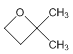
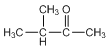
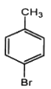
(4)有机物X的分子组成比C发生消去反应后的产物多2个“CH2”,请写出X符合下列条件的同分异构体:___。
①X分子结构中不含碳碳双键和羟基②X核磁共振氢谱有三组峰
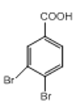
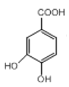
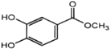
(5)以A和甲醇为原料合成B,请设计合成路线___(用流程图表示,无机试剂任选)。
【答案】BC 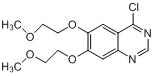
 +
+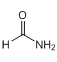 →
→ +CH3OH+H2O
+CH3OH+H2O 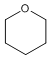 、
、![]() 、
、 、
、 、
、 、
、![]()
![]()
![]()
![]()
![]()
![]()
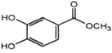
【解析】
B和C发生取代反应,生成D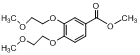 ,D发生硝化反应,根据I的结构确定D中硝基取代的位置,从而确定E的结构:
,D发生硝化反应,根据I的结构确定D中硝基取代的位置,从而确定E的结构: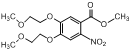 ,E中硝基被还原为氨基得到F
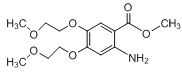
,E中硝基被还原为氨基得到F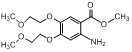 。F生成G的反应发生已知中的反应,
。F生成G的反应发生已知中的反应,  +
+ →
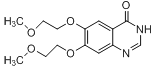
→ +CH3OH+H2O,该反应有两个小分子生成。G的结构简式为
+CH3OH+H2O,该反应有两个小分子生成。G的结构简式为 ,G到H的反应是陌生反应条件,在已知中也没有出现信息,可以根据G和H的分子组成进行对比,结合I结构,确定H的分子结构
,G到H的反应是陌生反应条件,在已知中也没有出现信息,可以根据G和H的分子组成进行对比,结合I结构,确定H的分子结构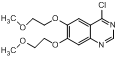 ,据此分析解答。
,据此分析解答。
(5)合成路线设计要注意基团的定位效应,由于甲基为邻对位定位基团,因此需要先将甲基氧化为羧基再引入溴原子。
(l)A.根据分析,上述流程中的反应中,D到E为硝化反应(取代反应),E中硝基被还原为氨基得到F,为还原反应,故A正确;
B.根据I的结构简式, 1molI中含有2mol苯环、2mol双键和1mol三键,2mol苯环消耗6mol H2,2mol双键消耗2mol H2,1mol三键消耗2mol H2,一定条件下最多可以和10molH2反应,故B错误;
C.D的结构简式为 ,共含有10种环境的氢原子,则氢核磁共振谱图中有10组峰,故C错误;
,共含有10种环境的氢原子,则氢核磁共振谱图中有10组峰,故C错误;
D.G的结构简式为 ,分子结构中含有肽键,具有类似于氨基酸的性质,可以发生水解反应,故D正确;
,分子结构中含有肽键,具有类似于氨基酸的性质,可以发生水解反应,故D正确;
答案选BC;
(2)根据分析,H的结构简式: ;
;
(3)根据分析F生成G的反应发生已知中的反应,化学方程式: +
+ →
→ +CH3OH+H2O;
+CH3OH+H2O;
(4)有机物X的分子组成比C发生消去反应后的产物多2个“CH2”, X分子结构中不含碳碳双键和羟基,X核磁共振氢谱有三组峰,说明含有三种不同环境的氢原子,则X符合下列条件的同分异构体:同分异构体为 、
、![]() 、
、 、
、 、
、 、
、![]() ;
;
(5)以A和甲醇为原料合成B,合成路线设计要注意基团的定位效应,由于甲基为邻对位定位基团,因此需要先将甲基氧化为羧基再引入溴原子,合成路线为:
![]()
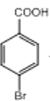
![]()
![]()
![]()
 。
。


科目:高中化学 来源: 题型:
【题目】氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:

(1)氢氧燃料电池能量转化的主要形式是____________________________________________,在导线中电子流动方向为________(用a、b表示)。
(2)负极反应式为________________________________________________________________。
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2===2LiH Ⅱ.LiH+H2O===LiOH+H2↑
①反应Ⅰ中的还原剂是________,反应Ⅱ中的氧化剂是________。
②金属锂吸收的氢气与放出的氢气的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经研究发现白蚁信息素有:![]() (2,4-二甲基-1-庚烯),
(2,4-二甲基-1-庚烯),![]() (3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)8CH==CH—CH==CH(CH2)8CH3。下列说法不正确的是
(3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)8CH==CH—CH==CH(CH2)8CH3。下列说法不正确的是
A.2,4-二甲基1庚烯的分子式为C9H18
B.2,4-二甲基-1-庚烯与3,7-二甲基-1-辛烯互为同系物
C.以上三种信息素均能使溴的四氯化碳溶液褪色
D.1 mol家蚕的性信息素与1 mol Br2加成,产物只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制比的过程如图所示。下列叙述正确的是( )

A.H2的标准燃烧热△H<-(△H1+△H2)
B.过程I适当降低反应体系温度,反应更有利
C.过程II中3mo1FeO(s)的总能量高于lmolFe3O4(s)
D.增加铁氧化合物的质量可以显著提高循环制H2的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)1mol Na2O2固体与水完全反应时转移的电子数_____________,反应的离子方程式为________________。
(2)工业上由辉铜矿生产铜的主要反应为:Cu2S+O2![]() 2Cu+SO2,该反应中被还原的元素是__________(填元素符号)。
2Cu+SO2,该反应中被还原的元素是__________(填元素符号)。
(3)反应(2)中产生的SO2尾气可用NaOH溶液吸收,若用1L 1mol/L的NaOH溶液吸收标准状况下22.4L SO2,反应的离子方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶于水时会发生电离产生自由移动的离子,电导率变化一定程度上可以反映溶液中自由移动的离子浓度变化。溶液中自由移动的离子浓度越大,电导率就越大。如图是向20mL0.01mol/LBa(OH)2溶液中滴入了2滴酚酞溶液,然后向Ba(OH)2溶液中匀速滴加0.2mol/LH2SO4溶液,获得电导率随时间变化的曲线图。
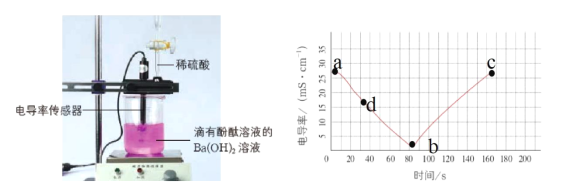
(1)0-80s观察到的实验现象是_____。
(2)写出该实验中的离子方程式_____。
(3)截至b点,加入0.2molL-1H2SO4溶液的体积为_____mL,解释b点的电导率不等于零和bc段电导率又增加的原因____。
(4)在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列分析正确的是(_____)(多选题)
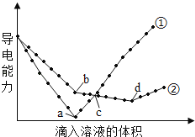
A.①代表滴加H2SO4溶液的变化曲线
B.b点,溶液中大量存在的离子是Na+、OH-
C.a、d两点对应的溶液均显中性
D.c点,两溶液中含有相同量的OH-
E.H+导电能力比Na+强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含铜化合物的化学式为Cux(OH)y(CO3)z(Cu为+2价)。取该样品22.2 g,充分加热后,得到黑色固体氧化铜16.0 g,则该物质的化学式为
A.Cu2(OH)4CO3B.Cu3(OH)4CO3
C.Cu2(OH)2CO3D.Cu4(OH)2(CO3)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用固体表面催化工艺进行NO分解的过程如图所示(![]() N
N![]() O)。下列说法不正确的是( )
O)。下列说法不正确的是( )
![]()
A.NO属于极性分子
B.含有非极性共价键
C.过程②释放能量,过程③吸收能量
D.标准状况下,NO分解生成5.6LN2转移电子数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、 Y、 Z、 M、 Q、 R为短周期元素, 其原子半径和最外层电子数之间的关系如图所示。下列说法错误的是

A.元素的金属性: Q<RB.R 的氧化物可能含共价键
C.热稳定性: ZX3<YX4D.X2M 的水溶液露置于空气中易变质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com