
【题目】将一小块钠投入盛饱和澄清石灰水的烧杯里,不可能观察到的现象是
A.钠熔成小球并在液面上游动
B.溶液底部有银白色物质生成
C.有气体生成
D.溶液变浑浊
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】有氯化钠和碘化钠的混合物共26.7 g,溶于水,通入足量氯气后,蒸干、灼烧,固体质量变为 17.55 g。
(1)原混合物中碘化钠的质量是________。
(2)原混合物中氯化钠的质量分数是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分离或除杂的方法正确的是
A.分离硬脂酸钠和甘油,加饱和食盐水盐析,过滤
B.除去乙酸乙酯中的乙酸,加烧碱溶液,蒸馏
C.分离苯酚和酒精混合液,分液
D.除去淀粉溶液中NaCl,过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)请写出分子式为C3H5Cl且含碳碳双键的所有同分异构体_______________________。
(2)有机物w分子式为C4H6,且其等效氢只有一种,请写出w所有的结构简式______________。
(3)已知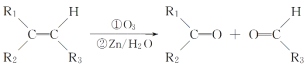 ,某含四元环的有机物发生这个反应后,得到
,某含四元环的有机物发生这个反应后,得到![]() 和
和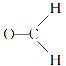 各1mol,请写出该有机物的结构简式_____________。
各1mol,请写出该有机物的结构简式_____________。
(4)已知![]() +NaOH
+NaOH![]() R—CH=CH2+NaCl+H2O请设计由乙烯制备乙炔的方案,无机试剂任意选择,用如下流程图表示反应的流程
R—CH=CH2+NaCl+H2O请设计由乙烯制备乙炔的方案,无机试剂任意选择,用如下流程图表示反应的流程
如:CH3-CH3![]() CH3-CH2Cl
CH3-CH2Cl
______________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)AgNO3光照易分解,生成Ag和红棕色气体等物质,其光照分解反应的化学方程式为___________________________________。
(2)已知Ksp(AgCl)=1.8×10-10,若向50mL0.018mol·L-1的AgNO3溶液中加入50mL0.020mol·L-1的盐酸,混合后溶液中Ag+的浓度为________mol·L-1,pH为________。
(3)25℃,在0.10mol·L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图(忽略溶液体积的变化、H2S的挥发)。pH=13时,溶液中的c(H2S)+c(HS-)=________mol·L-1。

(4)25℃,0.10mol·L-1CH3COONH4溶液中粒子浓度由大到小的顺序为____________________(已知醋酸和一水合氨的电离常数相等)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N元素是植物生长的必需元素,含氮化合物在工农业生产以及生活中都发挥着重要作用。
(1)氧化亚氮(N2O)是一种强温室气体,且易转换成颗粒污染物。研究氧化亚氮分解对环境保护有重要意义。污水生物脱氮过程中,在异养微生物催化下,硝酸铵可分解为N2O和另一种产物,该反应的化学方程式为____。
(2)氮的氧化物既是空气的重要污染物,同时也是重要的化工原料。某化学课外小组查阅资料后得知2NO(g)+O2(g)![]() 2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
①2NO(g)![]() N2O2(g)(快)ΔH1<0 K1
N2O2(g)(快)ΔH1<0 K1
②N2O2(g)+O2(g)![]() 2NO2(g)(慢)ΔH2<0 K2
2NO2(g)(慢)ΔH2<0 K2
反应2NO(g)+O2(g)![]() 2NO2(g)的ΔH=__(用含ΔH1和ΔH2的式子表示),K=___(用含K1和K2的式子表示)。决定2NO(g)+O2(g)
2NO2(g)的ΔH=__(用含ΔH1和ΔH2的式子表示),K=___(用含K1和K2的式子表示)。决定2NO(g)+O2(g)![]() 2NO2(g)的反应速率的是反应_____(填序号),则反应①的活化能E1,与反应②的活化能E2的大小关系为E1___(填“>”“<”或“=”)E2。
2NO2(g)的反应速率的是反应_____(填序号),则反应①的活化能E1,与反应②的活化能E2的大小关系为E1___(填“>”“<”或“=”)E2。
(3)在373 K时,向体积为2 L的恒容真空容器中通入0.40 mol NO2,发生反应:2NO2(g)![]() N2O4(g) ΔH=57.0 kJ·mol1。测得NO2的体积分数[φ(NO2)]与反应时间(t)的关系如下表:
N2O4(g) ΔH=57.0 kJ·mol1。测得NO2的体积分数[φ(NO2)]与反应时间(t)的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 |
φ(NO2) | 1.0 | 0.75 | 0.52 | 0.40 | 0.40 |
①0~20 min内,v(N2O4)=__________。
②上述反应中,v正(NO2)=k1·c2(NO2),v逆(N2O4)=k2·c(N2O4),其中k1、k2为速率常数,则373 K时,k1、k2的数学关系式为____。改变温度至T1时k1=k
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比pH的定义,对于稀溶液可以定义pC=-lgC,pKa=-lgKa。常温下,某浓度H2A溶液在不同pH值下,测得pC(H2A)、pC(HA-)、pC(A2-)变化如图所示。下列说法正确的是

A. pH=3.50时,c(H2A)>c(HA-)>c(A2-)
B. 常温下,pKa1(H2A)=5.30,pKa2(H2A)=0.80
C. b点时,![]() =104.50
=104.50
D. pH=3.00~5.30时,c(H2A)+c(HA-)+c(A2-)先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“摩尔庄园”是一款专门为7﹣12岁儿童设计的安全健康益智网页游戏,它和我们高中化学的“摩尔”没有任何的关系,我们所学的“摩尔”其实是
A.国际单位制中的一个物理量
B.摩尔是表示物质的量
C.摩尔是物质的量的单位
D.摩尔是表示物质数量的单位
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率,请回答下列问题。
(1)工业合成氨反应:N2+3H2 ![]() 2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1 mol N2完全反应生成NH3可放出92 kJ热量。如果将10 mol N2和足量H2混合,使其充分反应,放出的热量________(填“大于”、“小于”或“等于”)920kJ。
2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1 mol N2完全反应生成NH3可放出92 kJ热量。如果将10 mol N2和足量H2混合,使其充分反应,放出的热量________(填“大于”、“小于”或“等于”)920kJ。
(2)实验室模拟工业合成氨时,在容积为2 L的密闭容器内,反应经过10 min后,生成10 mol NH3
①则用N2表示的化学反应速率为__________________。
②一定条件下,当该反应进行到最大限度时,下列说法正确的是______(填编号)
a.N2的转化率达到最大值
b.N2、H2和NH3的体积分数之比为1 : 3 : 2
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
(3)某实验小组同学进行如下图所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度_______(填“升高”或“降低”)。反应过程____(填“①”或“②”)的能量变化可用图表示。

(4)用CH4和O2组合形成的质子交换膜燃料电池的结构如图:
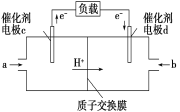
①则d电极是____(填“正极” 或“负极”),c电极的电极反应式为_____________________________。
②若线路中转移2 mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为______L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com