
【题目】能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率,请回答下列问题。
(1)工业合成氨反应:N2+3H2 ![]() 2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1 mol N2完全反应生成NH3可放出92 kJ热量。如果将10 mol N2和足量H2混合,使其充分反应,放出的热量________(填“大于”、“小于”或“等于”)920kJ。
2NH3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1 mol N2完全反应生成NH3可放出92 kJ热量。如果将10 mol N2和足量H2混合,使其充分反应,放出的热量________(填“大于”、“小于”或“等于”)920kJ。
(2)实验室模拟工业合成氨时,在容积为2 L的密闭容器内,反应经过10 min后,生成10 mol NH3
①则用N2表示的化学反应速率为__________________。
②一定条件下,当该反应进行到最大限度时,下列说法正确的是______(填编号)
a.N2的转化率达到最大值
b.N2、H2和NH3的体积分数之比为1 : 3 : 2
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
(3)某实验小组同学进行如下图所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度_______(填“升高”或“降低”)。反应过程____(填“①”或“②”)的能量变化可用图表示。

(4)用CH4和O2组合形成的质子交换膜燃料电池的结构如图:
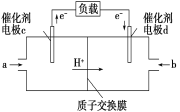
①则d电极是____(填“正极” 或“负极”),c电极的电极反应式为_____________________________。
②若线路中转移2 mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为______L。
【答案】小于 0.25mol/(L·min) ad 降低 ① 正极 CH4-8e-+2H2O=CO2+8H+ 11.2
【解析】
(1)依据合成氨的反应是可逆反应作答;
(2)①根据![]() ,结合反应速率之比等于系数之比求算;
,结合反应速率之比等于系数之比求算;
②化学平衡状态是正逆反应速率相等,各组分浓度保持不变的状态,反应达到最大限度,据此分析;
(3)Al与盐酸反应放出热量,Ba(OH)28H2O与NH4Cl反应吸收热量,图2中反应物总能量大于生成物总能量,为放热反应;
(4)①依据原电池工作图中电子流出的方向判断正负极;
②根据电极反应式列出关系式计算氧气的消耗量;
(1)合成氨是可逆反应,反应物不能完全转化,所以将10 mol N2和足量H2混合,使其充分反应,放出的热量小于920kJ;
(2)①![]() ,又因为化学反应中,各物质表示的反应速率之比等于其系数之比,则v(N2)=
,又因为化学反应中,各物质表示的反应速率之比等于其系数之比,则v(N2)=![]() v(NH3)=
v(NH3)= ![]() ×0.5mol/(Lmin) = 0.25mol/(Lmin),
×0.5mol/(Lmin) = 0.25mol/(Lmin),
故答案为:0.25mol/(Lmin);
②a.N2的转化率达到最大值,则说明反应达到平衡状态,a项正确;
b. N2、H2和NH3的体积分数之比为1 : 3 : 2,不能说明各物质的浓度保持不变,无法说明反应达到平衡状态,b项错误;
c.体系内气体的总质量保持不变,总体积保持不变,则气体的密度始终保持不变,因此密度不变不能说明反应达到平衡状态,c项错误;
d. 因反应是气体分子数减小的体系,体系内气体的总质量保持不变,若物质的平均相对分子质量保持不变时,则气体的总物质的量保持不变,可说明反应达到平衡状态,d项正确;
故答案选ad;
(3)Ba(OH)28H2O与NH4Cl反应吸收热量,则反应后②中的温度降低;Al与盐酸反应放出热量,又从图中能量变化图可以看出,反应物的总能量高于生成物的总能量,则可表示反应①的能量变化;
(4)①因c是电子流出的一极,则c为负极,d为正极,甲烷具有还原性,在负极上发生氧化反应生成CO2,电极反应式为:CH4-8e-+2H2O=CO2+8H+,故答案为:正极;CH4-8e-+2H2O=CO2+8H+
②原电池中正极电极反应为2O2+8H++8e-=4H2O,当转移2mol电子时,则消耗氧气物质的量为0.5mol,体积为0.5mol×22.4L/mol=11.2 L。


科目:高中化学 来源: 题型:
【题目】将一小块钠投入盛饱和澄清石灰水的烧杯里,不可能观察到的现象是
A.钠熔成小球并在液面上游动
B.溶液底部有银白色物质生成
C.有气体生成
D.溶液变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由二氧化碳、氢气、一氧化碳组成的混合气体在同温、同压下与氮气的密度相同。则该混合气体中二氧化碳、氢气、一氧化碳的体积比可能为
A. 29 : 8 : 13B. 13 : 8 : 13C. 22 : 1 : 14D. 26 : 18 : 13
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。完成下列填空:
(1)写出电解饱和食盐水的离子方程式________________。
(2)离子交换膜的作用为____________________。
(3)精制饱和食盐水从图中________位置补充,氢氧化钠溶液从图中________位置流出。(选填“a”、“b”、“c”或“d”)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O,以下叙述正确的是( )
5NaCl+NaClO3+3H2O,以下叙述正确的是( )
A. Cl2既做氧化剂又做还原剂
B. 被氧化的氯原子和被还原的氯原子的物质的量之比为5∶1
C. Cl2是氧化剂,NaOH是还原剂
D. 氧化剂得电子数与还原剂失电子数之比为5∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是

A. 加入Na2SO4可使溶液由a点变到b点
B. 通过蒸发可以使溶液由d点变到c点
C. d点无BaSO4沉淀生成
D. a点对应的Ksp大于c点对应的Ksp
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法正确的是( )
A. 将 (NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀可知二者均可使人中毒
B. 塑料的老化是由于与空气中的氧气发生了加成反应
C. 粮食酿酒的过程:淀粉![]() 葡萄糖
葡萄糖![]() 乙醇
乙醇
D. 可以用足量氢氧化钠溶液加热的方法区分地沟油(分离过的餐饮废弃油)与矿物油(汽油、煤油、柴油等)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是原子序数依次增大的短周期主族元素。已知W原子的最外层电子数是电子层数的2倍,Y原子次外层电子数与其它各层电子总数相等,W和X的原子序数之和等于Z的原子序数。下列说法正确的是
A. 含氧酸的酸性:Z>W
B. 在一定条件下W的单质能与Y的最高价氧化物对应的水化物反应
C. 四种元素均能与氢元素形成共价键
D. 简单离子半径:X>Y>Z
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com