
将5.4g Al投入200.0mL 2.0mol•L﹣1的某溶液中有氢气产生,充分反应后有金属剩余.该溶液可能为( )
|
| A. | HNO3溶液 | B. | Ba(OH)2溶液 | C. | H2SO4溶液 | D. | HCl溶液 |
| 铝的化学性质;化学方程式的有关计算.. | |
| 专题: | 化学反应中的能量变化. |
| 分析: | 200.0mL 2.0mol•L﹣1的某溶液中溶质的物质的量为0.2L×2.0mol•L﹣1=0.4mol,Al的物质的量为 |
| 解答: | 解:200.0mL 2.0mol•L﹣1的某溶液中溶质的物质的量为0.2L×2.0mol•L﹣1=0.4mol,Al的物质的量为 A、因Al与HNO3溶液不生成氢气,则不符合题意,故A错误; B、由2Al+2OH﹣+2H2O═2AlO2﹣+3H2↑,0.2molAl与0.4molBa(OH)2溶液反应时,碱过量,故B错误; C、由2Al+6H+═2Al3++3H2↑,0.2molAl与0.4molH2SO4溶液,硫酸过量,故C错误; D、由2Al+6H+═2Al3++3H2↑,0.2molAl与0.4molHCl溶液,Al过量,故D正确; 故选D. |
| 点评: | 本题考查铝的化学性质,明确铝与酸碱发生的化学反应是解答的关键,并注意利用量来判断过量问题即可解答. |


科目:高中化学 来源: 题型:
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
| 阳离子 | Ag+ Na+ |
| 阴离子 | NO3- SO42- Cl- |
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、B、C三种溶液,电极均为石墨电极。

接通电源,经过一端时间后,测得乙中c电极质量增加了27克。常温下各烧杯中溶液的pH与电解时间t的关系图如上。据此回答下列问题:
(1)M为电源的 极(填写“正”或“负”),甲、乙电解质分别为 、 (填写化学式)。
(2)要使电解后丙中溶液恢复到原来的状态,应加入 物质。(填写化学式)
(3) 若电解后甲溶液的体积为25L,且产生的气体全部逸出。该溶液常温时的pH为 。
(4)写出乙烧杯中发生反应的离子方程式
(5)写出甲烧杯中发生反应的离子方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
单质、氧化物、酸、碱和盐的相互关系,可以用图简单表示,限选择铁、碳、氧气、盐酸、氧化钙、二氧化碳、水、氢氧化钙8种物质作为反应物,将图中指定序号的转变用化学方程式表示(所写化学方程式不得重复)。
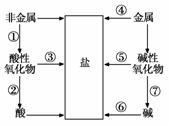
①C+O2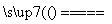 CO2
CO2
②________________________________________________________________________
③________________________________________________________________________
④________________________________________________________________________
⑤________________________________________________________________________
⑥________________________________________________________________________
⑦________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
质量分数为n的NaOH溶液,其物质的量浓度为amol/L,加热蒸发水使其质量分数变为2n,此时,该溶液中的物质的量浓度为bmol/L,则a与b的关系正确的是( )
|
| A. | b>2a | B. | b<2a | C. | b=2a | D. | a=2b |
查看答案和解析>>
科目:高中化学 来源: 题型:
相同条件下,相同浓度的盐酸分别与镁、铝、铁3种金属恰好完全反应,产生相同体积的氢气(相同状况下),则下列说法正确的是( )
|
| A. | 开始时,产生氢气的速率相同 |
|
| B. | 参加反应的金属的质量相同 |
|
| C. | 所得溶液的质量相等 |
|
| D. | 参加反应的金属的质量比为12:9:28 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组为了了解HCl、NaHSO4、NaHCO3在水溶液中的电离情况,进行了下列实验;
①分别测定了0.1mol/L的HCl、NaHSO4、NaHCO3溶液中H+的物质的量浓度,HCl溶液中c(H+)=0.1mol/L,NaHSO4溶液中c(H+)=0.1mol/L,而NaHCO3溶液中H+的物质的量浓度远远小于0.1mol/L.
②取少量NaHSO4溶液于试管中,滴入BaCl2溶液有不溶于硝酸的白色沉淀生成.
③取少量NaHCO3溶液于试管中,滴入几滴BaCl2无明显现象.
(1)请根据该小组同学的实验结果,分别写出NaHSO4、NaHCO3在水溶液中的电离方程式:
①NaHSO4: NaHSO4=Na++H++SO42﹣ 、
②NaHCO3: NaHCO3═Na++HCO3﹣ 、
(2)写出②中反应的离子方程式: SO42﹣+Ba2+=BaSO4↓ .
查看答案和解析>>
科目:高中化学 来源: 题型:
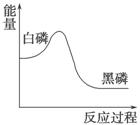
白磷在高压下隔绝空气加热后急速冷却,可得钢灰色固体黑磷,其转化过程中能量变化如图所示。下列叙述中正确的是
A.黑磷比白磷稳定 B.黑磷与白磷互为同分异构体
C.白磷转化为黑磷是氧化还原反应
D.白磷转化为黑磷是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)已知2 mol氢气燃烧生成液态水时放出572 kJ热量,反应方程式是2H2(g)+O2(g)===2H2O(l) 请回答下列问题:
①该反应的生成物能量总和________(填“大于”、“小于”或“等于”)反应物能量总和。
②若2 mol氢气完全燃烧生成水蒸气,则放出的热量________(填“>”、“<”或“=”)572 kJ。
(2)FeS2焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
2SO2(g)+O2(g)  2SO3(g) ΔH1=-197 kJ·mol-1;
2SO3(g) ΔH1=-197 kJ·mol-1;
H2O(g)===H2O(l) ΔH2=-44 kJ·mol-1;
2SO2(g)+O2(g)+2H2O(g)===2H2SO4(l) ΔH3=-545 kJ·mol-1
则SO3(g)与H2O(l)反应的热化学方程式是_________ _______。
(3)已知下列反应的热化学方程式:
①6C (s)+5H2(g)+3N2(g)+9O2(g)===2C3H5(ONO2)3(l) ΔH1
②2H2(g)+O2(g)===2H2O(g) ΔH2
③C(s)+O2(g)===CO2(g) ΔH3
则反应4C3H5(ONO2)3(l)===12CO2(g)+10H2O(g)+O2(g)+6N2(g)的ΔH为____ ____。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.液态HCl不导电,所以HCl是非电解质
B.NH3、CO2的水溶液均导电,所以NH3、CO2均是电解质
C.铜、石墨均导电,所以它们都是电解质
D.蔗糖在水溶液中或熔融时均不导电,所以是非电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com