
组同学发现84消毒液与洁厕剂(主要成分为盐酸)室温下混和有Cl2生成,于是尝试在实验室利用该反应原理制取Cl2。
(1)若用次氯酸钙、浓盐酸为原料,利用下图装置制取Cl2。装置中仪器a的名称为 。甲同学想证明Cl2溶于水有酸性物质生成,将发生装置产生的气体直接通入适量水中,并加入NaHCO3粉末,有无色气泡产生。乙同学认为不合理,理由是 。又知:室温下H2CO3的电离常数K1=4.2×10-7,K2=5.6×10-11,则pH为8.0的NaHCO3溶液中[CO32-]:[HCO3-]= 。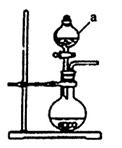
(2)经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。设计如下装置制备无水FeCl3。
①下列操作步骤的正确排序为 (填字母)。
| A.体系冷却后,停止通入Cl2 |
| B.通入干燥的Cl2赶尽装置中的空气 |
| C.在铁屑下方加热至反应完成 |
| D.用干燥的H2赶尽Cl2 |
 NaClO3+3H2
NaClO3+3H2 ,
, +Cl2
+Cl2 +2NaCl+2H2O。
+2NaCl+2H2O。| 物质 | 熔点/℃ | 沸点/℃ |
| C1O2 | -59 | 11 |
| Cl2 | -107 | -34.6 |
(1)分液漏斗(2分)
制取的氯气中含有HCl气体,HCl溶于水后能与NaHCO3反应产生气泡(2分)5.6×10-3(3分)
(2)①ebcad(3分)
②缺少尾气吸收装置(2分)
(3)Cl2(2分)Cl2、NaCl(2分)
将生成的气体冷水浴降温使ClO2液化分离出来(2分)
解析试题分析:(1)根据实验装置图可知仪器a为分液漏斗;因为浓盐酸具有挥发性,制取的Cl2中含有HCl,HCl溶于水后能与NaHCO3反应产生CO2气体;HCO3?电离产生CO32?:HCO3? CO32?+H+,K2=[CO32?][H+]/[HCO3?]=5.6×10-11, 可得[CO32-]:[HCO3-]= K2/[H+]=5.6×10-11/10-8=5.6×10-3
CO32?+H+,K2=[CO32?][H+]/[HCO3?]=5.6×10-11, 可得[CO32-]:[HCO3-]= K2/[H+]=5.6×10-11/10-8=5.6×10-3
(2)①首先检验装置的气密性,为防止空气影响实验,通入干燥的Cl2赶尽装置中的空气,然后加热铁屑进行Fe与Cl2的反应,反应完成后,等到体系冷却后,停止通入Cl2,最后用干燥的H2赶尽Cl2,所以正确顺序为:ebcad
②尾气中含有Cl2,有毒污染环境,需要进行尾气处理,所以该实验装置存在的明显缺陷是缺少尾气吸收装置。
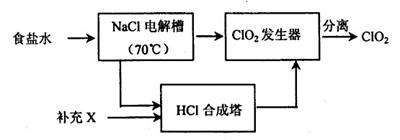
(3)根据题目所给信息,电解NaCl溶液和NaClO3与HCl反应的化学方程式,可知Cl2产量少,所以需要补充的物质X为为Cl2;NaClO3与HCl反应能生成Cl2和NaCl,所以能参与循环的物质是Cl2、NaCl;因为ClO2的沸点为11℃,所以将生成的气体冷水浴降温,可使使ClO2液化变为液体,分离出来。
考点:本题考查基本仪器、基本操作、实验步骤、离子浓度的计算、实验方案的设计与分析。


科目:高中化学 来源: 题型:填空题
(11) 某校化学兴趣小组的同学对硝酸盐的受热分解进行探究。他们设计了如下装置分别加热了Ca(NO3)2、Cu(NO3)2、AgNO3三种固体。(加热及夹持装置未画出)
(1)甲同学加热的是Ca(NO3)2。加热过程发现:装置②中产生 气泡,部分石蕊试液被压至装置③中;用带火星的木条检验②中的气体,木条复燃;分析装置①中剩余的固体得知,剩余固体中含有N元素,且显+3价。请写出Ca(NO3)2受热分解后生成产物的化学式: 、 。
(2)乙同学加热的是Cu(NO3)2。加热过程发现:装置②中也有气泡产生,但在上升的过程中消失。石蕊试液逐渐变为红色,液体几乎不被压至装置③中。装置①中的固体逐渐变为黑色。请写出Cu(NO3)2受热分解的化学方程式: ;
(3)丙同学加热的是AgNO3。加热过程发现:装置②中也有气泡产生,但在上升的过程中气泡部分消失,剩余的气体也能使带火星的木条复燃。石蕊试液也逐渐变为红色,有少量液体被压至装置③中。装置①中的固体逐渐变为黑色。丙同学据此写出了AgNO3受热分解可能的两种化学方程式:
(Ⅰ)4AgNO3  2Ag2O+4NO2↑+O2↑ (Ⅱ)2AgNO3
2Ag2O+4NO2↑+O2↑ (Ⅱ)2AgNO3 2Ag+2NO2↑+O2↑。
2Ag+2NO2↑+O2↑。
Ⅰ、Ⅱ中正确的是 ,并说明理由: 。
请你设计一个简单的实验证明你的结论是正确的: 。
(4)由上述3个实验的结果,请你推测硝酸盐受热分解的规律: 。
(5)标况下如丙同学操作,称量ag硝酸银,受热完全分解后,读取量筒体积为bml,求硝酸银的分解率:____________(化简成整数比例关系,可不用化成小数)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业上可用铜屑和浓硝酸为原料制取硝酸铜。在实际生产中,先把铜屑在空气中灼烧,再跟用等体积水稀释的浓硝酸反应来制取硝酸铜。请回答下列问题:
(1)不宜于用铜屑直接与硝酸反应来制取硝酸铜的原因是 。
(2)浓硝酸用等体积水稀释的目的是 。
(3)要得到硝酸铜晶体,应选用 。
(4)反应中硝酸表现出 性。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
钢化玻璃是一类性能良好的玻璃,它可以克服玻璃质脆易碎的缺点。离子交换法是玻璃进行钢化的一种重要方法。将普通的钠钙玻璃在碳酸钾的强化盐(475 ℃)中浸泡3.5小时后即可制得。下图是离子交换法的示意图。
(1)普通玻璃是由石英砂、__________和__________高温熔融而成。
(2)普通玻璃表面产生裂纹后非常容易破碎,清除表面裂纹的物质之一是氢氟酸,写出氢氟酸与玻璃反应的化学方程式________________。
(3)玻璃进行钢化过程中,离子交换是__________(填“物理变化”或“化学变化”)。
(4)在玻璃进行钢化处理时,能否用碳酸氢钾代替碳酸钾,__________(填“能”或“不能”),原因是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
一同学分析硫元素的化合价有-2、0、+4、+6,而硫单质处于中间价态,所以硫应该既有氧化性,又有还原性。该同学欲探究硫的还原性,下面是该同学的实验探究过程,请解答其中的问题。
(1)该同学应该选择________(填“氧化剂”或“还原剂”)进行实验探究。
(2)该同学用红热的玻璃棒引燃了石棉网上的硫粉,硫粉开始燃烧,反应的化学方程式为________________________________________________
(3)该同学欲验证硫燃烧产物的性质,请你帮助他选择合适的试剂,并说明原因。
| A.新制的氯水 | B.品红溶液 | C.滴有酚酞的NaOH稀溶液 | D.H2S气体 |
| 性质 | 试剂 | 化学方程式 |
| 漂白性 | | |
| 氧化性 | | |
| 还原性 | | |
| 酸性氧化物 | | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知A、B、C、D、E、F、G、H可以发生如图所示的转化,反应中部分生成物已略去。其中,A、G为同一主族元素的单质,B、C、H在通常情况下为气体,化合物C是一种形成酸雨的大气污染物。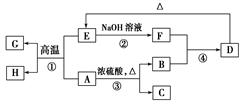
请完成以下填空:
(1)H的名称是________。
(2)E的两种用途是________、________。
(3)反应③的化学方程式是________。
(4)反应④的离子方程式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
一些常见化学反应可用下式表示 A + B → C+D+H2O 其中A为单质 (必要时可加热),请你根据下面的提示回答下列问题:
(1)若A、C、D均含有氯元素,则A与B溶液反应的离子方程式为: 。
(2)若C、D均为气体且有一种为红棕色,则B是 。
(3)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B反应的化学方程式为: 。
如何稀释B的浓溶液 。
(4) 若A为紫红色的固体,D为无色无味的气体,则A与B溶液反应的离子方程式为: 。若产生标准状况下4.48L的D气体,则被还原的B的物质的量是 mol。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
硅酸钠是一种重要的无机功能材料,某研究性学习小组设计的利用海边的石英砂(含氯化钠、氧化铁等杂质)制备硅酸钠的流程如下: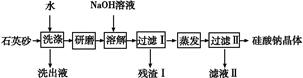
(1)石英砂加水洗涤的目的是 。
研磨后加入NaOH溶液溶解的离子方程式是 。
(2)实验室进行蒸发操作要用到的仪器有铁架台(含铁圈)、 和 。
(3)残渣Ⅰ的成分是 (填化学式)。将残渣Ⅰ溶于盐酸,再加入NaOH溶液得到沉淀,将该沉淀加入到NaClO和NaOH混合溶液中可制得一种优质净水剂,完成反应的离子方程式: + ClO-+ OH- + Cl-+ H2O
+ Cl-+ H2O
(4)按上述流程制得的硅酸钠晶体可表示为Na2O·nSiO2,若石英砂的质量为10.0 g,其中含SiO2的质量分数为90%,最终得到硅酸钠晶体15.2 g,则n= 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氯水具有多种性质,根据新制氯水分别与如图五种物质发生的反应填空(氯水足量):
(1)a、b、c中反应的离子方程式为: 。
e中的化学反应方程式为 。上述反应中发生了氧化还原反应的是: (填“a”、“b”、“c”或“e”)。
(2)能证明氯水具有漂白性的现象是____________________________。
(3)久置的氯水变为________,用化学反应方程式表示为__________。
(4)实验室保存饱和氯水的方法是_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com