
【题目】ⅰ.有下列物质:①铜;②硫酸钡固体;③氨水;④氢氧化钠固体;⑤熔融硝酸钾;⑥乙醇;⑦盐酸;⑧金刚石;⑨二氧化硫;⑩冰醋酸。
其中能导电的有_______;(填序号,下同)属于非电解质的有_____;属于强电解质的有_____;
ⅱ.写出①H2SO3 ②CH3COONH4在水中的电离方程式:
___________________________________________________________;
___________________________________________________________。
【答案】①③⑤⑦ ⑥⑨ ②④⑤ H2SO3![]() H++HSO3- CH3COONH4=NH4++CH3COO-
H++HSO3- CH3COONH4=NH4++CH3COO-
【解析】
ⅰ.①铜是金属单质,能导电,不是电解质也不是非电解质;②硫酸钡固体是盐,属于电解质。熔融状态下能完全电离,是强电解质;③氨水是混合物,能导电,不是电解质也不是非电解质;④氢氧化钠固体是电解质,由于是固体,所以不能导电;在水中或熔融状态下能完全电离,是强电解质;⑤熔融硝酸钾是电解质,因为在熔融态,因此可以导电;在水中或熔融状态下能完全电离,是强电解质;⑥乙醇是非电解质,不能导电;⑦盐酸是混合物,能导电,不是电解质也不是非电解质;⑧金刚石是非金属单质,不能导电,不是电解质也不是非电解质;⑨二氧化碳是非电解质,不能导电;⑩冰醋酸是电解质,由于都是以电解质分子的形式存在,所以不能导电。在水溶液中存在电离平衡,因此是弱电解质。因此其中能导电的有①③⑤⑦;属于非电解质的有⑥⑨;属于强电解质的有②④⑤ ;
ⅱ.H2SO3是二元弱酸,在水中电离出H+和HSO3-,电离方程式为:H2SO3![]() H++HSO3-;CH3COONH4水中完全电离出NH4+和CH3COO-,电离方程式为:CH3COONH4=NH4++CH3COO-。
H++HSO3-;CH3COONH4水中完全电离出NH4+和CH3COO-,电离方程式为:CH3COONH4=NH4++CH3COO-。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】将1molCO和1molNO2充入密闭容器中,在催化剂存在下发生反应NO2(g)+CO(g)![]() CO2(g)+NO(g)并达到化学平衡,发现有50%的CO转化为CO2。在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中CO2的体积分数是( )
CO2(g)+NO(g)并达到化学平衡,发现有50%的CO转化为CO2。在其它条件不变的情况下,若将1molCO和2molNO2充入上述反应器中,则反应达到化学平衡时,混合气体中CO2的体积分数是( )
A.1/9B.1/6C.2/9D.1/3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】福酚美克是一种影响机体免疫功能的药物,可通过以下方法合成:
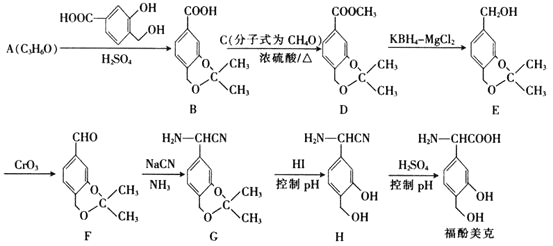
已知:
①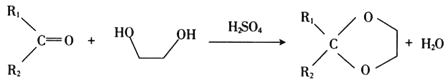 ;
;
②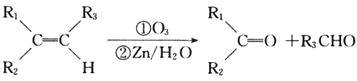 。
。
(1)C的名称为________,A的结构简式为________________。
(2)福酚美克中所含官能团有________________![]() 填名称
填名称![]() 。
。![]() 的反应类型为________。
的反应类型为________。
(3)已知![]() 的转化属于取代反应,则该反应的另一产物的结构简式为________。
的转化属于取代反应,则该反应的另一产物的结构简式为________。
(4)写出F发生银镜反应的化学方程式:________________________________。
(5)E的一种同分异构体Q满足下列条件,则Q的结构简式为________。
①Q的苯环上只有2个取代基,且Q的核磁共振氢谱图中有4组吸收峰
②Q能与![]() 溶液发生显色反应
溶液发生显色反应
③![]() 最多能与
最多能与![]() 发生反应
发生反应
(6)根据已有知识并结合题给信息,写出以![]() 为原料
为原料![]() 无机试剂任用
无机试剂任用![]() 制备
制备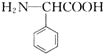 的合成路线流程图_________
的合成路线流程图_________![]() 无机试剂任选
无机试剂任选![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是石油化学工业的一种重要催化剂,其中Ag起催化作用,
是石油化学工业的一种重要催化剂,其中Ag起催化作用,![]() 是载体且不溶于硝酸,该催化剂的回收实验如图1所示.其中的转化反应为:
是载体且不溶于硝酸,该催化剂的回收实验如图1所示.其中的转化反应为:![]()
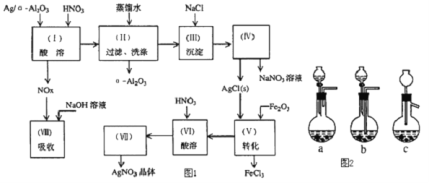
阅读上述实验流程,完成下列填空:
![]() 加酸溶解应该选用装置
加酸溶解应该选用装置![]() 图
图![]() ______
______ ![]() 选填a、b、
选填a、b、![]() .
.
![]() 在实验操作
在实验操作![]() Ⅱ
Ⅱ![]() ,如果用自来水代替蒸馏水进行洗涤,将会发生化学反应的离子方程式 ______ .
,如果用自来水代替蒸馏水进行洗涤,将会发生化学反应的离子方程式 ______ .
![]() 实验操作
实验操作![]() Ⅳ
Ⅳ![]() 所需玻璃仪器为 ______
所需玻璃仪器为 ______ ![]() 填写三种
填写三种![]() .
.
![]() 实验操作
实验操作![]() Ⅶ
Ⅶ![]() 从
从![]() 溶液获得
溶液获得![]() 晶体需要进行的实验操作依次为: ______
晶体需要进行的实验操作依次为: ______ ![]() 多选扣分
多选扣分![]() .
.
![]() 蒸馏
蒸馏![]() 蒸发
蒸发![]() 灼烧
灼烧![]() 冷却结晶
冷却结晶
![]() 已知:
已知:![]() ;
;
![]()
NO和![]() 的混合气体的组成可表示为
的混合气体的组成可表示为![]() 该混合气体通入NaOH溶液被完全吸收时,x的值为 ______
该混合气体通入NaOH溶液被完全吸收时,x的值为 ______
![]()
![]()
![]()
![]() 已知
已知![]() 中Ag的质量分数,若计算Ag的回收率,还必须知道的实验数据为 ______ 和 ______ .
中Ag的质量分数,若计算Ag的回收率,还必须知道的实验数据为 ______ 和 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某火电厂收捕到的粉煤灰的主要成分为SiO2、Al2O3、FeO、Fe2O3、MgO、TiO2等。研究小组对其进行综合处理的流程如下:
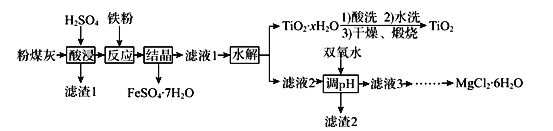
已知:①“酸浸”后钛主要以TiOSO4形式存在,强电解质TiOSO4在溶液中仅能电离SO42-和一种阳离子
②常温下,Ksp[Al(OH)3]=1.0×10-34,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mg(OH)2]= 5.61×10-12
③滤液1中仍有Fe2+剩余
请回答下列问题:
(1)为了提高粉煤灰浸出速率,在“酸浸”时可采取的措施有_______________________
(2)“水解”反应的离子方程式为______________________________________。怎样判断TiO2xH2O沉淀已经洗涤干净____________________________________________。
(3)加入双氧水调节溶液pH时离子方程式为_______________________________________。滤渣2成分为________________。为使滤渣2沉淀完全(溶液中离子浓度小于10-5mol/L)。需“调pH”为________。(保留两位有效数字)
(4)滤液3在蒸发结晶制备MgCl26H2O应注意_____________________________________。
(5)“结晶”需控制在70℃左右,温度过高的后果会导致的后果为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素单质及其化合物有广泛的用途,请根据周期表中短周期元素相关知识回答下列问题:
(1)空气中含量最高的元素与第三周期非金属性最强的元素形成的化合物的电子式: ___;
(2)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是____;
a.NH3 b.HI c.SO2 d.CO2
(3)第三周期金属性最强和非金属性最强元素形成的化合物的水溶液通电条件下发生的离子反应方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是( )
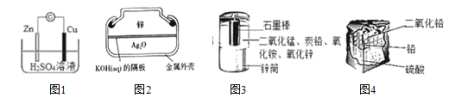
A.图 1 锌铜原电池中,Zn2+向 Cu 电极方向移动,Cu 电极附近溶液中 H+浓度增加
B.图 2 纽扣式银锌电池中,正极的电极反应式为 Ag2O+2e -+H2O = 2Ag+2OH-
C.图 3 锌锰干电池中,锌筒作负极,发生氧化反应,锌筒会变薄
D.图 4 铅蓄电池中,使用一段时间后,电解质溶液的酸性减弱,导电能力下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制得的氮化铝(AlN)产品中常含有少量Al4C3、Al2O3、C等杂质。某同学设计如下实验分别测定氮化铝(AlN)样品中AlN和Al4C3的质量分数(忽略NH3在强碱性溶液中的溶解)。
(1)实验原理:
①Al4C3与硫酸反应可生成CH4;
②AIN溶于强酸产生铵盐,溶于强碱生成氨气,请写出AlN与NaOH溶液反应的化学方程式:__________________________________________________________________
(2)实验装置(如图所示,量气管为碱式滴定管改装)
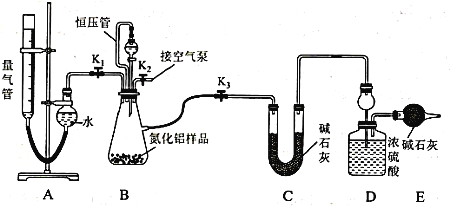
连好装置后,首先应进行的操作是_____________________________________ 。
(3)实验过程:称得装置D的初始质量为y g;称取x g AlN样品置于装置B锥形瓶中,各装置中加入相应药品,重新连好装置;读取量气管的初始读数为a mL(量气装置左右液面相平)。
①欲首先测量Al4C3质量分数的有关数据,对K1、K2、K3三个活塞的操作是关闭活塞_______,打开活塞______。
②若无恒压管,对所测气体体积的影响是_______(填“偏大”、“偏小”或“无影响”)。
③量气管中液面不再发生变化,说明反应已经结束。读取读数之前,应对量气管进行的操作为 ______________________________________ ;若量气管中的液面高于右侧球形容器中的液面,所测气体的体积_________(填“偏大”、“偏小”或“无影响”)。
④记录滴定管的读数为b mL(已知:该实验条件下的气体摩尔体积为Vm L· mol-1),则Al4C3的质量分数为___________(用可能含a、b、x、y、Vm的代数式表示)。
⑤测量AlN质量分数的数据:首先关闭活塞K1,打开活塞K3,通过分液漏斗加入过量NaOH溶液,与装置B瓶内物质充分反应;反应完成后,___________________________(填该步应进行的操作),最后称得装置D的质量为z g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com