
【题目】端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。2R—C≡C—H![]() R—C≡C—C≡C—R+H2该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:
R—C≡C—C≡C—R+H2该反应在研究新型发光材料、超分子化学等方面具有重要价值。下面是利用Glaser反应制备化合物E的一种合成路线:
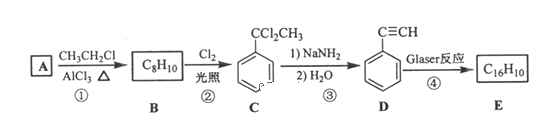
回答下列问题:
(1)B的结构简式为___,D的化学名称为___。
(2)①和③的反应类型分别为___、___。
(3)E的结构简式为___。用1molE合成1,4二苯基丁烷,理论上需要消耗氢气___mol。
(4)化合物(![]() )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为___。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为___。
(5)假设(4)生成1mol单一聚合度的G,若生成的G的总质量为1260g,则G的n值理论上应等于___。
(6)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中3种的结构简式___。
(7)写出用2苯基乙醇为原料(其他无机试剂任选)制备化合物D的合成路线___。
【答案】![]() 苯乙炔 取代反应 消去反应
苯乙炔 取代反应 消去反应 ![]() 4 n
4 n![]() +(n-1)H2O 10
+(n-1)H2O 10 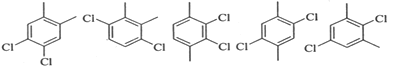 (任意三种)
(任意三种) 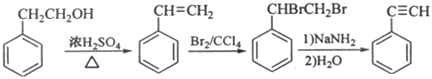
【解析】
B在光照下与Cl2发生取代反应生成C,可知B为乙苯,结构简式为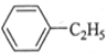 ,A与CH3CH2Cl得到B,可知A为苯。根据信息,2分子D发生Glaser反应,得到E,结构简式为
,A与CH3CH2Cl得到B,可知A为苯。根据信息,2分子D发生Glaser反应,得到E,结构简式为![]() 。
。
(1) B在光照下与Cl2发生取代反应生成C,由C的结构简式,可知B为乙苯,结构简式为 ;D的名称为苯乙炔;
;D的名称为苯乙炔;
(2)反应①为苯和CH3CH2Cl反应,苯环上的H原子被乙基取代,引入乙基,为取代反应;由C和D的结构可知,C中脱去2分子的HCl,得到D,则反应③为消去反应;
(3)根据信息,2分子D发生Glaser反应,得到E,结构简式为![]() ;1mol碳碳三键完全加成需要2mol氢气,现加成为1,4二苯基丁烷,则需要4mol氢气;
;1mol碳碳三键完全加成需要2mol氢气,现加成为1,4二苯基丁烷,则需要4mol氢气;
(4)根据信息,发生Claser反应时,C-H断裂,化合物发生缩聚反应时,将C-H断开,可以发生缩聚反应得到高分子化合物,化学方程式为n![]() +(n-1)H2;
+(n-1)H2;
(5)假设(4)生成1mol单一聚合度的G,若生成的G的总质量为1260g,链接的相对分子质量为124, 1mol单一聚合度的G,总质量为1260g,则有124×n+2=1260,则n=10;
(6)C的分子式为C8H8Cl2,F是C的同分异构体,其分子中只有与两种不同化学环境的氢,数目比为3:1,则可知道F中含有2个处于对称位置的甲基和2个处于对称位置的Cl原子,结构有 ;
;
(7)苯乙醇先发生消去反应,得到苯乙烯,在与溴发生加成反应,得到卤代烃,再模仿C到D,得到苯乙炔;答案为 。
。


科目:高中化学 来源: 题型:
【题目】某Na2CO3、NaAlO2的混合溶液中逐滴加入1molL1的盐酸,测得溶液中的CO32、HCO3、AlO2、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。则下列说法正确的是( )(已知:H2CO3的电离平衡常数K1 = 4.3×107,K2 = 5.6×1011;Al(OH)3的酸式电离平衡常数K=6.3×1013)

A. a曲线表示的离子方程式为:AlO2+4H+ = Al3+ + 2H2O
B. M点时生成的CO2为0.05 mol
C. 原混合溶液中的CO32与AlO2的物质的量之比为1:2
D. V1:V2=1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组拟探究CO2和锌粒反应是否生成CO,已知CO能与银氨溶液反应产生黑色固体。实验装置如图所示:

下列说法正确的是
A. 实验开始时,先点燃酒精灯,后打开活塞K
B. b、c、f中试剂依次为氢氧化钠溶液、浓硫酸、银氨溶液
C. 装置e的作用是收集一氧化碳气体
D. 用上述装置(另择试剂)可以制备氢气并探究其还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向 NaOH 和Na2CO3 混合溶液中滴加 0.1 mol·L1 稀盐酸,CO2 的生成量与加入盐酸的体积的关系如图。下列判断正确的是( )
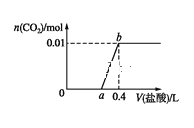
A.在 0~a 范围内,发生中和反应和 CO32-+H+=HCO3-
B.ab 段发生反应的离子方程式为: CO32-+2H+ CO2 +H2O
C.a=0.2
D.原混合溶液中NaOH 与 Na2CO3 的物质的量之比为 1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是两个氢原子相互接近时的能量变化图,则有关该图的说法正确的是( )
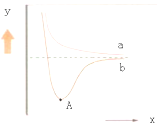
A.y代表两原子之间的核间距
B.x代表体系具有的能量
C.a代表核外电子自旋相反的两个氢原子能量变化
D.A点时表示两原子间形成了稳定的共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图装置(气密性已检查)制备Fe(OH)2白色沉淀。

请回答:
(1) 仪器1的名称________。装置5的作用________。
(2) 实验开始时,关闭K2,打开K1,反应一段时间后,再打开K2,关闭K1,发现3中溶液不能进入4中。请为装置作一处改进,使溶液能进入4中________。
(3) 装置改进后,将3中反应后溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白色沉淀的原因________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如下图所示。下列说法错误的是
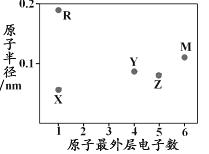
A. R的氧化物含有离子键 B. 最高价含氧酸的酸性:Z<Y
C. M的氢化物常温常压下为气体 D. Y形成的化合物种类最多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向200 mL FeBr2溶液中逐渐通入Cl2,其中n(Fe 3+)、n(Br2) 随通入n(Cl2)的变化如图所示,下列说法不正确的是( )
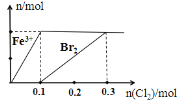
A.氧化性强弱:Br2 > Fe3+
B.由图可知,该FeBr2溶液的浓度为1 mol·L-l
C.n(Cl2) =0. 12 mol时,溶液中的离子浓度有:c (Fe 3+)∶c( Br-)=1∶8
D.n(FeBr2)∶n(Cl2) =1∶1时,反应的离子方程式为:2Fe2++2Br-+ 2Cl2=2Fe3++Br2 + 4Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第16届海南国际车展上:展出了中国研制的新型燃料电池汽车,该车装有“绿色心脏”---质子交换膜燃料电池。某种质子交换膜燃料电池如图所示。下列说法正确的是
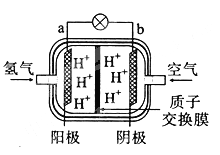
A.该电池的a极发生氧化反应B.正极反应为:O2+4e-+2H2O=4OH-
C.质子(H+)通过质子交换膜移动到a电极D.该燃料电池的能量转化率可达到100%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com