
【题目】某化学实验小组为探究SO2、Cl2的性质,并比较SO2和氯水的漂白性,设计了如下的实验。
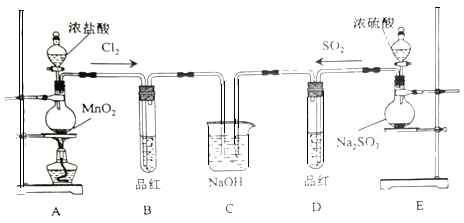
(1)图中盛放浓盐酸仪器的名称为___,装置A中发生反应的化学方程式___。
(2)反应一段时间后,B、D中品红褪色。反应结束后,分别加热B、D中的试管,可观察到的现象为:B___、D___。
(3)C装置的作用是吸收尾气,写出SO2与足量NaOH溶液反应的离子方程式:___。
(4)有同学将SO2和Cl2按1:1同时通入到品红溶液中,发现褪色效果并不明显。可能的原因是___(用化学方程式表示),设计实验证明上述原因___。
【答案】分液漏斗 MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑ 无明显现象 溶液由无色变为红色 Cl2+2OH﹣═Cl﹣+ClO﹣+H2O SO2+Cl2+2H2O=H2SO4+2HCl 取少量反应后的溶液少许加入试管中,加入氯化钡溶液生成白色沉淀证明生成了硫酸根离子,说明二氧化硫被氯气氧化
MnCl2+2H2O+Cl2↑ 无明显现象 溶液由无色变为红色 Cl2+2OH﹣═Cl﹣+ClO﹣+H2O SO2+Cl2+2H2O=H2SO4+2HCl 取少量反应后的溶液少许加入试管中,加入氯化钡溶液生成白色沉淀证明生成了硫酸根离子,说明二氧化硫被氯气氧化
【解析】
A用浓盐酸和 二氧化锰在加热条件下制备氯气,B用于检验气体的漂白性,C用于吸收尾气。E用于制备SO2,实验室用亚硫酸钠固体与硫酸反应制取![]() 气体,该反应为
气体,该反应为![]() ,D用于检验二氧化硫的生成,
,D用于检验二氧化硫的生成,
(1)图中盛放浓盐酸仪器为分液漏斗,![]() 和浓盐酸在加热的条件下制备氯气;
和浓盐酸在加热的条件下制备氯气;
(2)氯气和二氧化硫都能使品红溶液褪色,但是二氧化硫漂白后的物质具有不稳定性,加热时又能变为红色,而氯气的漂白具有不可逆性;
(3)氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水;
(4)![]() 和
和![]() 按1:1通入,
按1:1通入,![]() 和
和![]() 恰 好反应,二者反应生成
恰 好反应,二者反应生成![]() 和
和![]() ,生成 物都无漂白性,取少量反应后的溶液少许加入试管中,加入氯化钡溶液生成白色沉淀证明生成了硫酸根离子。
,生成 物都无漂白性,取少量反应后的溶液少许加入试管中,加入氯化钡溶液生成白色沉淀证明生成了硫酸根离子。
(1)图中盛放浓盐酸仪器为分液漏斗,MnO2和浓盐酸在加热的条件下制备氯气,反应的化学方程式:MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑,故答案为:分液漏斗;MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑,故答案为:分液漏斗;MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑;
MnCl2+2H2O+Cl2↑;
(2)氯气和二氧化硫都能使品红溶液褪色,但是二氧化硫漂白后的物质具有不稳定性,加热时又能变为红色,而氯气的漂白具有不可逆性,所以再给B、D两个试管分别加热,两个试管中的现象分别为B:无明显现象,D:溶液由无色变为红色,故答案为:无明显现象;溶液由无色变为红色;
(3)氯气与NaOH反应生成NaCl、NaClO和水,氯气、水在离子反应中保留化学式,该离子反应方程式:Cl2+2OH﹣═Cl﹣+ClO﹣+H2O,故答案为:Cl2+2OH﹣═Cl﹣+ClO﹣+H2O;
(4)SO2和Cl2按1:1通入,SO2和Cl2恰好反应,二者反应生成H2SO4和HCl,生成物都无漂白性,方程式为:SO2+Cl2+2H2O=H2SO4+2HCl,生成物都无漂白性,设计实验证明上述原因是:取少量反应后的溶液少许加入试管中,加入氯化钡溶液生成白色沉淀证明生成了硫酸根离子,说明二氧化硫被氯气氧化,故答案为:SO2+Cl2+2H2O=H2SO4+2HCl;取少量反应后的溶液少许加入试管中,加入氯化钡溶液生成白色沉淀证明生成了硫酸根离子,说明二氧化硫被氯气氧化。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】聚合硫酸铁铝、聚合氯化铝是高效水处理剂。以废铁屑、废铝质易拉罐及硫酸为原料,制备聚合硫酸铁铝的工艺流程如下:
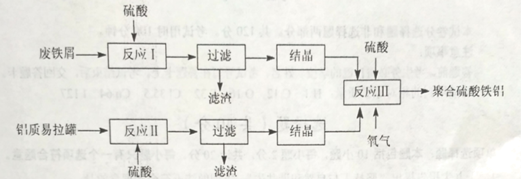
(1) 为提高反应I、II金属元素的浸出率,可以采取的措施有___。
(2) 反应III中FeSO4转化为Fe2(SO4)3的化学方程式为_____。
(3) 反应III的温度应控制在50℃~70℃为宜,原因是_____。反应II过程中往往加入少量硝酸铝,其作用如图16-1所示,转化①的离子方程式为___。
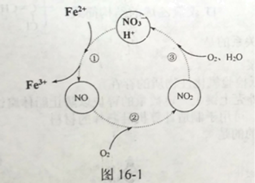
(4) 写出Fe2(SO4)3 水解生成Fe2(OH)n(SO4)3-n/2 的离子方程式:_____。
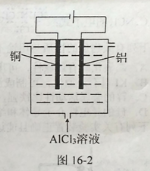
(5) 利用图16-2所示电解装置可制备净水剂聚合氯化铝。实际生产中,阳极附近因为副反应可能产生的气体有____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语表示正确的是( )
A.硅的原子结构示意图:
B.中子数为10的氧原子:![]() O
O
C.漂白粉有效成分的化学式;CaClO
D.NaHCO3在水溶液中的电离方程式:NaHCO3=Na++H++CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2(g)![]() 2NO(g)+ O2(g) 在体积不变的密闭容器中进行,达到平衡状态的标志是( )
2NO(g)+ O2(g) 在体积不变的密闭容器中进行,达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
A. ①④ B. ②③⑤ C. ①③④ D. ①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景,可以用多种方法合成。
Ⅰ.用CO2生产甲醇
(1)已知:H2的燃烧热为-285.8kJ/mol,CH3OH(l)的燃烧热为-725.8kJ/mol,
CH3OH(g)=CH3OH(l) ΔH=-37.3kJ/mol
则CO2(g)+3H2(g)![]() CH3OH(g)+H2O(l)ΔH=__kJ/mol。
CH3OH(g)+H2O(l)ΔH=__kJ/mol。
(2)将CO2和H2按物质的量之比1:3充入体积为2.0L的恒容密闭容器中反应,如图1两条曲线分别表示压强为0.1MPa和5.0MPa下CO2转化率随温度的变化关系。
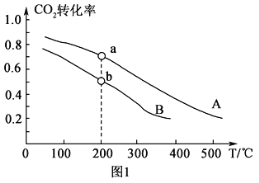
其中a点的平衡常数表达式为:__。
②a,b两点化学反应速率分别用Va、Vb表示,则Va__Vb(填“大于”、“小于”或“等于”)。
(3)在1.0L恒容密闭容器中投入1molCO2和2.75molH2发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图2所示,下列说法正确的是__。
CH3OH(g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图2所示,下列说法正确的是__。

A.该反应的正反应为放热反应
B.压强大小关系为p1<p2<p3
C.M点对应的平衡常数K的值约为1.04×10-2
D.在p2及512K时,图中N点v(正)<v(逆)
Ⅱ.用CO生产甲醇
(4)已知:CO(g)+2H2(g)![]() CH3OH(g),如图3是该反应在不同温度下CO的转化率随时间变化的曲线。
CH3OH(g),如图3是该反应在不同温度下CO的转化率随时间变化的曲线。
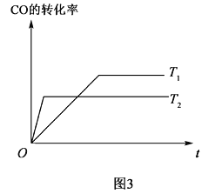
①该反应的焓变ΔH__0(填“ ”、“ ”或“ ”)。
②T1和T2温度下的平衡常数大小关系是K1___K2(填“>”、“<”或“=”)。
Ⅲ.甲醇的应用
(5)甲醇制氢气。甲醇水蒸气重整制氢反应:CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49kJ/mol。某温度下,将[n(H2O):n(CH3OH)]=1:1的原料气充入恒容密闭容器中,初始压强为p1,反应达到平衡时总压强为p2,则平衡时甲醇的转化率为___。
(6)以甲醇为主要原料,电化学合成碳酸二甲酯的工作原理如图4所示。阳极的电极反应式为__。
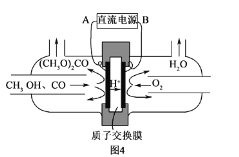
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:回答下列问题:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:回答下列问题:
T/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=___。
(2)该反应为___反应(选填吸热、放热)。
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为___℃。此温度下加入2molCO2(g)和2molH2(g),充分反应,达到平衡时,H2的转化率为___。
(4)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为:CO2(g)为2 mol/L,H2(g)为2mol/L,CO(g)为1mol/L,H2O(g)为3mol/L,则正、逆反应速率的关系为v(正)___v(逆)(填<、>、或=)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1200 ℃时,天然气脱硫工艺中会发生下列反应:H2S(g)+![]() O2(g)===SO2(g)+H2O(g) ΔH1,2H2S(g)+SO2(g)===
O2(g)===SO2(g)+H2O(g) ΔH1,2H2S(g)+SO2(g)===![]() S2(g)+2H2O(g) ΔH2,H2S(g)+1/2O2(g)===S(g)+H2O(g) ΔH3,2S(g)===S2(g) ΔH4 则ΔH4的正确表达式为( )
S2(g)+2H2O(g) ΔH2,H2S(g)+1/2O2(g)===S(g)+H2O(g) ΔH3,2S(g)===S2(g) ΔH4 则ΔH4的正确表达式为( )
A. ΔH4=![]() (ΔH1+ΔH2-3ΔH3)B. ΔH4=
(ΔH1+ΔH2-3ΔH3)B. ΔH4=![]() (3ΔH3-ΔH1-ΔH2)
(3ΔH3-ΔH1-ΔH2)
C. ΔH4=![]() (ΔH1+ΔH2-3ΔH3)D. ΔH4=
(ΔH1+ΔH2-3ΔH3)D. ΔH4=![]() (ΔH1-ΔH2-3ΔH3)
(ΔH1-ΔH2-3ΔH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质中,均含有相同的某种元素,在一定条件下,它们之间具有如下转化关系:甲![]() 乙
乙![]() 丙
丙![]() 丁。下列有关物质的推断不正确的是( )
丁。下列有关物质的推断不正确的是( )
A.若甲为C,则乙可能是CO
B.若甲为S,则丁可能是H2SO4
C.若甲为Na,则丙可能是Na2O2
D.若甲为Fe,则丁可能是Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:①CH3OH(g)+H2O(g)===CO2(g)+3H2(g) ΔH=+49.0 kJ/mol
②CH3OH(g)+![]() O2(g)===CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol
O2(g)===CO2(g)+2H2O(g) ΔH=-192.9 kJ/mol
由上述方程式可知:CH3OH的燃烧热________(填“大于”“等于”或“小于”)192.9 kJ/mol。
已知水的气化热为44 kJ/mol。则表示氢气燃烧热的热化学方程式为__________。
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。
已知:①2NH3(g)+CO2(g)===NH2CO2NH4(s) ΔH=-159.5 kJ/mol
②NH2CO2NH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+116.5 kJ/mol
③H2O(l)===H2O(g) ΔH=+44.0 kJ/mol
写出CO2与NH3合成尿素和液态水的热化学方程式是_____________________________。
(3)已知:①Fe(s)+![]() O2(g)===FeO(s) ΔH1=-272.0 kJ/mol
O2(g)===FeO(s) ΔH1=-272.0 kJ/mol
②2Al(s)+![]() O2(g)===Al2O3(s) ΔH2=-1675.7 kJ/mol
O2(g)===Al2O3(s) ΔH2=-1675.7 kJ/mol
Al和FeO发生铝热反应的热化学方程式是_____________________________________。该反应的自发性趋势很大,原因是________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com