
【题目】甲、乙、丙、丁四种物质中,均含有相同的某种元素,在一定条件下,它们之间具有如下转化关系:甲![]() 乙
乙![]() 丙
丙![]() 丁。下列有关物质的推断不正确的是( )
丁。下列有关物质的推断不正确的是( )
A.若甲为C,则乙可能是CO
B.若甲为S,则丁可能是H2SO4
C.若甲为Na,则丙可能是Na2O2
D.若甲为Fe,则丁可能是Fe(OH)3
 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
【题目】利用硫酸渣(主要成分为Fe2O3和少量的SiO2、FeO)可以制备高纯度的氧化铁,制备流程如图:
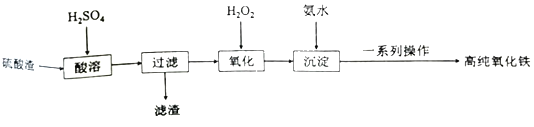
(1)滤渣的主要成分是___。
(2)“氧化”时发生反应的离子方程式为___。
(3)检验沉淀是否完全的方法为___。
(4)一系列操作包括:过滤、沉涤、干燥、___。
(5)用高温分解FeSO4也可以制备较纯的Fe2O3,写出反应的化学方程式___。
(6)上述硫酸渣含铁28%,现需高纯氧化铁64吨,理论上需用硫酸渣多少吨?___(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组为探究SO2、Cl2的性质,并比较SO2和氯水的漂白性,设计了如下的实验。
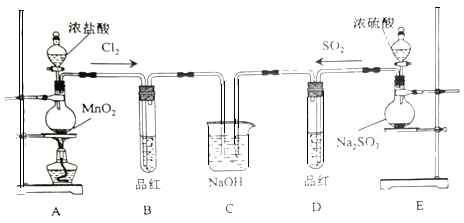
(1)图中盛放浓盐酸仪器的名称为___,装置A中发生反应的化学方程式___。
(2)反应一段时间后,B、D中品红褪色。反应结束后,分别加热B、D中的试管,可观察到的现象为:B___、D___。
(3)C装置的作用是吸收尾气,写出SO2与足量NaOH溶液反应的离子方程式:___。
(4)有同学将SO2和Cl2按1:1同时通入到品红溶液中,发现褪色效果并不明显。可能的原因是___(用化学方程式表示),设计实验证明上述原因___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物 H(结构简式为 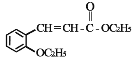 )是合成高分子化合物 M 的单体,H可以通过有机物A(分子式为 C7H8O)和丙酮为原料来进行合成,其合成路线如下:
)是合成高分子化合物 M 的单体,H可以通过有机物A(分子式为 C7H8O)和丙酮为原料来进行合成,其合成路线如下:
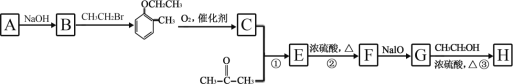
已知:① ![]()
②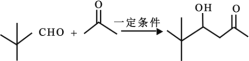
请回答下列问题:
(1)A结构简式为_____,C 中所含官能团的名称是_____;①和③的反应类型分别是_____。
(2)简述溴乙烷中溴原子检验方法_____。
(3)高分子化合物M 的结构简式为_____。
(4)反应③的化学反应方程式为_____。
(5)有机物 C 有多种同分异构体,其中苯环上只有两个侧链的芳香酯的同分异构体有_____种。
(6)设计由苯甲醛和 2-丙醇制备![]() 的合成路线_____(无机试剂任选)。
的合成路线_____(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草图经》有“白矾多人药用”。白矾[KAl(SO4)2·12H2O]又称明矾.钾铝矾、钾明矾等,是一种重要的化学试剂。下列说法正确的是( )
A.含白矾的药物不宜与胃药奧美拉唑碳酸氢钠胶囊同时服用
B.0.1molL-1白矾溶液完全水解生成Al(OH)3胶粒数小于6.02×1022
C.向含0.1mol白矾的溶液中滴入Ba(OH)2溶液,若SO42-和Al3+全部转化为BaSO4和Al(OH)3沉淀,则此时生成沉淀的质量最大
D.室温下,0.1molL-1白矾溶液中水电离出c(H+)小于10-7mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列判断正确的是( )
A.1mol N2含有的原子数目为NA
B.24gMg变为Mg2+时失去的电子数目为2NA
C.1 molL﹣1CaCl2溶液中含有的Cl﹣数目为2NA
D.常温常压下,11.2LCO2中含有的原子数目为1.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用蒸馏水稀释0. 1mol/L的CH3COOH溶液时,始终保持增大趋势的是
A. c(CH3COOH)B. c(H+)C. c(CH3COO-)D. c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式书写正确的是
A.溴乙烷发生消去反应:![]()
B.向![]() 溶液中加入过量氨水:
溶液中加入过量氨水:![]()
C.向![]() 溶液中加入过量
溶液中加入过量![]() 溶液:
溶液:![]()
D.向含![]() 和KOH均为0.1 mol的混合溶液中通人标准状况下4.48 L
和KOH均为0.1 mol的混合溶液中通人标准状况下4.48 L![]() 气体:
气体:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末,微溶于水、不溶于乙醇和稀硫酸。工业上用制作印刷电路的废液(含![]() 、
、![]() 、
、![]() 、
、![]() )生产CuCl的流程如图所示:
)生产CuCl的流程如图所示:

根据以上信息回答下列问题:
(1)生产过程中:X是______。(填化学式)
(2)写出生成CuCl的离子方程式______。
(3)析出的CuCl晶体不用水而用无水乙醇洗涤的原因是____。
(4)在CuCl的生成过程中理论上不需要补充SO2气体,其理由是___________。
(5)CuCl的另一种制备原理是Cu2++Cu+2Cl-=2CuCl K=5.85×106,向0.01 molL-1的CuCl2溶液中加入足量的铜,能否生成CuCl?(通过计算说明)_________。
(6)使用CuCl捕捉CO气体的反应为CuCl(s)+xCO(g) ![]() CuClxCO(s) △H < 0,为提高CO的平衡转化率,可采取的措施有____(填标号)。
CuClxCO(s) △H < 0,为提高CO的平衡转化率,可采取的措施有____(填标号)。
A 降低温度 B 增大压强 C 延长反应时间 D 把CuCl分散到疏松多孔的分子筛中
(7)已知:CuCl![]() Cu++Cl- K1; CuCl+Cl-
Cu++Cl- K1; CuCl+Cl-![]() CuCl2- K2;则反应Cu++2Cl-
CuCl2- K2;则反应Cu++2Cl-![]() CuCl2-的平衡常数K=_______(用K1、K2表示)。
CuCl2-的平衡常数K=_______(用K1、K2表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com