
����Ŀ����������������Ҫ�ɷ�ΪFe2O3��������SiO2��FeO�������Ʊ��ߴ��ȵ����������Ʊ�������ͼ��
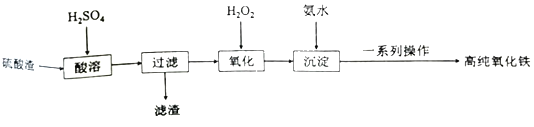
��1����������Ҫ�ɷ���___��
��2����������ʱ������Ӧ�����ӷ���ʽΪ___��
��3����������Ƿ���ȫ�ķ���Ϊ___��
��4��һϵ�в������������ˡ����ӡ����___��
��5���ø��·ֽ�FeSO4Ҳ�����Ʊ��ϴ���Fe2O3��д����Ӧ�Ļ�ѧ����ʽ___��
��6����������������28%������ߴ�������64�֣��������������������ٶ֣�___��д��������̣�
���𰸡�SiO2 2Fe2++H2O2+2H+��2Fe3++2H2O ���ã�ȡ���ɳ�������ϲ���Һ���������軯����Һ������Ѫ��ɫ�������������ȫ ���������� FeSO4![]() Fe2O3+SO2��+SO3�� 160t
Fe2O3+SO2��+SO3�� 160t
��������
������(��Ҫ��![]() ������Ϊ
������Ϊ![]() ��
��![]() ��)�������ܽ⣬����������ת��Ϊ���������ӣ��������費�ܣ����ˣ��õ����ж�����������������Һ�Ͷ��������������ټ�˫��ˮ��������������Ϊ
��)�������ܽ⣬����������ת��Ϊ���������ӣ��������費�ܣ����ˣ��õ����ж�����������������Һ�Ͷ��������������ټ�˫��ˮ��������������Ϊ![]() �����백ˮ���õ����������ij������ٹ��ˡ�ϴ�ӡ�������յõ���������������
�����백ˮ���õ����������ij������ٹ��ˡ�ϴ�ӡ�������յõ���������������
��1�����ݷ������
��2��˫��ˮ��������������Ϊ![]() ��
��
��3������Ϊ������������û�г�����ȫ���������������Լ�������Ƿ���ȫ�ķ����ǣ����ã�ȡ���ɳ�������ϲ���Һ���������軯����Һ������Ѫ��ɫ�������������ȫ��
��5�����������ڸ��������£�������ԭ��Ӧ�õ��������������������������
��6��������Ԫ���غ������
��1�����ݷ�����������ҪΪSiO2���ʴ�Ϊ��SiO2��
��2��˫��ˮ��������������ΪFe3+�����ӷ���ʽΪ2Fe2++H2O2+2H+��2Fe3++2H2O���ʴ�Ϊ��2Fe2++H2O2+2H+��2Fe3++2H2O��
��3������Ϊ������������û�г�����ȫ�����������������Լ�������Ƿ���ȫ�ķ����ǣ����ã�ȡ���ɳ�������ϲ���Һ���������軯����Һ������Ѫ��ɫ�������������ȫ���ʴ�Ϊ�����ã�ȡ���ɳ�������ϲ���Һ���������軯����Һ������Ѫ��ɫ�������������ȫ��
��4��Ҫ����������ת��������������Ҫ���������أ��ʴ�Ϊ�����������أ�
��5�����������ڸ��������£�������ԭ��Ӧ�õ����������������������������ʽΪ��FeSO4![]() Fe2O3+SO2��+SO3�����ʴ�Ϊ��FeSO4
Fe2O3+SO2��+SO3�����ʴ�Ϊ��FeSO4![]() Fe2O3+SO2��+SO3����
Fe2O3+SO2��+SO3����
��6��������Ԫ���غ㣬����Ҫ��������Ϊx�֣�����������Ϊ28%x�֣�����������ȫ����Դ�ڴˣ�64������������������Ϊ![]() ��64t��44.8t��������ʽ��28%x��44.8t�����x��160t��
��64t��44.8t��������ʽ��28%x��44.8t�����x��160t��
������Ҫ��������Ϊx�֣�����������Ϊ28%x�֣�64������������������Ϊ![]() ��64t��44.8t��������ʽ��28%x��44.8t�����x��160t��
��64t��44.8t��������ʽ��28%x��44.8t�����x��160t��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Z�Ǻϳ�ijҩ����м��壬��ϳ�ԭ������:
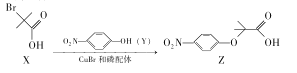
����˵����ȷ����.
A.��NaHCO3��Һ���Լ���X��ZB.X��Y��Z���ܷ���ȡ����Ӧ
C.X��������̼ԭ�ӿ��ܹ�ƽ��D.��X������ͬ�����ŵ�ͬ���칹�廹��5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ۺ������������ۺ��Ȼ����Ǹ�Чˮ���������Է���м������������������Ϊԭ�ϣ��Ʊ��ۺ����������Ĺ�������������
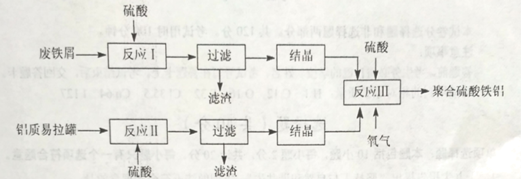
(1) Ϊ��߷�ӦI��II����Ԫ�صĽ����ʣ����Բ�ȡ�Ĵ�ʩ��___��
(2) ��ӦIII��FeSO4ת��ΪFe2(SO4)3�Ļ�ѧ����ʽΪ_____��
(3) ��ӦIII���¶�Ӧ������50��~70��Ϊ�ˣ�ԭ����_____����ӦII����������������������������������ͼ16-1��ʾ��ת���������ӷ���ʽΪ___��
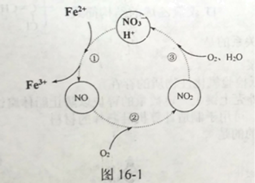
(4) д��Fe2(SO4)3 ˮ������Fe2(OH)n(SO4)3-n/2 �����ӷ���ʽ��_____��
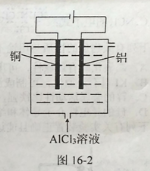
(5) ����ͼ16-2��ʾ���װ�ÿ��Ʊ���ˮ���ۺ��Ȼ�����ʵ�������У�����������Ϊ����Ӧ���ܲ�����������____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������̼����ȼ�ϵ��ԭ��ʾ����ͼ�������йظõ�ص�˵����ȷ���ǣ� ��

A. ��ӦCH4��H2O![]() 3H2��CO,ÿ����1molCH4ת��12mol ����
3H2��CO,ÿ����1molCH4ת��12mol ����
B. �缫A��H2����ĵ缫��ӦΪ��H2��2OH����2e��=2H2O
C. ��ع���ʱ��CO32����缫B�ƶ�
D. �缫B�Ϸ����ĵ缫��ӦΪ��O2��2CO2��4e��=2CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��ͬ��ѧԪ������ɵĻ��������˵������ȷ����

A. ��ͼ�Т�Ϊij�ֶ����ĵ��壬���������ǰ�����
B. ���ڴ�����Ƥ�º�����������Χ�Ȳ�λ�������֬��
C. ��һ���Ǻ��������ɺ���ĵ��������
D. �����Dz��빹��ֲ��ϸ���ڵ�һ�ֶ��ǣ�������������ά��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У����ڷ�Ӧ��������Ũ�Ȳ���ı䷴Ӧ������ǣ� ��
A.Fe��Cl2��Ӧ
B.CO2ͨ��ʯ��ˮ
C.HNO3���Cu
D.AlCl3��Һ�е���NaOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йػ�ѧ�����ʾ��ȷ���ǣ� ��
A.���ԭ�ӽṹʾ��ͼ��
B.������Ϊ10����ԭ�ӣ�![]() O
O
C.Ư����Ч�ɷֵĻ�ѧʽ��CaClO
D.NaHCO3��ˮ��Һ�еĵ��뷽��ʽ��NaHCO3=Na++H++CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ��2NO2(g)![]() 2NO(g)+ O2(g) �����������ܱ������н��У��ﵽƽ��״̬�ı�־�ǣ� ��
2NO(g)+ O2(g) �����������ܱ������н��У��ﵽƽ��״̬�ı�־�ǣ� ��
����λʱ��������n mol O2��ͬʱ����2n mol NO2
����λʱ��������n mol O2��ͬʱ����2n mol NO
����NO2��NO��O2�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2:2:1��״̬
������������ɫ���ٸı��״̬
�����������ܶȲ��ٸı��״̬
A. �٢� B. �ڢۢ� C. �٢ۢ� D. �٢ڢۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ����������������У���������ͬ��ij��Ԫ�أ���һ�������£�����֮���������ת����ϵ����![]() ��
��![]() ��
��![]() ���������й����ʵ��ƶϲ���ȷ����(����)
���������й����ʵ��ƶϲ���ȷ����(����)
A.����ΪC�����ҿ�����CO
B.����ΪS��������H2SO4
C.����ΪNa�����������Na2O2
D.����ΪFe��������Fe(OH)3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com