
ΓΨΧβΡΩΓΩ¬»Μ·―«Ά≠Θ®CuClΘ©≥Θ”ΟΉς”–ΜζΚœ≥…ΙΛ“Β÷–ΒΡ¥ΏΜ·ΦΝΘ§ «“Μ÷÷ΑΉ…ΪΖέΡ©Θ§ΈΔ»ή”ΎΥ°ΓΔ≤Μ»ή”Ύ““¥ΦΚΆœΓΝρΥαΓΘΙΛ“Β…œ”Ο÷ΤΉς”ΓΥΔΒγ¬ΖΒΡΖœ“ΚΘ®Κ§![]() ΓΔ
ΓΔ![]() ΓΔ
ΓΔ![]() ΓΔ
ΓΔ![]() Θ©…ζ≤ζCuClΒΡΝς≥Χ»γΆΦΥυ ΨΘΚ
Θ©…ζ≤ζCuClΒΡΝς≥Χ»γΆΦΥυ ΨΘΚ

ΗυΨί“‘…œ–≈œΔΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©…ζ≤ζΙΐ≥Χ÷–ΘΚX «______ΓΘΘ®ΧνΜ·―ß ΫΘ©
Θ®2Θ©–¥≥ω…ζ≥…CuClΒΡάκΉ”ΖΫ≥Χ Ϋ______ΓΘ
Θ®3Θ©Έω≥ωΒΡCuClΨßΧε≤Μ”ΟΥ°Εχ”ΟΈόΥ°““¥Φœ¥Β”ΒΡ‘≠“ρ «____ΓΘ
Θ®4Θ©‘ΎCuClΒΡ…ζ≥…Ιΐ≥Χ÷–άμ¬έ…œ≤Μ–η“Σ≤Ι≥δSO2ΤχΧεΘ§Τδάμ”… «___________ΓΘ
Θ®5Θ©CuClΒΡΝμ“Μ÷÷÷Τ±Η‘≠άμ «Cu2++Cu+2ClΘ≠ΘΫ2CuCl KΘΫ5.85ΓΝ106Θ§œρ0.01 molLΘ≠1ΒΡCuCl2»ή“Κ÷–Φ”»κΉψΝΩΒΡΆ≠Θ§ΡήΖώ…ζ≥…CuClΘΩΘ®Ά®ΙΐΦΤΥψΥΒΟςΘ©_________ΓΘ
Θ®6Θ© Ι”ΟCuCl≤ΕΉΫCOΤχΧεΒΡΖ¥”ΠΈΣCuCl(s)+xCO(g) ![]() CuClxCO(s) ΓςH < 0Θ§ΈΣΧαΗΏCOΒΡΤΫΚβΉΣΜ·¬ Θ§Ω…≤…»ΓΒΡ¥κ ©”–____Θ®Χν±ξΚ≈Θ©ΓΘ
CuClxCO(s) ΓςH < 0Θ§ΈΣΧαΗΏCOΒΡΤΫΚβΉΣΜ·¬ Θ§Ω…≤…»ΓΒΡ¥κ ©”–____Θ®Χν±ξΚ≈Θ©ΓΘ
A ΫΒΒΆΈ¬Ε» B ‘ω¥σ―Ι«Ω C ―”≥ΛΖ¥”Π ±Φδ D Α―CuClΖ÷…ΔΒΫ ηΥ…ΕύΩΉΒΡΖ÷Ή”…Η÷–
Θ®7Θ©“―÷ΣΘΚCuCl![]() Cu++ClΘ≠ K1ΘΜ CuCl+Cl-
Cu++ClΘ≠ K1ΘΜ CuCl+Cl-![]() CuCl2Θ≠ K2ΘΜ‘ρΖ¥”ΠCu++2ClΘ≠
CuCl2Θ≠ K2ΘΜ‘ρΖ¥”ΠCu++2ClΘ≠![]() CuCl2Θ≠ΒΡΤΫΚβ≥Θ ΐKΘΫ_______Θ®”ΟK1ΓΔK2±μ ΨΘ©ΓΘ
CuCl2Θ≠ΒΡΤΫΚβ≥Θ ΐKΘΫ_______Θ®”ΟK1ΓΔK2±μ ΨΘ©ΓΘ
ΓΨ¥πΑΗΓΩFe 2Cu2ΘΪΘΪSO2ΘΪ2ClΘ≠ΘΪ2H2O=2CuClΓΐΘΪSO42Θ≠ΘΪ4HΘΪ Φθ…Ό≤ζΤΖCuClΒΡΥπ ßΘ§“Ή”ΎΗ…‘ο CuΘΪ2H2SO4(≈®ΝρΥα)![]() CuSO4ΘΪSO2ΓϋΘΪ2H2OΖ¥”Π÷–…ζ≥…ΒΡCuSO4ΚΆSO2ΈΣ1ΘΚ1Θ§CuCl2ΘΪCuSO4ΘΪSO2ΘΪ2H2O=2CuClΓΐΘΪ2H2SO4Ζ¥”Π÷–œϊΚΡCuSO4ΚΆSO2“≤ΈΣ1ΘΚ1Θ§Υυ“‘άμ¬έ…œ≤Μ–η“Σ≤Ι≥δSO2 ΡήΘ§
CuSO4ΘΪSO2ΓϋΘΪ2H2OΖ¥”Π÷–…ζ≥…ΒΡCuSO4ΚΆSO2ΈΣ1ΘΚ1Θ§CuCl2ΘΪCuSO4ΘΪSO2ΘΪ2H2O=2CuClΓΐΘΪ2H2SO4Ζ¥”Π÷–œϊΚΡCuSO4ΚΆSO2“≤ΈΣ1ΘΚ1Θ§Υυ“‘άμ¬έ…œ≤Μ–η“Σ≤Ι≥δSO2 ΡήΘ§![]() AB
AB ![]()
ΓΨΫβΈωΓΩ
¬Υ‘ϋΔΎΚΆ≈®ΝρΥαΖ¥”ΠΩ…“‘ΒΟΒΫCuSO4Θ§Ω…÷Σ¬Υ‘ϋΔΎΈΣCuΘ§Ω…÷Σ¬Υ‘ϋΔΌάοΒΡ≥…Ζ÷ΈΣCuΚΆΙΐΝΩΒΡXΓΘΖœ“Κ÷–÷ς“Σ «Fe2ΘΪΓΔFe3ΘΪΓΔCu2ΘΪΓΔClΘ≠Θ§≤Μ“ΐ»κ–¬ΒΡ‘”÷ Θ§ΙΐΝΩXΈΣFeΖέΘ§ΙΐΝΩΒΡFe÷ΟΜΜ≥ωCuΘ§¬Υ“ΚΔΌ÷ς“Σ «FeCl2Θ§Ά®»κΙΐΝΩΒΡCl2Θ§ΒΟΒΫFeCl3Θ§Ω…“‘ ¥ΩΧΒγ¬ΖΑεΓΘ¬Υ‘ϋΔΌΈΣCuΚΆFeΘ§Φ”»κΙΐΝΩΒΡHClΘ§FeΚΆHClΖ¥”Π…ζ≥…FeCl2Θ§¬Υ“ΚΔΎ÷ς“ΣΈΣFeCl2Θ§ΓΘCuCl2ΚΆSO2ΓΔCuSO4Ζ¥”ΠΒΟΒΫCuClΓΘ
(1)ΗυΨίΖ÷ΈωXΈΣFeΘΜ
(2)ΗυΨίΆΦ ΨCuSO4ΓΔSO2ΓΔCuCl2Ζ¥”ΠΒΟΒΫCuClΘ§SO2÷–SΒΡΜ·ΚœΦέ¥”ΘΪ4…ΐΗΏΒΫΘΪ6Θ§…ζ≥…H2SO4Θ§ΕχCuCl2ΚΆCuSO4÷–CuΒΡΜ·ΚœΦέ¥”ΘΪ2ΫΒΒΆΒΫΘΪ1Θ§ΒΟΒΫCuClΨßΧεΘ§άκΉ”ΖΫ≥Χ ΫΈΣ2Cu2ΘΪΘΪSO2ΘΪ2ClΘ≠ΘΪ2H2O=2CuClΓΐΘΪSO42Θ≠ΘΪ4HΘΪΘΜ
(3)CuClΈΔ»ή”ΎΥ°Θ§≤Μ»ή”Ύ““¥ΦΘ§”Ο““¥Φœ¥Β”Θ§Ω…“‘Φθ…Όœ¥Β”Ιΐ≥Χ÷–ΒΡ»ήΫβΥπ ßΘ§Εχ«“““¥Φ“ΉΜ”ΖΔΘ§œ¥Β”Κσ“ΉΗ…‘οΘΜ
(4)Ά≠ΚΆ≈®ΝρΥαΖ¥”Π…ζ≥…SO2ΚΆCuSO4Θ§ΕχSO2ΚΆCuSO4”κCuCl2Ζ¥”Π…ζ≥…CuClΘ§ΗυΨίΜ·―ßΖΫ≥Χ≈–ΕœΘ§άμ”… «CuΘΪ2H2SO4(≈®ΝρΥα)![]() CuSO4ΘΪSO2ΓϋΘΪ2H2OΖ¥”Π÷–…ζ≥…ΒΡCuSO4ΚΆSO2ΈΣ1ΘΚ1Θ§CuCl2ΘΪCuSO4ΘΪSO2ΘΪ2H2O=2CuClΓΐΘΪ2H2SO4Ζ¥”Π÷–œϊΚΡCuSO4ΚΆSO2“≤ΈΣ1ΘΚ1Θ§Υυ“‘άμ¬έ…œ≤Μ–η“Σ≤Ι≥δSO2ΘΜ
CuSO4ΘΪSO2ΓϋΘΪ2H2OΖ¥”Π÷–…ζ≥…ΒΡCuSO4ΚΆSO2ΈΣ1ΘΚ1Θ§CuCl2ΘΪCuSO4ΘΪSO2ΘΪ2H2O=2CuClΓΐΘΪ2H2SO4Ζ¥”Π÷–œϊΚΡCuSO4ΚΆSO2“≤ΈΣ1ΘΚ1Θ§Υυ“‘άμ¬έ…œ≤Μ–η“Σ≤Ι≥δSO2ΘΜ
(5)Ζ¥”Π Cu2++Cu+2ClΘ≠ΘΫ2CuClΒΡΤΫΚβ≥Θ ΐ±μ Ψ Ϋ![]() Θ§‘Ύ0.01 molLΘ≠1ΒΡCuCl2»ή“Κ÷–Φ”»κΉψΝΩΒΡΆ≠Θ§Ω…ΗυΨί≈®Ε»…ΧQc≈–ΕœΘ§
Θ§‘Ύ0.01 molLΘ≠1ΒΡCuCl2»ή“Κ÷–Φ”»κΉψΝΩΒΡΆ≠Θ§Ω…ΗυΨί≈®Ε»…ΧQc≈–ΕœΘ§![]() Θ§Qc<KΘ§ΤΫΚβ’ΐœρΫχ––ΘΜ“ρ¥ΥΖ¥”ΠΡήΙΜΖΔ…ζΘ§”…”Ύ
Θ§Qc<KΘ§ΤΫΚβ’ΐœρΫχ––ΘΜ“ρ¥ΥΖ¥”ΠΡήΙΜΖΔ…ζΘ§”…”Ύ![]() Θ§Qc<KΘ§ΤΫΚβ’ΐœρΫχ––ΘΜ
Θ§Qc<KΘ§ΤΫΚβ’ΐœρΫχ––ΘΜ
(6)AΘ°ΗΟΖ¥”Π «Ζ≈»»Ζ¥”ΠΘ§ΫΒΒΆΈ¬Ε»Θ§ΤΫΚβ’ΐœρ“ΤΕ·Θ§COΒΡΉΣΜ·¬ ‘ωΦ”Θ§AΖϊΚœΧβ“βΘΜ
BΘ°‘ω¥σ―Ι«ΩΘ§œρΤχΧεΧεΜΐΦθ–ΓΒΡΖΫœρ“ΤΕ·Θ§Φ¥’ΐœρ“ΤΕ·Θ§COΉΣΜ·¬ Μα‘ωΦ”Θ§BΖϊΚœΧβ“βΘΜ
CΘ°¥οΒΫΤΫΚβΚσΘ§―”≥ΛΖ¥”Π ±ΦδΘ§Μ·―ßΤΫΚβ≤ΜΜα“ΤΕ·Θ§C≤ΜΖϊΚœΧβ“βΘΜ
DΘ°CuCl «ΙΧΧεΘ§Ζ÷…ΔΒΫ ηΥ…ΕύΩΉΒΡΖ÷Ή”…Η÷–Θ§÷Μ «‘ωΦ”ΝΥΫ”¥ΞΟφΜΐΘ§Φ”ΩλΖ¥”ΠΥΌ¬ Θ§ΤΫΚβ≤Μ“ΤΕ·Θ§D≤ΜΖϊΚœΧβ“βΘΜ
¥πΑΗ―ΓABΘΜ
(7)ΡΩ±ξΖ¥”ΠΩ…”…Ζ¥”Π2Θ≠Ζ¥”Π1ΒΟΒΫΘ§Μ·―ßΖΫ≥Χ ΫœύΦθΘ§‘ρΤΫΚβ≥Θ ΐœύ≥ΐΘ§‘ρCu++ClΘ≠![]() CuCl2Θ≠ΒΡΤΫΚβ≥Θ ΐK=
CuCl2Θ≠ΒΡΤΫΚβ≥Θ ΐK=![]() ΓΘ
ΓΘ


 ΨΌ“ΜΖ¥»ΐΆ§≤Ϋ«…Ϋ≤ΨΪΝΖœΒΝ–¥πΑΗ
ΨΌ“ΜΖ¥»ΐΆ§≤Ϋ«…Ϋ≤ΨΪΝΖœΒΝ–¥πΑΗ ΩΎΥψ”κ”Π”ΟΧβΩ®œΒΝ–¥πΑΗ
ΩΎΥψ”κ”Π”ΟΧβΩ®œΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΦΉΓΔ““ΓΔ±ϊΓΔΕΓΥΡ÷÷Έο÷ ÷–Θ§ΨυΚ§”–œύΆ§ΒΡΡ≥÷÷‘ΣΥΊΘ§‘Ύ“ΜΕ®ΧθΦΰœ¬Θ§ΥϋΟ«÷°ΦδΨΏ”–»γœ¬ΉΣΜ·ΙΊœΒΘΚΦΉ![]() ““
““![]() ±ϊ
±ϊ![]() ΕΓΓΘœ¬Ν–”–ΙΊΈο÷ ΒΡΆΤΕœ≤Μ’ΐ»ΖΒΡ «(ΓΓΓΓ)
ΕΓΓΘœ¬Ν–”–ΙΊΈο÷ ΒΡΆΤΕœ≤Μ’ΐ»ΖΒΡ «(ΓΓΓΓ)
A.»τΦΉΈΣCΘ§‘ρ““Ω…Ρή «CO
B.»τΦΉΈΣSΘ§‘ρΕΓΩ…Ρή «H2SO4
C.»τΦΉΈΣNaΘ§‘ρ±ϊΩ…Ρή «Na2O2
D.»τΦΉΈΣFeΘ§‘ρΕΓΩ…Ρή «Fe(OH)3
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΘ®1Θ©“―÷ΣΘΚΔΌCH3OH(g)ΘΪH2O(g)===CO2(g)ΘΪ3H2(g)ΓΓΠΛHΘΫΘΪ49.0 kJ/mol
ΔΎCH3OH(g)ΘΪ![]() O2(g)===CO2(g)ΘΪ2H2O(g)ΓΓΠΛHΘΫΘ≠192.9 kJ/mol
O2(g)===CO2(g)ΘΪ2H2O(g)ΓΓΠΛHΘΫΘ≠192.9 kJ/mol
”……œ ωΖΫ≥Χ ΫΩ…÷ΣΘΚCH3OHΒΡ»Φ…’»»________(ΧνΓΑ¥σ”ΎΓ±ΓΑΒ»”ΎΓ±ΜρΓΑ–Γ”ΎΓ±)192.9 kJ/molΓΘ
“―÷ΣΥ°ΒΡΤχΜ·»»ΈΣ44 kJ/molΓΘ‘ρ±μ Ψ«βΤχ»Φ…’»»ΒΡ»»Μ·―ßΖΫ≥Χ ΫΈΣ__________ΓΘ
Θ®2Θ©“‘CO2”κNH3ΈΣ‘≠ΝœΩ…Κœ≥…Μ·Ζ ΡρΥΊ[Μ·―ß ΫΈΣCO(NH2)2]ΓΘ
“―÷ΣΘΚΔΌ2NH3(g)ΘΪCO2(g)===NH2CO2NH4(s)ΓΓΠΛHΘΫΘ≠159.5 kJ/mol
ΔΎNH2CO2NH4(s)===CO(NH2)2(s)ΘΪH2O(g)ΓΓΠΛHΘΫΘΪ116.5 kJ/mol
ΔέH2O(l)===H2O(g)ΓΓΠΛHΘΫΘΪ44.0 kJ/mol
–¥≥ωCO2”κNH3Κœ≥…ΡρΥΊΚΆ“ΚΧ§Υ°ΒΡ»»Μ·―ßΖΫ≥Χ Ϋ «_____________________________ΓΘ
Θ®3Θ©“―÷ΣΘΚΔΌFe(s)ΘΪ![]() O2(g)===FeO(s)ΓΓΠΛH1ΘΫΘ≠272.0 kJ/mol
O2(g)===FeO(s)ΓΓΠΛH1ΘΫΘ≠272.0 kJ/mol
ΔΎ2Al(s)ΘΪ![]() O2(g)===Al2O3(s)ΓΓΠΛH2ΘΫΘ≠1675.7 kJ/mol
O2(g)===Al2O3(s)ΓΓΠΛH2ΘΫΘ≠1675.7 kJ/mol
AlΚΆFeOΖΔ…ζ¬Ν»»Ζ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ Ϋ «_____________________________________ΓΘΗΟΖ¥”ΠΒΡΉ‘ΖΔ–‘«ς ΤΚή¥σΘ§‘≠“ρ «________________________________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Ζ¥”ΠΦ» «―θΜ·ΜΙ‘≠Ζ¥”ΠΘ§”÷ «Έϋ»»Ζ¥”ΠΒΡ «
A. ΉΤ»»ΒΡΧΩ”κCO2Ζ¥”Π B. ―θΜ·Χζ”κ¬ΝΖ¥”Π
C. ΡΤ”κ““¥ΦΖ¥”Π D. Ba(OH)2ΓΛ8H2O”κNH4C1Ζ¥”Π
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ”–ΜζΈοA «÷Ί“ΣΒΡΙΛ“Β‘≠ΝœΘ§‘Ύ“ΜΕ®ΧθΦΰœ¬Ω…Κœ≥…Εύ÷÷“©ΈοΜρ“Ϋ“©÷–ΦδΧεΓΘ
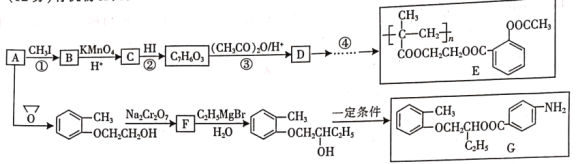
“―÷ΣΘΚ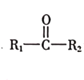
![]()
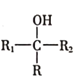
![]()
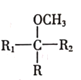 (R±μ ΨΧΰΜυΘ§
(R±μ ΨΧΰΜυΘ§![]() ΓΔ
ΓΔ![]() ±μ ΨΧΰΜυΜρ«β‘≠Ή”)ΓΘ«κΜΊ¥πΘΚ
±μ ΨΧΰΜυΜρ«β‘≠Ή”)ΓΘ«κΜΊ¥πΘΚ
(1)œ¬Ν–ΥΒΖ®÷–≤Μ’ΐ»ΖΒΡ «__________(ΧνΉ÷ΡΗ)ΓΘ
A.”–ΜζΈοGΒΡΖ÷Ή” Ϋ «![]()
B.”–ΜζΈοAΚΆFΨυΡή ΙδεΥ°Ά …Ϊ
C.Κœ≥…Ιΐ≥Χ÷–…ηΦΤΖ¥”ΠΔΌΓΔΔΎΒΡΡΩΒΡ «±ΘΜΛΖ”τ«Μυ≤Μ±Μ―θΜ·
D.1mol E”κΉψΝΩΒΡNaOH»ή“ΚΖ¥”ΠΘ§ΉνΕύΩ…“‘œϊΚΡ4mol NaOH
(2)”–ΜζΈοBΒΡΫαΙΙΦρ Ϋ «__________ΓΘ
(3)Ζ¥”ΠΔή÷–ΒΡΚœ≥…‘≠Νœ≥ΐDΆβΘ§ΜΙ–η“ΣΒΡ”–ΜζΈο «__________ΓΔ__________ΓΘ(–¥ΫαΙΙΦρ Ϋ)
(4)Ζ¥”ΠΔέΒΡΜ·―ßΖΫ≥Χ Ϋ «__________ΓΘ
(5)–¥≥ωΜ·ΚœΈοFΆ§ ±ΖϊΚœœ¬Ν–ΧθΦΰΒΡΥυ”–Ω…ΡήΒΡΆ§Ζ÷“λΙΙΧεΒΡΫαΙΙΦρ ΫΘΚ__________ΓΘ
ΔΌ±ΫΜΖ…œ÷Μ”–ΝΫ÷÷≤ΜΆ§Μ·―ßΜΖΨ≥ΒΡ«β‘≠Ή”ΘΜ
ΔΎΡήΖΔ…ζΥ°ΫβΖ¥”ΠΘ§1molΗΟΈο÷ ΡήœϊΚΡ2mol NaOH
(6)“άΨίΧα Ψ–≈œΔΘ§…ηΦΤ“‘AΈΣ‘≠Νœ÷Τ±Η ΒΡΚœ≥…¬ΖœΏ__________(ΧαΙ©
ΒΡΚœ≥…¬ΖœΏ__________(ΧαΙ©![]() ΦΑ–η“ΣΒΡΈόΜζ ‘ΦΝ)ΓΘΉΔΘΚΚœ≥…¬ΖœΏΒΡ ι–¥Ηώ Ϋ≤Έ’’»γœ¬ ΨάΐΝς≥ΧΆΦΘΚCH3CH2OH
ΦΑ–η“ΣΒΡΈόΜζ ‘ΦΝ)ΓΘΉΔΘΚΚœ≥…¬ΖœΏΒΡ ι–¥Ηώ Ϋ≤Έ’’»γœ¬ ΨάΐΝς≥ΧΆΦΘΚCH3CH2OH![]() H2C=CH2
H2C=CH2![]() BrH2C-CH2Br
BrH2C-CH2Br
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΑ¥“Σ«σΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©œ÷”–“‘œ¬Έο÷ ΘΚΔΌNaClΨßΧε ΔΎ“ΚΧ§HCl ΔέCaCO3ΙΧΧε Δή»έ»ΎKCl Δί’αΧ« ΔόΆ≠ ΔΏCO2 ΔύH2SO4 ΔαKOHΙΧΧε
a. “‘…œΈο÷ ÷–ΡήΒΦΒγΒΡ «________________________________ΓΘ
b. “‘…œΈο÷ ÷– τ”ΎΒγΫβ÷ ΒΡ «_______________________Θ§ τ”ΎΖ«ΒγΫβ÷ ΒΡ «_______________________ΓΘ
c. “‘…œΈο÷ ÷–Θ§»ή”ΎΥ°«“ΡήΒΦΒγΒΡΈο÷ «_______________________ΓΘ
Θ®2Θ©ΫΚΧεΚΆ»ή“ΚΒΡ±Ψ÷ «χ±π «________________Θ§Φχ±πΫΚΧεΚΆ»ή“ΚΥυ≤…”ΟΒΡΖΫΖ® «Ιέ≤λ «ΖώΡήΖΔ…ζ___________–ß”ΠΓΘ
Θ®3Θ©œ¬Ν–3ΗωΖ¥”ΠΘ§Α¥“Σ«σΧν–¥œύΙΊΝΩΓΘ
ΔΌ2Na2O2+2H2OΘΫ4NaOH+ O2ΓϋΖ¥”Π÷–Θ§ΟΩœϊΚΡ1 mol Na2O2…ζ≥…_____ g O2ΓΘ
ΔΎ‘ΎNaHCO3ΒΡ»»Ζ÷ΫβΖ¥”Π÷–Θ§ΟΩœϊΚΡ168 g NaHCO3Θ§±ξΉΦΉ¥Ωωœ¬…ζ≥…_____L CO2ΓΘ
ΔέCl2+H2OΘΫHCl+HClOΖ¥”Π÷–Θ§±ξΉΦΉ¥Ωωœ¬ΟΩœϊΚΡ22.4LCl2Θ§ΉΣ“Τ_____molΒγΉ”ΓΘ
Θ®4Θ©‘Ύ“ΜΗωΟή±’»ίΤς÷–Ζ≈»κ“‘œ¬ΥΡ÷÷Έο÷ Θ§‘Ύ“ΜΕ®ΧθΦΰœ¬ΖΔ…ζΜ·―ßΖ¥”ΠΘ§“ΜΕΈ ±ΦδΚσΘ§≤βΒΟ”–ΙΊ ΐΨί»γœ¬ΘΚ
Έο÷ | M | N | Q | P |
Ζ¥”Π«Α÷ ΝΩΘ®gΘ© | 50 | 1 | 3 | 12 |
Ζ¥”ΠΚσ÷ ΝΩΘ®gΘ© | x | 26 | 3 | 30 |
ΔΌΗΟ±δΜ·ΒΡΜυ±ΨΖ¥”Πάύ–Ά «_____Ζ¥”ΠΘΜ
ΔΎΈο÷ Q‘ΎΖ¥”Π÷–ΤπΒΡΉς”Ο «_____ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩXΓΔYΓΔZΓΔVΓΔWΈε÷÷ΕΧ÷ήΤΎ‘ΣΥΊΘ§‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§Τδ÷–ZΒΡ‘≠Ή”ΑκΨΕΉν¥σΘ§ZΒΡΒΞ÷ ‘ΎWΒΡΒΞ÷ ÷–»Φ…’≤ζ…ζΜΤ…ΪΜπ―φΘΜΈε÷÷‘ΣΥΊΩ…“‘Ήι≥…“Μ÷÷”–Μζ―ΈΘ®»γΆΦΥυ ΨΘ©ΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
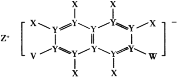
A.Y”κW–Έ≥…ΒΡΖ÷Ή”÷–Ης‘≠Ή”ΉνΆβ≤ψΨυ¬ζΉψ8ΒγΉ”Έ»Ε®ΫαΙΙ
B.‘≠Ή”ΑκΨΕΒΡ¥σ–ΓΙΊœΒΈΣΘΚV >Z > W
C.»»Έ»Ε®–‘ΘΚX”κVΉι≥…ΒΡΕΰ‘ΣΜ·ΚœΈο>X”κWΉι≥…ΒΡΕΰ‘ΣΜ·ΚœΈο
D.Y”κVΉι≥…ΒΡΕΰ‘ΣΜ·ΚœΈοΖ÷Ή”÷–Κ§”–ΝΫΗωYΘ≠VΦϋ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ(1)12.4 g Na2RΚ§NaΘΪ0.4 molΘ§‘ρNa2RΒΡΡΠΕϊ÷ ΝΩΈΣ________Θ§RΒΡœύΕ‘‘≠Ή”÷ ΝΩΈΣ________ΓΘΚ§RΒΡ÷ ΝΩΈΣ1.6 gΒΡNa2RΘ§ΤδΈο÷ ΒΡΝΩΈΣ________ΓΘ
(2)86.4gAΒΞ÷ ”κ4.80molCl2Άξ»ΪΖ¥”ΠΘ§…ζ≥…3.20molAClx,‘ρx=___________Θ§AΒΡΡΠΕϊ÷ ΝΩΈΣ__________________gΓΛmol-1
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ “Έ¬œ¬Θ§ΒΞ÷ AΓΔBΓΔCΖ÷±πΈΣΙΧΧεΓΔΜΤ¬Χ…ΪΤχΧεΓΔΈό…ΪΤχΧεΘ§‘ΎΚœ ΒΡΖ¥”ΠΧθΦΰœ¬Θ§ΥϋΟ«Ω…Α¥œ¬ΟφΩρΆΦΫχ––Ζ¥”ΠΓΘ”÷÷ΣD»ή“ΚΈΣΜΤ…ΪΘ§E»ή“ΚΈΣΈό…ΪΘ§«κΜΊ¥πΘΚ
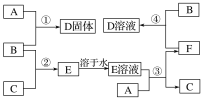
(1)A «__________Θ§B «__________Θ§C «_______________(Χν–¥Μ·―ß Ϋ)ΓΘ
(2)Ζ¥”ΠΔΌΒΡΜ·―ßΖΫ≥Χ ΫΈΣ_______________________________ΓΘ
(3)Ζ¥”ΠΔέΒΡΜ·―ßΖΫ≥Χ ΫΈΣ________________________________________ΓΘ
(4)Ζ¥”ΠΔήΒΡΜ·―ßΖΫ≥Χ ΫΈΣ____________________________________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com