
【题目】下列反应既是氧化还原反应,又是吸热反应的是
A. 灼热的炭与CO2反应 B. 氧化铁与铝反应
C. 钠与乙醇反应 D. Ba(OH)2·8H2O与NH4C1反应
【答案】A
【解析】A项,灼热的炭与CO2的反应为氧化还原反应,是吸热反应;B项,氧化铁与铝的反应是氧化还原反应,是放热反应;C项,Na与乙醇的反应为氧化还原反应,是放热反应;D项,Ba(OH)2·8H2O与NH4Cl的反应不是氧化还原反应,是吸热反应。
A项,灼热的炭与CO2反应的化学方程式为C+CO2![]() 2CO,反应前后元素的化合价有升降,该反应为氧化还原反应,是吸热反应;B项,氧化铁与铝反应的化学方程式为2Al+Fe2O3
2CO,反应前后元素的化合价有升降,该反应为氧化还原反应,是吸热反应;B项,氧化铁与铝反应的化学方程式为2Al+Fe2O3![]() 2Fe+Al2O3,反应前后元素的化合价有升降,该反应是氧化还原反应,铝热反应是放热反应;C项,Na与乙醇反应的化学方程式为2Na+2CH3CH2OH→2CH3CH2ONa+H2↑,反应前后元素的化合价有升降,该反应为氧化还原反应,是放热反应;D项,Ba(OH)2·8H2O与NH4Cl反应的化学方程式为Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O,反应前后元素的化合价没有改变,该反应不是氧化还原反应,是吸热反应;符合题意的是A项,答案选A。
2Fe+Al2O3,反应前后元素的化合价有升降,该反应是氧化还原反应,铝热反应是放热反应;C项,Na与乙醇反应的化学方程式为2Na+2CH3CH2OH→2CH3CH2ONa+H2↑,反应前后元素的化合价有升降,该反应为氧化还原反应,是放热反应;D项,Ba(OH)2·8H2O与NH4Cl反应的化学方程式为Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O,反应前后元素的化合价没有改变,该反应不是氧化还原反应,是吸热反应;符合题意的是A项,答案选A。


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示,其中A为地壳中含量最高的金属元素。
B | C | D | ||
A | E |
请用化学用语回答下列问题:
(1)A、D、E元素简单离子半径由大到小的顺序为 > > (填粒子符号)_____
(2)F与D同主族且相邻二者气态氢化物稳定性的大小关系为 > (填粒子符号)_________
(3)用高能射线照射含有10电子的D元素氢化物分子时,一个分子能释放出一个电子,同时产生一种
具有较强氧化性的阳离子,试写出该阳离子的电子式:______________。该阳离子中存在的化学键有_________。
(4)由C、E两种元素组成的化合物甲,常温下为易挥发的淡黄色液体,甲分子构型为三角锥形,且分子中C、E两种原子最外层均达到8个电子的稳定结构。甲遇水蒸气可形成一种常见的漂白性物质。写出甲遇水蒸气的化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸铵(NH4ClO4)为白色晶体,是强氧化剂,常用作火箭发射的推进剂。已知:①NH4ClO4在400℃时开始分解,产物为N2、Cl2、O2、H2O;②Mg3N2易水解。请用下图所示装置设计实验证明分解产物中含有Cl2、H2O以及装置A中生成了Mg3N2(装置不重复使用)。
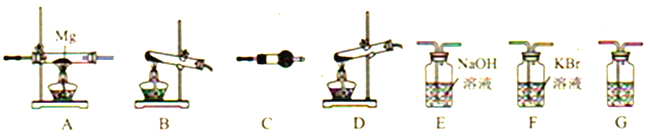
(1)写出高氯酸铵分解的化学方程式__________。
(2)高氯酸铵分解选择的装置是__________(填字母)。
(3)按气流从左到右,装置的连接顺序是:分解装置→_____→_____→_____→_____→_____。______________
(4)C中所放的试剂是__________,G的作用是__________ 。
(5)能证明有Cl2产生的现象是__________。
(6)要证明装置A中生成了Mg3N2需要进行的实验操作以及对应的实验现象是__________。
(7)某实验宣存放的高氯酸铵样品中含有少量杂质,已知可用蒸馏法测定NH4ClO4的含量,其测定流程如下(杂质不参加反应),则样品中NH4ClO4的含量(w)为__________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M 有抗菌作用,其合成路线如下图所示:
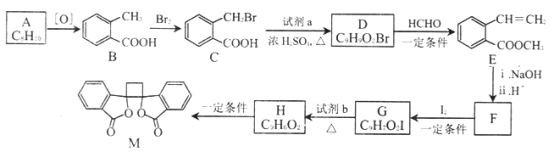
已知:
①RCH2Br R-HC=CH-R
R-HC=CH-R
②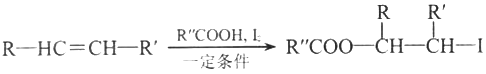
③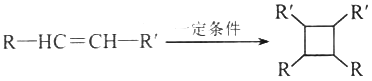
(以上R、R'、R”代表氢、烷基或芳基等)
(1)A的结构简式是___________。
(2)B 的名称是__________,M 中的官能团名称是__________ 。
(3)分别写出B-C、G-H 的反应类型__________ 、__________ 。
(4)写出C-D 的化学方程式__________________。
(5)E 的同分异构体中,符合下列条件的结构共有_______种。
①苯的二元取代物 ②与E 具有相同的官能团 ③能发生银镜反应和水解反应
(6)由F 与I在一定条件下反应生成G 的化学方程式是__________;此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在生物实验中,可以根据与某些化学试剂所产生的颜色反应,检测生物组织中的有关有机化合物的存在。在下列实验列表中,正确的是( )
选项 | 待检测的物质 | 使用试剂 | 呈现颜色 |
A | 苹果中的还原糖 | 斐林试剂 | 橘黄色 |
B | 马铃薯中的淀粉 | 双缩脲试剂 | 蓝色 |
C | 花生的脂肪 | 苏丹Ⅲ染液 | 橘黄色 |
D | 大豆中的蛋白质 | 斐林试剂 | 紫色 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钒和镍及其化合物是重要合金材料和催化剂,其储氢合金可作为一种新型锌离子电池的负极材料,该电池以Zn(CF3SO3)2为电解质,以有缺陷的阳离子型ZnMn2O4为电极,成功获得了稳定的大功率电流。
(1)基态钒原子的核外电子排布式为________,其排布时能量最高电子所占据能级的原子轨道有________个伸展方向。
(2)VO2+可与多种物质形成配合物,与氧同周期且第一电离能比氧大的主族元素有____(写元素符号)。
(3)镍形成的配离子[Ni(NH3)6]2+、[Ni(CN)4]2-中,NH3分子的空间构型为_______,与CN-互为等电子体的一种分子的化学式为__________。
(4)三氟甲磺酸(CF3SO3H)是一种有机强酸,结构式如图1所示,通常以CS2、IF3、H2O2等为主要原料来制取。
①H2O2分子中O原子的杂化方式为________。
②三氟甲磺酸能与碘苯反应生成三氟甲磺酸苯酯和碘化氢。1个三氟甲磺酸苯酯分子中含有σ键的数目为__________。

(5)硫化锌晶体的构型有多种,其中一种硫化锌的晶胞如图2所示,该晶胞中S2-的配位数为____。
(6)镧镍合金是重要储氢材料,其储氢后的晶胞如图3所示。
①储氢前该镧镍合金的化学式为___________。
②该镧镍合金储氢后氢气的密度为________(用NA表示阿伏加德罗常数的数值)g.cm-3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com