
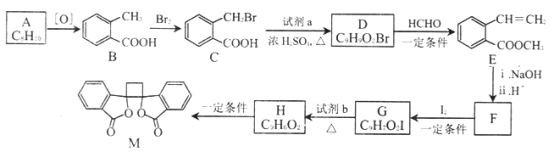
【题目】有机物M 有抗菌作用,其合成路线如下图所示:
已知:
①RCH2Br R-HC=CH-R
R-HC=CH-R
②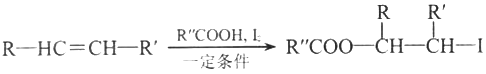
③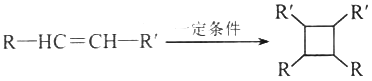
(以上R、R'、R”代表氢、烷基或芳基等)
(1)A的结构简式是___________。
(2)B 的名称是__________,M 中的官能团名称是__________ 。
(3)分别写出B-C、G-H 的反应类型__________ 、__________ 。
(4)写出C-D 的化学方程式__________________。
(5)E 的同分异构体中,符合下列条件的结构共有_______种。
①苯的二元取代物 ②与E 具有相同的官能团 ③能发生银镜反应和水解反应
(6)由F 与I在一定条件下反应生成G 的化学方程式是__________;此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是__________。
【答案】 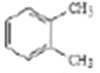 邻甲基苯甲酸 酯基 取代反应 消去反应
邻甲基苯甲酸 酯基 取代反应 消去反应 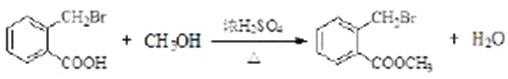 18
18 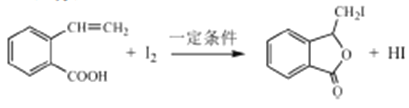
 或
或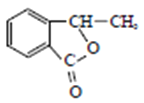
【解析】考查有机物的合成和推断,(1)根据B的结构简式,A的分子式,以及A生成B,发生的是氧化反应,因此A的结构简式为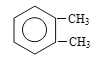 ;(2)根据有机物命名原则,B的名称为邻甲基苯甲酸;根据M的结构简式,M含有官能团是酯基;(3)根据B和C的结构简式,Br取代-CH3上的氢原子,发生的反应类型为取代反应,G和H的分子式对比,H比G少了1个H和1个I,即G→H发生的消去反应;(4)对比C和E的结构简式,以及根据信息①,C→D发生酯化反应,即试剂a为CH3OH,反应方程式为
;(2)根据有机物命名原则,B的名称为邻甲基苯甲酸;根据M的结构简式,M含有官能团是酯基;(3)根据B和C的结构简式,Br取代-CH3上的氢原子,发生的反应类型为取代反应,G和H的分子式对比,H比G少了1个H和1个I,即G→H发生的消去反应;(4)对比C和E的结构简式,以及根据信息①,C→D发生酯化反应,即试剂a为CH3OH,反应方程式为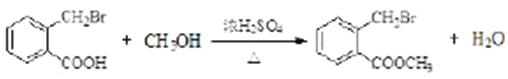 ;(5)与E具有相同的官能团,即含有碳碳双键和酯基,苯环上有连个取代基,取代基位置为邻间对,能发生银镜反应以及水解反应,应是甲酸某酯的形式,因此符合条件的结构简式分别是
;(5)与E具有相同的官能团,即含有碳碳双键和酯基,苯环上有连个取代基,取代基位置为邻间对,能发生银镜反应以及水解反应,应是甲酸某酯的形式,因此符合条件的结构简式分别是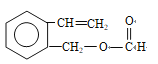 (邻间对三种)、
(邻间对三种)、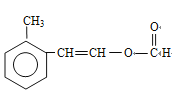 (邻间对三种)、
(邻间对三种)、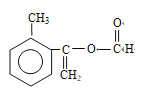 (邻间对三种)、
(邻间对三种)、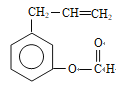 (邻间对三种)、
(邻间对三种)、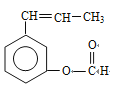 (邻间对三种)、
(邻间对三种)、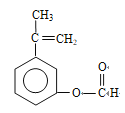 (邻间对三种),共有18种;(6)E生成F发生酯的水解,即F的结构简式为:
(邻间对三种),共有18种;(6)E生成F发生酯的水解,即F的结构简式为: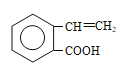 ,根据信息②,F→G的化学反应方程式为
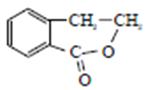
,根据信息②,F→G的化学反应方程式为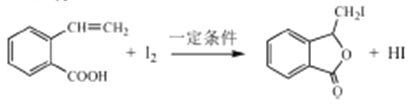 ,羧酸与酯互为同分异构,因此副产物是
,羧酸与酯互为同分异构,因此副产物是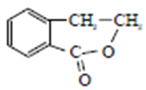 或
或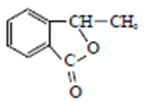 。
。


科目:高中化学 来源: 题型:
【题目】实验室从海带灰中提取碘的操作过程中仪器选用不正确的是
A. 称取3 g左右的干海带——托盘天平
B. 灼烧干海带至完全变成灰烬——蒸发皿或坩埚
C. 过滤煮沸后的海带灰和水的混合物——漏斗
D. 用四氯化碳从氧化后的海带灰浸取液中提取碘——蒸馏烧瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物仅由C,H,O三种元素组成,其相对分子量小于150,若其中氧的质量分数为百分之50,则分子中C原子个数最多为( )
A. 4 B. 5 C. 6 D. 7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应2SO2(g)+O2(g)2SO3(g)△H<0,某研究小组探究其他条件下不变时,改变某一条件对上述反应的影响,下列分析正确的是( ) 
A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响
B.图Ⅱ表示的是t1时刻加入催化剂后对反应速率的影响
C.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙的高
D.图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是吸热反应的是
A. 灼热的炭与CO2反应 B. 氧化铁与铝反应
C. 钠与乙醇反应 D. Ba(OH)2·8H2O与NH4C1反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下表部分短周期元素信息,判断以下叙述正确的是( )
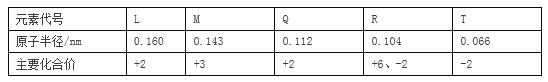
A. 氢化物的沸点为H2T<H2R B. 单质与稀盐酸反应的剧烈程度L<Q
C. M与T形成的化合物具有两性 D. L2+与R2﹣的核外电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化尿素是一种新型漂白剂、消毒剂、漂白、消毒的效果优于H2O2和过氧乙酸。某工业用过氧化尿素的部分参数见下表:
分子式 | 外观 | 热分解温度 | 熔点 | 水溶性(20℃) |
CO(NH2)2·H2O2 | 白色晶体 | 45℃ | 75~85℃ | 500g·L-1 |
合成过氧化尿素的步骤及反应器的示意图如下:在250mL三颈烧瓶中加入一定量的30%的H2O2溶液,再加入30g尿素,在不断搅拌下升温至300℃,使尿素完全溶解,保温30min,冷却至-5℃进行结晶。抽滤得白色粉末状结晶。在50℃下干燥2h,得过氧化尿素产品。回答下列问题:
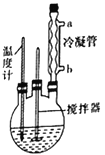
(1)控制反应温度的适宜方法是__________ (填序号)。
A.酒精灯加热 B.酒精喷灯加热 C.电炉加热 D.水浴加热
(2)反应器中发生反应的化学方程式为___________________________________。
(3)反应器中冷凝管中冷水从______(填“a”或“b”)流进;反应器加热温度不能太高的原因是___________。
(4)搅拌器不能选择铁质或铝质材料的原因是_______________________________________。
(5)为测定产品中活性氧的含量(活性氧16%,相当于含H2O234%),称取干燥样品12.000g,溶解,在250mL 容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1mL6mol·L-1的硫酸,然后用0.2000mol·L-1KMnO4标准溶液滴定(KMnO4溶液与尿素不反应),平行实验三次,实验结果如下:
实验序号 | 1 | 2 | 3 | |
KMnO4溶液体积/mL | 滴定前读数 | 0.00 | 0.00 | 2.00 |
滴定后读数 | 19.98 | 21.70 | 22.02 | |
①KMnO4溶液应盛放在__________滴定管中,滴定终点的现象是_____________。
②产品中活性氧的质量分数为____________。
③若滴定前滴定管尖嘴处无气泡,滴定后有气泡,会使测得的活性氧含量__________(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
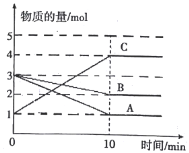
【题目】将一定量的A、B、C三种物质(都是气体)放入固定体积为1L的密闭容器中,一定条件下发生反应,一段时间内测得各物质的物质的量变化如下图所示。请回答下列问题:
(1)反应的化学方程式用A、B、C可表示为____________。
(2)用A表示在0~10min内的反应速率____________。
(3)在该条件达到反应的限度时反应物B的转化率为_____________。(计算结果用百分数表示,并保留1位小数)
(4)开始时容器中的压强与平衡时的压强之比为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝氢化钠(NaAlH4)是有机合成的重要还原剂,其合成线路如下图所示。

(1)制备无水AlCl:
实验装置如下。已知AlCl3178℃升华,在潮湿的空气中易水解。

①实验时应先点燃_______(填“A”或“D”)处酒精灯,当观察到_______时,再点燃另一处酒精灯。
②装置F的作用是_________________。
(2)制取铝氢化钠
制取铝氢化钠的化学方程式是_________________,AlCl3配成有机溶液的目的是__________。
(3)铝氢化钠样品性质探究和纯度测定
①称取一定质量实验制得的铝氢化钠样品(除含产物杂质外,还可能含有过量的NaH),滴加足量的水,观察到产生气体,该气体是________________。
②向反应后的溶液中滴加酚酞,溶液变红。猜想可能是生成了NaOH呈碱性,也可能
是_________________。为验证猜想,可再逐滴滴加盐酸并振荡,当观察到____________时,即可证明两种猜想均成立。
③设计如下两种装置测定生成气体的体积(若其他操作一致),用甲装置测得铝氢化钠的含量________乙装置。(填“大于”、“小于”或“等于”)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com