
【题目】下列不属于电离方程式的是( )。
A.2H2O ![]() H3O++OH-B.CH3COOH+H2O
H3O++OH-B.CH3COOH+H2O ![]() CH3COO-+H3O+
CH3COO-+H3O+
C.H2CO3![]() H++HCO3-D.CH3COOH+NaOH = CH3COONa+H2O
H++HCO3-D.CH3COOH+NaOH = CH3COONa+H2O
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】硫代硫酸钠![]() 是一种重要的化工产品,将
是一种重要的化工产品,将![]() 通入
通入![]() 和
和![]() 混合溶液中可制得
混合溶液中可制得![]() 。其制备装置如下图所示。
。其制备装置如下图所示。

(1)![]() 中反应的化学方程式为________。
中反应的化学方程式为________。
(2)为保证![]() 和
和![]() 得到充分利用,两者的物质的量之比应为________。
得到充分利用,两者的物质的量之比应为________。
(3)为了保证硫代硫酸钠的产量,实验中通入的![]() 不能过量,原因是________。
不能过量,原因是________。
(4)待![]() 和
和![]() 完全消耗后,结束反应。过滤B中的混合物,滤液经过________、________
完全消耗后,结束反应。过滤B中的混合物,滤液经过________、________![]() 填操作名称
填操作名称![]() 、过滤、洗涤、干燥,得到
、过滤、洗涤、干燥,得到![]() 晶体。
晶体。
(5)称取![]() 产品
产品![]() ,相对分子质量为
,相对分子质量为![]() ,配成250mL溶液,取
,配成250mL溶液,取![]() 溶液,以淀粉作指示剂,用
溶液,以淀粉作指示剂,用![]() 碘的标准溶液滴定。
碘的标准溶液滴定。![]() 反应原理为:
反应原理为:![]() ,忽略
,忽略![]() 与
与![]() 反应
反应![]() 。
。
①滴定终点的现象为________。
②重复三次的实验数据如表所示,其中第三次读数时滴定管中起始和终点的液面位置如图所示,则![]() ________,产品的纯度为________。
________,产品的纯度为________。

实验序号 | 消耗标准溶液体积 |
1 |
|
2 |
|
3 | x |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室制备乙酸乙酯的化学方程式:CH3COOH+C2H5OH![]() CH3COOC2H5+H2O,为证明浓硫酸在该反应中起到了催化剂和吸收剂的作用,某同学利用下图所示装置进行了以下四个实验,实验开始先用酒精灯微热3 min,再加热使之微微沸腾3min。实验结束后充分振荡试管Ⅱ再测有机层的厚度,实验记录如下:
CH3COOC2H5+H2O,为证明浓硫酸在该反应中起到了催化剂和吸收剂的作用,某同学利用下图所示装置进行了以下四个实验,实验开始先用酒精灯微热3 min,再加热使之微微沸腾3min。实验结束后充分振荡试管Ⅱ再测有机层的厚度,实验记录如下:
实验编号 | 试管Ⅰ中的试剂 | 试管Ⅱ中试剂 | 测得有机层的厚度/cm |
A | 2 mL乙醇、2 mL乙酸、1 mL 18 mol·L-1浓硫酸 | 饱和碳酸钠 溶液 | 5.0 |
B | 3 mL乙醇、2 mL乙酸 | 0.1 | |
C | 3 mL乙醇、2 mL乙酸、6mL 3 mol·L-1硫酸 | 1.2 | |
D | 3 mL乙醇、2 mL乙酸、盐酸 | 1.2 |
(1)实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是________mL和________mol/L。
(2)分析实验________(填实验编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是_____________________。
(3)加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是______________(答出两条即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷化镓是继硅之后研究最深人、应用最广泛的半导体材料。回答下列问题:
(1)Ga基态原子核外电子排布式为________________,As基态原子核外有__________个未成对电子。
(2)Ga、As、Se的第一电离能由大到小的顺序是__________,Ga、As、Se的电负性由大到小的顺序是__________________。
(3)比较下列镓的卤化物的熔点和沸点,分析其变化规律及原因:________,GaF的熔点超过1000℃,可能的原因是__________________________。
(4)二水合草酸镓的结构如图1所示,其中镓原子的配位数为__________,草酸根离子中碳原子的杂化轨道类型为__________。
(5)砷化镓的立方晶胞结构如图2所示,晶胞参数为a=0.565nm,砷化镓晶体的密度为__________g·cm-3(设NA为阿伏加德罗常数的值,列出计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项叙述中,正确的是
A.AB3型的分子空间构型一定为平面三角形
B.电负性相差越大的元素间越易形成离子键
C.分子晶体中,分子间作用力越大,分子越稳定
D.用于幽门螺旋杆菌示踪的![]() 价电子排布为2s22p3
价电子排布为2s22p3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用电解对含氮生活污水进行处理。若污水中含有Cl-,主要靠有效氯(HC1O、ClO-)将NH4+氧化为N2。其工作原理如图所示,下列分析正确的是
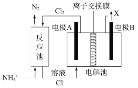
A.电极A为阴极
B.电极B上发生电极反应:2H++2e-=H2↑
C.电解池中离子交换膜为阴离子交换膜
D.处理含l mol NH4+的废水,反应池中共转移电子数目为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)25℃下,纯水中c(H+)=1×10-7 mol·L-1,则此时c(OH-)=______________,该温度下向纯水中加盐酸,使溶液中的c(H+)=1×10-3 mol·L-1,则此时溶液的pH=_______________。若25℃下,向纯水中加入NaOH固体,使溶液的pH=13,此时溶液中c(OH-)=___________。 与纯水的电离相似,液氨中也存在着微弱的电离:2NH3 ![]() NH4++NH2-,请写出液氨的电离平衡常数表达式K =____________________________。
NH4++NH2-,请写出液氨的电离平衡常数表达式K =____________________________。
(2)同素异形体相互转化的反应热相当少而转化速率慢,有时还很不完全,测定时很 困难,现可依据盖斯定律进行计算。已知:
P4 (白磷,s) + 5O2 (g) = 2P2O5 (s); △H1 =-283.2 kJ·mol-1 ①
4P (红磷,s) + 5O2 (g) = 2P2O5 (s); △H2 =-184.0kJ·mol-1 ②
由热化学方程式看来,更稳定的磷的同素异形体是 ______(填“白磷”或“红磷”) ,试写出白磷转化成红磷的热化学方程式______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)[Fe2(OH)n(SO4)3-0.5n]m和绿矾FeSO4·7H2O,其过程如图所示,下列说法不正确的是
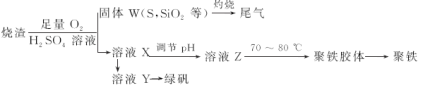
A.炉渣中FeS与硫酸、氧气反应的离子方程式为:4FeS+3O2+12H+=4Fe3++4S+6H2O
B.溶液Z加热到70~80 ℃的目的是促进Fe3+的水解
C.溶液Y经蒸发浓缩、冷却结晶、过滤等步骤可得到绿矾
D.溶液Z的pH影响聚铁中铁的质量分数,若pH偏小导致聚铁中铁的质量分数偏大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应C(s)+H2O(g)![]() CO(g)+H2(g),ΔH=+206.4 kJ·mol-1,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是
CO(g)+H2(g),ΔH=+206.4 kJ·mol-1,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是
A.升高温度B.增大水蒸气浓度
C.加入大量CD.降低压强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com