
【题目】下列各项叙述中正确的是
A. 同一原子中,能层序数越大,s原子轨道的形状相同,半径越大
B. 在同一能层上运动的电子,其自旋方向肯定不同
C. 镁原子由1s22s22p63s2→1s22s22p63p2时,释放能量,由基态转化成激发态
D. 杂化轨道可用于形成σ键、π键或用于容纳未参与成键的孤电子对
 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
【题目】电离平衡是溶液化学中的重要内容,某化学兴趣小组拟以乙酸为例探究弱酸的性质。
(1)实验一:氢氧化钠标准溶液的配制。
现要配制0.1000mol/LNaOH标准溶液250mL,需要用到的玻璃仪器有玻璃棒、烧杯、胶头滴管和______,操作过程中如果没有将烧杯等的洗涤液一并转入容量瓶,在其它操作都正确的情况下,将该标准溶液用来滴定下列(2)中的未知浓度的乙酸溶液,将会使侧定的结果偏_(填“高”、“低”、“不影响”)
(2)实验二:现有一瓶乙酸溶液,常温下测定其中乙酸的电离平衡常数。设计实验方案,将待测物理量和对应的测定方法填写在下表中。
待测物理量 | 测定方法 |
①_______ | 量取25.00mL乙酸溶液于锥形瓶中,滴加指示剂,将0.1000mol/LNaOH标准溶液装入碱式滴定管,滴定至终点,记录数据。重复滴定2次。 |
②H+的物质的量浓度 | 取适最乙酸溶液于烧杯中,用______测定溶液pH。 |
③ 上述实验中,如果在某温度时测得乙酸溶液的物质的量浓度为0.1000mol/L,pH=3,则在该温度时乙酸的电离平衡常数为____________。
(3)实验三:探究酸的强弱对酸与镁条反应速率的影响。
① 设计实验方案如下表,表中c=_______g。
编号 | 酸的种类 | 酸的浓度(mol/L) | 酸的体积/mL | 镁条质量/g |
l | 乙酸 | 0.5 | 17.0 | 2.0 |
2 | 盐酸 | 0.5 | 17.0 | c |
② 实验步骤:
a)下图的装置中,在添加药品之前必须________;
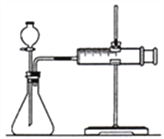
b)反应开始后,__________;
c)将所记录的欲据绘制成曲线图(下图)。

③ 写出镁与乙酸溶液反应的离子方程式:_______________。
④ 描述O~5min盐酸与镁条反应的反应速率变化规律:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.在①苯 ②苯酚 ③甲苯 ④氯乙烷 ⑤乙烯 ⑥乙醇中,(填编号)
<1>能和金属钠反应放出H2的有______ <2>能与NaOH溶液反应的有______
<3>常温下能与溴水反应的有_________ <4>能使酸性KMnO4溶液褪色的烃有_______
II.已知某有机物的结构简式为: ![]()
①该有机物中所含官能团的名称是________________________。
②该有机物发生加聚反应后,所得产物的结构简式为__________。
③写出该有机物发生消去反应的化学方程式(注明反应条件):_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.2 mol·L-1的NaOH溶液滴定10.00mL0.2 mol·L-1一元酸HA溶液,溶液的温度和pH随加入NaOH溶液体积(V)的变化曲线如图所示。下列有关说法不正确的是
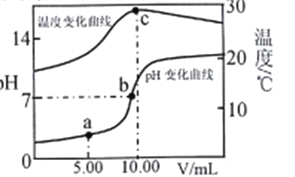
A. HA是弱酸
B. c点水的离子积最大
C. c点后温度降低主要原因是NaA水解吸热
D. 在a、b点之间(不包括b点)一定有c(A-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为一种微生物燃料电池结构示意图,下列叙述正确的是

A. 放电过程中,电子从正极转移到负极
B. 放电过程中,H+从正极区移向负极区
C. 正极反应式为:MnO2+4H++2e- =Mn2++2H2O
D. 若C m(H2O)n是葡萄糖,当电路中转移了6NA电子时,消耗的葡萄糖是1mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示。下列说法错误的是( )
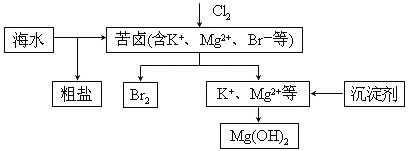
A. 向苦卤中通入Cl2是为了提取溴
B. 工业生产中常选用NaOH作为沉淀剂
C. 粗盐可采用除杂和重结晶等过程提纯
D. 富集溴一般先用空气和水蒸气吹出单质溴,再用![]() 将其还原吸收
将其还原吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列物质进行分类:
A.O2和O3 B. ![]() C和
C和![]() C C.CH2=CH-CH3和CH2=CH-CH2-CH3
C C.CH2=CH-CH3和CH2=CH-CH2-CH3
D.淀粉和纤维素 E.葡萄糖和蔗糖
F. G.
G.
(1)互为同位素的是 ________________(填编号,下同);
(2)互为同素异形体的是____________;
(3)互为同分异构体的是____________;
(4)互为同系物的是____________;
(5)同一物质是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,FeS和ZnS的饱和溶液中,金属阳离子与S2-的物质的量浓度的负对数关系如图所示。下列说法正确的是

A. 溶解度S(FeS)<S(ZnS)
B. a点表示FeS的不饱和溶液,且c(Fe2+)>c(S2-)
C. 向b点对应溶液中加入Na2S溶液,可转化为c点对应的溶液
D. 向c点对应的溶液中加入Na2S溶液,ZnS的KSP增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不能用于金属防腐处理的是( )
A. 涂油漆 B. 海轮在海洋上航行,为防止船体腐蚀,常在船体上镶上铜块
C. 在金属表面进行电镀 D. 改变金属内部结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com