


科目:高中化学 来源: 题型:
| A、由水电离的c(H+)=1×10-12mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| B、使甲基橙呈黄色的溶液中:I-、Cl-、NO3-、Na+ |
| C、pH=10的溶液中:Na+、Cl-、SO42-、NO3- |
| D、含有CO32-的溶液中:K+、C6H5OH、Cl2、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 ⑦O2和O3 ⑧CH3CH(CH3)CH3和CH(CH3)3 ⑨金刚石和石墨.
⑦O2和O3 ⑧CH3CH(CH3)CH3和CH(CH3)3 ⑨金刚石和石墨.查看答案和解析>>
科目:高中化学 来源: 题型:
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色K2FeO4和KNO2等产物 |
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色Na2FeO4溶液 |
| ||
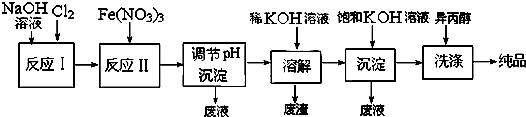
查看答案和解析>>
科目:高中化学 来源: 题型:
 下面a~e是中学化学实验中常见的几种定量仪器:
下面a~e是中学化学实验中常见的几种定量仪器:| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol?L-1盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com