
【题目】一定条件下反应mA(g)+nB(g)![]() pC(g)+qD(g)在一密闭容器中进行,测得平均反应速度v(C)=2v(B)。若反应达平衡后保持温度不变,加大体系压强时平衡不移动,则m、n、p、q的数值可以是( )
pC(g)+qD(g)在一密闭容器中进行,测得平均反应速度v(C)=2v(B)。若反应达平衡后保持温度不变,加大体系压强时平衡不移动,则m、n、p、q的数值可以是( )
A.2、6、3、5B.3、1、2、2
C.3、1、2、1D.1、3、2、2
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积为1L的容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图所示,则下列表述中正确的是( )

A.该反应的化学方程式为2M![]() N
N
B.t2时,正、逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A. pH=1的溶液中:Fe2+、NO3﹣、Na+、SO42﹣
B. 水电离出的c(H+)=10﹣12mol/L的溶液中:Ca2+、K+、Cl﹣、HCO3﹣
C. c(H+)/c(OH—)=1012的水溶液中:NH4+、Al3+、NO3﹣、Cl﹣
D. c(Fe3+)=0.1mol/L的溶液中:K+、ClO﹣、SO42﹣、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaCO3广泛存在于自然界,是一种重要的化工原料。大理石主要成分为CaCO3,另外有少量的含硫化合物。实验室用大理石和稀盐酸反应制备CO2气体。下列装置可用于CO2气体的提纯和干燥。完成下列填空:

(1)用浓盐酸配制1:1(体积比)的稀盐酸(约6 mol·L-1),需要的玻璃仪器有___________
(2)上述装置中,A是___________溶液,其作用是___________ 。
(3)上述装置中,B物质是___________。
(4)一次性饭盒中石蜡和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重
①从物质分类的角度分析,石蜡属于有机物中的____________类,为了将石蜡从饭盒中溶出,应选用下列试剂中的__________。
a.氯化钠溶液 b.稀醋酸 c.稀硫酸 d 正已烷
②饭盒中的碳酸钙常用稀醋酸将其溶出,试写出其反应的离子方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图示法和图像法都是常用的科学研究方法。
(1)科学家通过X射线推测胆矾中既含有配位键又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示。

①写出基态Cu原子的核外电子排布式________________________________。
②写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来)________。
(2)下图是研究部分元素氢化物的沸点变化规律的图像,折线c可以表达出第________族元素氢化物的沸点变化规律。两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线——折线a和折线b,你认为正确的是________(填“a”或“b”),理由是______________________________________________________________。

(3)第三周期元素的气态电中性基态原子失去最外层一个电子转化为气态基态正离子所需的最低能量叫做第一电离能(设为E)。如图所示:

①同周期内,随着原子序数的增大,E值变化的总趋势是________;
②根据图中提供的信息,试推断E氧________E氟(填“>”、“<”或“=”,下同);
③根据第一电离能的含义和元素周期律,试推断E镁________E钙。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸溶液中存在电离平衡CH3COOH![]() H++CH3COO-,不正确的是( )
H++CH3COO-,不正确的是( )
A. 醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-)
B. 常温下0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)减小
C. CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动
D. 常温下pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双氟磺酰亚胺锂[LiN(SO2F)2]是具有广泛应用前景的电解质溶液,氮化锂(Li3N)是合成它的原料之一,氮化锂遇水剧烈反应。实验室用饱和NH4Cl溶液和NaNO2溶液共热制N2,N2和锂在加热条件下反应生成氮化锂。某小组设计下列装置制备Li3N。下列说法正确的是( )
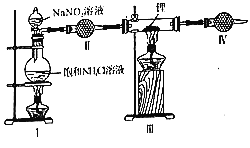
A.装置Ⅱ中盛装无水硫酸铜,检验氮气中水蒸气
B.实验时,先点燃Ⅰ处酒精灯,后点燃Ⅲ处酒精灯
C.装置Ⅳ的作用是吸收尾气,避免污染环境
D.若Li3N产品含少量Li,利用与水反应生成气体的量测其纯度会偏低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ZrO2常用作陶瓷材料,可由锆英砂(主要成分为ZrSiO4,还含少量FeCO3、Fe2O3、Al2O3、SiO2等杂质)通过如下流程制取。
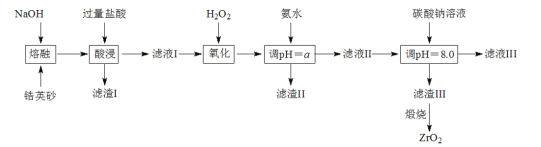
已知:①ZrSiO4能与烧碱反应生成Na2ZrO3和Na2SiO3,Na2ZrO3与酸反应生成ZrO2+
②部分金属离子在实验条件下开始沉淀和完全沉淀的pH如下表。
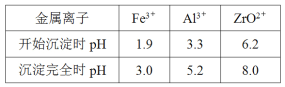
(1)“熔融”过程中, ZrSiO4发生反应的化学方程式是______________________滤渣I的化学式为_______________
(2)“氧化”过程中,发生反应的离子方程式是__________________调“pH=a”时,a的范围是________________
(3)为得到纯净的ZrO2,滤渣Ⅲ要用水洗,检验沉淀是否洗涤干净的方法是________________
(4)滤渣Ⅲ的成分是Zr(CO3)2·xZr(OH)4取干操后的滤渣Ⅲ 37.0g,煅烧后可得到24.6 g ZrO2则x等于____________________,“调pH=8.0”时,所发生反应的离子方程式为________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关说法正确的是( )
A.![]() 分子中仅含极性共价键
分子中仅含极性共价键
B.钢管被原油中的含硫化合物腐蚀属于化学腐蚀
C.乙酸与用18O标记的乙醇反应得到的有机产物为C2H5O18OCCH3
D.NH4Br的电子式: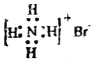
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com