
| A. | 分子式为C5H12的烃有三种可能的结构 | |
| B. | 乙烯和聚乙烯均能和溴水发生加成反应而使溴水褪色 | |
| C. | 苯乙烯在合适条件下催化加氢可生成乙基环己烷 | |
| D. | 淀粉、纤维素和蛋白质都是高分子化合物,它们在一定条件下都能水解 |
分析 A.分子式为C5H12的烃为戊烷,有正戊烷、异戊烷、新戊烷;
B.聚乙烯没有不饱和键;
C.苯乙烯中碳碳双键、苯环在合适条件下都能催化加氢;
D.淀粉、纤维素和蛋白质都是高分子化合物,淀粉、纤维素水解生成葡萄糖,蛋白质水解生成氨基酸.
解答 A.分子式为C5H12的烃为戊烷,有正戊烷、异戊烷、新戊烷,共3种同分异构体,故A正确;
B.聚乙烯没有不饱和键,不能和溴水发生加成反应而使溴水褪色,故B错误;
C.苯乙烯中碳碳双键、苯环在合适条件下都能催化加氢,生成乙基环己烷,故C正确;
D.淀粉、纤维素和蛋白质都是高分子化合物,淀粉、纤维素水解生成葡萄糖,蛋白质水解生成氨基酸,故D正确.
故选B.
点评 本题考查了有机物的同分异构体、反应类型、有机高分子化合物,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 取样,若加入淀粉溶液,溶液显蓝色,则一定有I- | |
| B. | 取样,若加入AgNO3溶液由白色沉淀,则一定有Cl- | |
| C. | 取样,若加入BaCl2溶液,有白色沉淀产生,则一定有SO42- | |
| D. | 取样,若加入NaOH溶液,微热,产生使湿润红色石蕊试纸变蓝的气体,则一定有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{a+b}{5}×100%$ | B. | $\frac{2(a+b)}{5b}×100%$ | C. | $\frac{2(a+b)}{5}×100%$ | D. | $\frac{a+b}{5a}×100%$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15种 | B. | 13种 | C. | 11种 | D. | 9种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 反应在前50 s 的平均速率v(PCl3)=0.0032 mol•L-1•s-1 | |
| B. | 相同温度下,起始时向容器中充入1.0 mol PCl5、0.20mol PCl3 和0.20 mol Cl2,反应达到平衡前v(正)>v(逆) | |
| C. | 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol•L-1,则反应的△H<0 | |
| D. | 相同温度下,起始时向容器中充入2.0 mol PCl3 和2.0mol Cl2,达到平衡时,PCl3 的转化率小于80% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.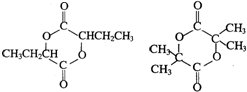 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
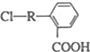 (其中R为饱和烃基),X在一定条件下如图所示的转化关系,已知Q的蒸气密度是相同条件下H2密度的74倍,分子组成符号CaHbO2
(其中R为饱和烃基),X在一定条件下如图所示的转化关系,已知Q的蒸气密度是相同条件下H2密度的74倍,分子组成符号CaHbO2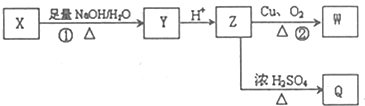
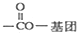 ),写出任意一种能发生银镜反应的符合上述条件的物质的结构简式
),写出任意一种能发生银镜反应的符合上述条件的物质的结构简式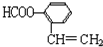
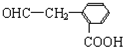 .于由X通过一步反应得到P,该反应的化学方程式是
.于由X通过一步反应得到P,该反应的化学方程式是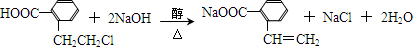
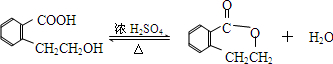 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | A | B | C | |||||
| 3 | D | E | F | G | H | |||
| 4 | I | J |
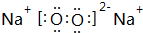 ,该化合物是由离子和共价键形成.
,该化合物是由离子和共价键形成.| 实验步骤 | 实验现象 |
| ①将E单质用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | 1.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②向新制的Na2G溶液中滴加新制的单质H的水溶液 | 2.有气体产生,溶液变成浅红色 |
| ③将一小块金属D放入滴有酚酞溶液的冷水中 | 3.剧烈反应,迅速产生大量无色气体. |
| ④将单质E投入稀盐酸中 | 4.反应开始不十分剧烈,产生无色气体. |
| ⑤将单质F投入稀盐酸中 | 5.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向FH3溶液中滴加DOH溶液至过量 | 6.生成淡黄色沉淀. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
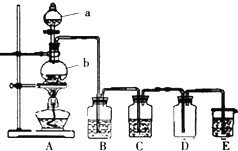
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com