
【题目】(1)写出制取硝基苯的化学反应方程式_________________________________;
(2)写出镁铝氢氧化钠原电池的负极电极反应式___________________________;
(3)氯气是重要的化工原料,可以用来制备很多化工产品,比如可以制备净水剂高铁酸钾(K2FeO4),写出碱性条件下,由氯化铁制备高铁酸钾的离子方程式___________;
写出工业制漂白粉的化学反应方程式__________________________。
【答案】  Al—3e-+4OH-=AlO2-+2H2O 2Fe3++3Cl2+16OH-=2FeO42-+6Cl-+8H2O 2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
Al—3e-+4OH-=AlO2-+2H2O 2Fe3++3Cl2+16OH-=2FeO42-+6Cl-+8H2O 2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
【解析】(1)实验室用浓硝酸和苯在浓硫酸作用下制备硝基苯,反应的化学方程式为![]() ;
;
(2)因为Al可以与NaOH溶液反应而Mg不能,所以负极是Al,正极是Mg,负极反应为:2Al-6e-+4OH-=2AlO2-+2H2O;
(3)用氯气在碱性条件下氧化氯化铁制备高铁酸钠,根据电子得失守恒以及原子守恒可得,反应的离子方程式为2Fe3++3Cl2+16OH-=2FeO42-+6Cl-+8H2O;工业用氯气和石灰乳反应制漂白粉,化学反应方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】铜、银、金与社会生活联系密切,请回答下列相关问题。
(1)在元素周期表中,铜、银、金元素位于同一族,它们基态原子的价层电子排布式中各能级上的电子数相等,各能层数依次增大,其通式为________(用n表示核外电子层数);铜元素所在周期中,基态原子未成对电子数最多的原子M 的价层电子轨道表达式为___________。
(2)乙醛是重要的化工原料,① CH3CH2OH 、CH3CHO的沸点分别为78.5℃、20.8℃,它们的相对分子质量相差2,而沸点相差比较大,其主要原因__________。
② 在H、C、N、O中,第一电离能最大的元素和电负性最大的元素组成的化合物的化学式为_____(填一种即可),CH4、NH3、H2O分子的键角从大到小的顺序为__________。
(3)金不溶于硝酸,但溶于“王水”,发生如下反应:Au + 4HCl+ HNO3 = H [ AuCl4]+NO + 2H2O,金溶于王水的主要原因是形成了[ AuCl4]-,提高了金的活泼性。在[ AuCl4]-中配位键的数目为______,写出该离子的结构式:_____________。
(4)金、银的一种合金具有较强的储氢能力。该合金的晶胞为面心立方结构,银原子位于面心,金原子位于顶点。该合金的化学式可以表示为__________。
(5)Cu(OH)2难溶于氢氧化钠溶液,但是易溶于浓氨水,用离子方程式表示其主要原因:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、社会密切相关。下列有关说法正确的是
A. 在人体内酶的作用下,纤维素可以发生水解生成葡萄糖
B. 福尔马林(甲醛溶液)可用于浸泡生肉及海产品以防腐保鲜
C. 新型材料聚酯纤维、光导纤维都属于有机高分子材料
D. 医药中常用酒精来消毒,是因为酒精能够使病毒的蛋白质发生变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室获取氮气有很多种途径,常见的3种方法是:
方法一:将氨气通入灼热的氧化铜粉末,得到纯净的氮气和铜;
方法二:将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末;
方法三:将亚硝酸钠(NaNO2)和氯化铵的混合溶液加热,氮元素全部转化为氮气。进行实验时可选择的实验仪器如下图所示(省略夹持装置与加热装置):
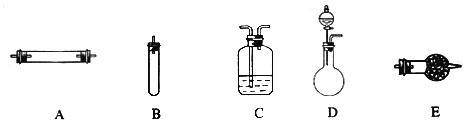
(1)方法一:制氮气所需的氨气可以用浓氨水滴加到生石灰中得到,此反应的发生装置最好选用________________(选填装置编号)。请写出生石灰在此反应中的两个作用____________、___________。
(2)方法二:为保证所得氮气尽可能纯净,除了使用铜外,还可以向装置__________(选填装置编号)中加入____以除去其它杂质气体。
(3)方法三:制氮气的化学方程式为_____________________________。
(4)绿色化学是指在制造和应用化学产品时应有效利用(最好可再生)原料,消除废物和避免使用有毒的和危险的试剂与溶剂。在制取氮气的3种方法中,联合使用方法一和方法二与单独使用方法三相比,具有很多优越性,请从绿色化学的角度进行评价:______________。
(5)1892年,英国科学家瑞利(( Rayleigh)发现,采用方法二得到的氮气在相同条件下比方法三得到的氮气密度总是偏大50‰左右。若上述实验设计与操作均无错误,且氮气已完全干燥,请解释产生这一现象的原因:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. lmolNaCl 固体中含有NA个Na+
B. 18gD2O和18gH2 O中含有的质子数均为10NA
C. 标准状况下2.24LH2O 含有的共价键数为0.2NA
D. 密闭容器中2molNO 与lmolO2充分反应,产物的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列5种基团中的2个不同基团两两组合,形成的有机物能与NaOH反应的有
①一OH ②一CH3 ③—COOH ④一CHO ⑤一C6H5
A. 2种 B. 3种 C. 4种 D. 5种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com