
����Ŀ�����º����£���2 L�ܱ������м���MgSO4(s)��CO(g)��������Ӧ��MgSO4(s)��CO(g)![]() MgO(s)��CO2(g)��SO2(g)����Ӧ�����вⶨ�IJ������ݼ��±���
MgO(s)��CO2(g)��SO2(g)����Ӧ�����вⶨ�IJ������ݼ��±���
��Ӧʱ��/min | n(MgSO4)/mol | n(CO)/mol | n(SO2) / mol |
0 | 2.0 | 2.0 | 0 |
2 | 0.8 | ||
4 | 1.2 | ||
6 | 1.2 | 2.8 |
����˵����ȷ����
A. 0��2 min�ڵ�ƽ������Ϊ�� (CO)��0.6 mol/(L��min)
B. 4 min��ƽ���ƶ���ԭ����������������м�����2.0 mol��SO2
C. �������¶ȣ���Ӧ��ƽ�ⳣ����Ϊ1.0��������ӦΪ���ȷ�Ӧ
D. �������������䣬��ʼʱ������MgSO4��CO��Ϊ1.0 mol����ƽ��ʱn(SO2)=0.6 mol
���𰸡�B
�����������������A���ɱ���ʱ���֪��0��2min��CO�����ʵ����仯��Ϊ2mol-0.8mol=1.2mol������(CO)��![]()
="0.3" molL-1min-1����A����B���ɱ������ݽ�Ϸ���ʽ��֪��0��2min��CO��CO2��SO2�����ʵ����仯��Ϊ2mol-0.8mol=1.2mol������2��4minʱ��ƽ��״̬��4��6minʱ��CO������0.4mol������ƽ���ƶ���ԭ��������������м�����2.0 mol��SO2����B��ȷ��C���ɱ���ʱ���֪��
MgSO4(s)+CO(g)![]() MgO(s)+CO2(g)+SO2(g)
MgO(s)+CO2(g)+SO2(g)
��ʼ��mol���� 2 0 0
�仯��mol���� 1.2 1.2 1.2
ƽ�⣨mol���� 0.8 1.2 1.2
�ʸ��¶���ƽ�ⳣ��k=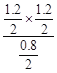 =0.9���������¶ȣ���Ӧ��ƽ�ⳣ����Ϊl.0����ƽ��������Ӧ�����ƶ�����������ӦΪ���ȷ�Ӧ����C����D����1L�ܱ������г���1.0mol MgSO4��1.0molCO����ԭƽ���ǵ�Чƽ�⣬n(CO2)=0.60mol�����������ݻ�����2Lʱ��ƽ�������ƶ����ʵ���ƽ��ʱn(CO2)��0.60mol����D����ѡB��
=0.9���������¶ȣ���Ӧ��ƽ�ⳣ����Ϊl.0����ƽ��������Ӧ�����ƶ�����������ӦΪ���ȷ�Ӧ����C����D����1L�ܱ������г���1.0mol MgSO4��1.0molCO����ԭƽ���ǵ�Чƽ�⣬n(CO2)=0.60mol�����������ݻ�����2Lʱ��ƽ�������ƶ����ʵ���ƽ��ʱn(CO2)��0.60mol����D����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʷ������ȷ����ǣ� ��
������� | ������ | ����� | ���������� | ���������� |
A. | Ư�� | ��ˮ | ������̼ | ������ |
B. | �ɱ� | ̼��� | һ������ | ���������� |
C. | CaCl2��8NH3 | ˮ | �������� | �������� |
D. | Һ�� | �Ȼ��� | �������� | ������ |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʵķ�����ȷ���ǣ�������
A. SO2��SiO2��CO������������
B. ϡ���������ᡢ�Ȼ�����Һ��Ϊ����
C. ���ᡢ���ᡢ������Ϊǿ��
D. ��ˮ��ˮ��������ˮ��Ϊ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���10 mL 0.40 mol/L H2O2��Һ�м�������FeCl3��Һ����ͬʱ�̲������O2�������������Ϊ��״�������±���ʾ��������ʾ����Ӧ���������У�
��2Fe3++ H2O2 ![]() 2Fe2++ O2��+ 2H+���� H2O2 + 2Fe2+ + 2H+
2Fe2++ O2��+ 2H+���� H2O2 + 2Fe2+ + 2H+ ![]() 2Fe3++2H2O��
2Fe3++2H2O��
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
��Ӧ�����������仯����ͼ��ʾ��

����˵������ȷ����
A. 0��6 min��ƽ����Ӧ���ʣ�v(H2O2) = 3.33��10-2 mol/( L��min)
B. Fe3+�������������������ķֽ�����
C. ��Ӧ�������ȷ�Ӧ����Ӧ���Ƿ��ȷ�Ӧ
D. ��Ӧ2H2O2(aq) ![]() 2H2O(l) + O2(g)����H > 0
2H2O(l) + O2(g)����H > 0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ʵ���Żش𣺢�K2SO4���� ���� ������ ��ϡ���� �ڳ������ܵ������ �� ���ڵ���ʵ��� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��14gͭ��Ͻ���������ijŨ��HNO3��Ӧ����������������2.24L(��״��)O2��ϣ�ͨ��ˮ�У�����ǡ�ñ���ȫ���գ���Ͻ���ͭ������Ϊ�� ��
A.9.6gB.6.4gC.12.8gD.1.6g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ̽����ҵ���ϵ������ã�ij��ѧ��ȤС���������ͼʵ�鷽�����ú�����������ͭ�ĺϽ���ȡ�Ȼ������̷����壨FeSO47H2O���͵������塣

��ش�
��1��������о�����е�ʵ�������_______________��ʵ�����н��иò���ʱ���õ��IJ����������ձ���______________________��
��2����ҺA�е���������Ҫ��__________________���ɺϽ�����A��Һ�����ӷ���ʽΪ��_______________���Լ�X��________________��
��3������ҺA��ͨ�����CO2�������ɹ���C�����ӷ���ʽΪ_________________��
��4���ӻ��������Ƕȿ��ǣ����ù���F��������ϡ��������Ȳ�����������Ʊ�CuSO4��Һ���仯ѧ����ʽ��_______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������
A.ͨ������£������ǿ�ᡢǿ�ǿ����������Ӧ
B.�����ʵ����ļ�������������ȡ����Ӧ��������һ�ȼ�������ʵ������
C.������ȴ��ﶼ������ˮ
D.�����¼�������������ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������
A.ʯ�ͷ����������仯���ɵõ����͡�ú�͵�
B.ú��������Һ��Ϊ��ѧ�仯
C.ʯ���ѽ��Ŀ����������͵�����ȼ�͵IJ���������
D.��ά��ˮ�������ˮ��õ������ղ�����ͬ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com