
【题目】研究发现艾滋病治疗药物利托那韦对新型冠状病毒也有很好的抑制作用,它的合成中间体2-异丙基-4-(甲基氨基甲基)噻唑可按如下路线合成:
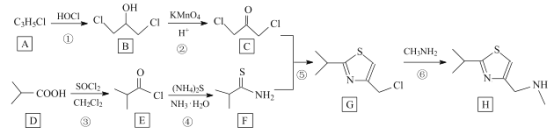
回答下列问题:
(1)A的结构简式是__________,C中官能团的名称为 ______________。
(2)①、⑥的反应类型分别是__________、_____。D的化学名称是______。
(3)E极易水解生成两种酸,写出E与NaOH溶液反应的化学方程式:_______。
(4)H的分子式为 __________________。
(5)I是相对分子质量比有机物 D 大 14 的同系物, 写出I 符合下列条件的所有同分异构体的结构简式:_____________。
①能发生银镜反应 ②与NaOH反应生成两种有机物
(6)设计由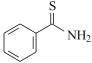 ,和丙烯制备
,和丙烯制备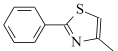 的合成路线______________(无机试剂任选)。
的合成路线______________(无机试剂任选)。
【答案】CH2=CH-CH2Cl 羰基、氯原子 加成反应 取代反应 2-甲基丙酸 ![]() +2NaOH→
+2NaOH→![]() +NaCl+H2O C8H14N2S HCOOCH2CH2CH2CH3、HCOOCH2CH(CH3)2、HCOOCH(CH3)CH2CH3、HCOOC(CH3)3
+NaCl+H2O C8H14N2S HCOOCH2CH2CH2CH3、HCOOCH2CH(CH3)2、HCOOCH(CH3)CH2CH3、HCOOC(CH3)3 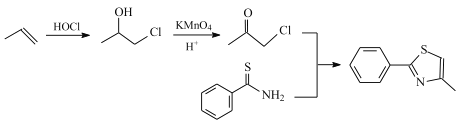
【解析】
根据合成路线中,有机物的结构变化、分子式变化及反应条件分析反应类型及中间产物;根据目标产物及原理的结构特征及合成路线中反应信息分析合成路线;根据结构简式、键线式分析分子式及官能团结构。
(1)根据B的结构及A的分子式分析知,A与HOCl发生加成反应得到B,则A的结构简式是CH2=CH-CH2Cl;C中官能团的名称为羰基、氯原子;故答案为:CH2=CH-CH2Cl;羰基、氯原子;
(2)根据上述分析,反应①为加成反应;比较G和H的结构特点分析,G中氯原子被甲胺基取代,则反应⑥为取代反应;D为![]() ,根据系统命名法命名为2-甲基丙酸;故答案为:加成反应;取代反应;2-甲基丙酸;
,根据系统命名法命名为2-甲基丙酸;故答案为:加成反应;取代反应;2-甲基丙酸;
(3)E水解时C-Cl键发生断裂,在碱性条件下水解生成两种盐,化学方程式为:![]() +2NaOH→
+2NaOH→![]() +NaCl+H2O,故答案为:
+NaCl+H2O,故答案为:![]() +2NaOH→
+2NaOH→![]() +NaCl+H2O;
+NaCl+H2O;
(4)H的键线式为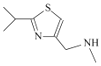 ,则根据C、N、S原子的成键特点分析分子式为C8H14N2S,故答案为:C8H14N2S;
,则根据C、N、S原子的成键特点分析分子式为C8H14N2S,故答案为:C8H14N2S;
(5)I是相对分子质量比有机物 D 大14 的同系物,则I的结构比D多一个CH2原子团;①能发生银镜反应,则结构中含有醛基;②与NaOH反应生成两种有机物,则该有机物为酯;结合分析知该有机物为甲酸某酯,则I结构简式为:HCOOCH2CH2CH2CH3、HCOOCH2CH(CH3)2、HCOOCH(CH3)CH2CH3、HCOOC(CH3)3,故答案为:HCOOCH2CH2CH2CH3、HCOOCH2CH(CH3)2、HCOOCH(CH3)CH2CH3、HCOOC(CH3)3;
(6)根据合成路线图中反应知,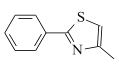 可由
可由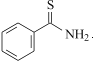 与
与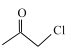 合成得到,
合成得到, 由
由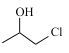 氧化得到,
氧化得到, 可由丙烯加成得到,合成路线为:
可由丙烯加成得到,合成路线为: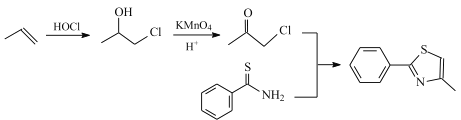 ,故答案为:
,故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】Ⅱ组命题正确且能用I组命题加以解释的是( )
选项 | I组 | Ⅱ组 |
A |
|
|
B |
|
|
C |
|
|
D |
|
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲图为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能,乙图是一种用惰性电极电解饱和食盐水的消毒液发生器。关于甲、乙的说法正确的是
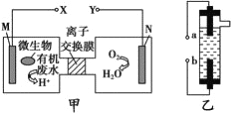
A. 装置乙中的b极要与装置甲的X极连接
B. 装置乙中a极的电极反应式为:2Cl- -2e-=Cl2↑
C. 当N极消耗5.6L(标准状况下)气体时,则有2NA个H+通过离子交换膜
D. 若有机废水中主要含有葡萄糖,则装置甲中M极发生的电极反应为: C6H12O6+6H2O-24e-=6CO2↑+24H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2是一种大气污染物,但它在化工和食品工业上却有广泛应用。某兴趣小组同学对SO2的实验室制备和性质实验进行研究。
(1)甲同学按照教材实验要求设计如图所示装置制取SO2
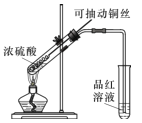
①本实验中铜与浓硫酸反应的化学方程式是 ______,铜丝可抽动的优点是_______。
②实验结束后,甲同学观察到试管底部出现黑色和灰白色固体,且溶液颜色发黑。甲同学认为灰白色沉淀应是生成的白色CuSO4夹杂少许黑色固体的混合物,其中CuSO4以白色固体形式存在体现了浓硫酸的________性。
③乙同学认为该实验设计存在问题,请从实验安全和环保角度分析,该实验中可能存在的问题是________。
(2)兴趣小组查阅相关资料,经过综合分析讨论,重新设计实验如下(加热装置略):
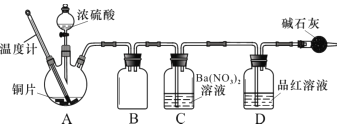
实验记录 A 中现象如下:
序号 | 反应温度/℃ | 实验现象 |
1 | 134 | 开始出现黑色絮状物,产生后下沉,无气体产生 |
2 | 158 | 黑色固体产生的同时,有气体生成 |
3 | 180 | 气体放出的速度更快,试管内溶液为黑色浑浊 |
4 | 260 | 有大量气体产生,溶液变为蓝色,试管底部产生灰白色固体,品红溶液褪色 |
5 | 300 | 同上 |
查阅资料得知: 产物中的黑色和灰白色固体物质主要成分为 CuS、Cu2S 和 CuSO4,其中CuS 和 Cu2S为黑色固体,常温下都不溶于稀盐酸,在空气中灼烧均转化为CuO和SO2。
①实验中盛装浓硫酸的仪器名称为 ____________。
②实验记录表明__________对实验结果有影响,为了得到预期实验现象,在操作上应该____________。
③装置C 中发生反应的离子方程式是 ___________________。
④将水洗处理后的黑色固体烘干后,测定灼烧前后的质量变化,可以进一步确定黑色固体中是否一定含有 CuS其原理为__________(结合化学方程式解释)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,国家电投集团正在建设国内首座百千瓦级铁-铬液流电池储能示范电站。铁-铬液流电池总反应为Fe2+ + Cr3+![]() Fe3 + + Cr2+,工作示意图如图。下列说法错误的是
Fe3 + + Cr2+,工作示意图如图。下列说法错误的是

A.放电时a电极反应为 Fe 3++e- =Fe2+
B.充电时b电极反应为 Cr3++e- =Cr2+
C.放电过程中H+通过隔膜从正极区移向负极区
D.该电池无爆炸可能,安全性高,毒性和腐蚀性相对较低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是一种用途广泛的精细化工产品。工业生产乙酸乙酯的方法很多,如图:

下列说法正确的是
A. 反应①、②均是取代反应
B. 反应③、④的原子利用率均为100%
C. 与乙酸乙酯互为同分异构体的酯类化合物有2种
D. 乙醇、乙酸、乙酸乙酯三种无色液体可用Na2CO3溶液鉴别
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在人们的日常生活、生产和环保事业中属于“明星物质”。回答下列问题:
(1)氨气是农业肥料和化工生产的重要原料,其电子式为____。
(2)叠氮化钠(NaN3)在药物制备、合成影像、化学分析、汽车制造等行业有着广泛的用途,但该物质极易爆炸,且有副毒。可用NaClO溶液对含有叠氮化钠的溶液进行处理,生成一种无污染的气体单质,反应的化学方程式为______________。
(3)“固氮”是农业科学家研究的永恒主题。在某特殊催化剂和光照条件下,N2与水反应可生成NH3。
已知:
(i)4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) △H1=-1266 kJ/mol;
2N2(g) +6H2O(g) △H1=-1266 kJ/mol;
(ii)H2O(g)=H2O(l) △H2= -44.0kJ/mol。
则2N2(g) +6H2O(l)![]() 4NH3(g)+3O2(g) △H3=______kJ/mol。
4NH3(g)+3O2(g) △H3=______kJ/mol。
(4)目前“人工固氮”最成功的应用就是工业合成氨:
N2(g) +3H2(g)![]() 2NH3(g) △H=-92.4kJ/mol。将1.00molN2和3.00molH2充入到容积为3L的恒容密闭容器中,发生上述反应。
2NH3(g) △H=-92.4kJ/mol。将1.00molN2和3.00molH2充入到容积为3L的恒容密闭容器中,发生上述反应。

①图甲是测得X、Y 的浓度随时间变化的曲线.其中Y 为_____(写化学式),反应达到平衡时的平均反应速率v(N2) =_________。
②在不同温度和压强下,平衡体系中NH3的体积分数与温度、压强关系如图乙,则压强p1_____p2(填“>”“<”“=”或“不确定”,下同),B、D 两点的平衡常数KB____KD,B 点N2 的转化率=_________(保留3位有效数字)。
(5)“绿水青山就是金山银山”,利用原电池原理(6NO2 +8NH3=7N2+12H2O)可以处理氮的氧化物和NH3 尾气,装置原理图如图丙:

负极反应式为__________,当有标准状况下4.48 L NO2被处理时,转移电子的物质的量为_____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M 是某香料的有效成分,其分子中含 3 个六元环。M 的一种合成路线如下:
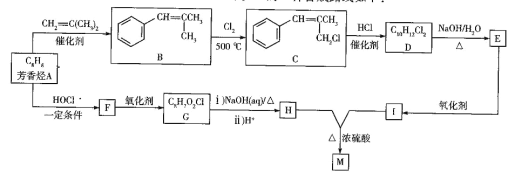
已知:①A 分子中所有原子可能共平面;②D 的核磁共振氢谱上有6个峰;③H 和 I 互为同系物。 请回答下列问题:
(1)A 的名称是____________;E 中所含官能团名称是___________。
(2)B→C 的反应类型是____________。
(3)写出 H 和 I 反应生成 M 的化学方程式:___________。
(4)T是 H 的同分异构体,同时具备下列条件的T有___________种(不考虑立体异构),其中,苯环上一溴代物只有 2 种的结构简式为____________。
①遇FeCl3溶液发生显色反应;②能发生水解反应和银镜反应。
(5)A 酸(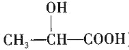 )在医药方面广泛用作防腐剂、载体剂、助溶剂等。参照上述流程,以 2—丁烯和乙烯为原料合成乳酸,设计合成路线:_____________________(无机试剂任选)。
)在医药方面广泛用作防腐剂、载体剂、助溶剂等。参照上述流程,以 2—丁烯和乙烯为原料合成乳酸,设计合成路线:_____________________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下,Ka1(H2CO3)=4.3×10-7,Ka2(H2CO3)=5.6×10-11。某二元酸H2R及其钠盐的溶液中,H2R、HR-、R2-三者的物质的量分数随溶液pH变化关系如图所示,下列叙述错误的是( )
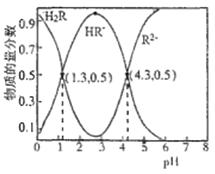
A.在pH=4.3的溶液中:3c(R2-)=c(Na+)+c(H+)-c(OH-)
B.等体积、等浓度的NaOH溶液与H2R溶液混合后,此溶液中水的电离程度比纯水小
C.在pH=3的溶液中存在![]() =10-3
=10-3
D.向Na2CO3溶液中加入少量H2R溶液,发生反应:CO32-+H2R=HCO3-+HR-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com