
【题目】下列叙述错误的是
A.生铁中含有碳,抗腐蚀能力比纯铁弱
B.下图为埋在地下的钢管道采用牺牲阳极保护法防腐
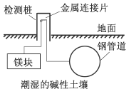
C.金属在一般情况下发生的电化学腐蚀主要是吸氧腐蚀
D.马口铁(镀锡铁)镀层破损后,被腐蚀时首先是镀层被氧化
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】下列各组离子在给定条件下一定能大量共存的是
A.强酸性溶液中:H+、NO![]() 、SO
、SO![]()
B.pH=12的溶液中:OH-、K+、Cl-、HCO![]()
C.加入铝粉能放出氢气的溶液中一定存在:NH![]() 、NO
、NO![]() 、AlO
、AlO![]() 、SO
、SO![]()
D.25C时pH=7的无色溶液中:Na+、Cl-、SO![]() 、K+
、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列应用与反应原理设计不一致的是( )
A.热的纯碱溶液清洗油污:CO![]() +H2O
+H2O![]() HCO
HCO![]() +OH-
+OH-
B.明矾净水:Al3++3H2O![]() Al(OH)3+3H+
Al(OH)3+3H+
C.用TiCl4制备TiO2:TiCl4+(x+2)H2O(过量) ![]() TiO2xH2O↓+4HCl
TiO2xH2O↓+4HCl
D.配制氯化亚锡溶液时加入氢氧化钠:SnCl2+H2O![]() Sn(OH)Cl+HCl
Sn(OH)Cl+HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图所示装置的判断,叙述正确的是( )
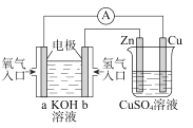
A.左边的装置是电解池,右边的装置是原电池
B.该装置中铜为正极,锌为负极
C.电子流向:Cu→经过CuSO4溶液→Zn→b
D.当铜片的质量变化为12.8g时,a极上消耗的O2在标准状况下的体积为2.24L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型NaBH4/H2O2燃料电池(DBFC)的装置示意图如下,下列叙述正确的是
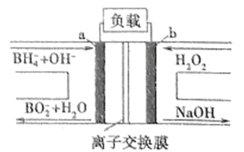
A.b极为正极,发生氧化反应
B.电池应选用阴离子交换膜
C.电子移动方向:电极a→离子交换膜→电极b
D.a极的电极反应式为![]() +8OH--8e-=
+8OH--8e-=![]() +6H2O
+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用特殊电极材料制作的新型二次电池,放电时发生如下图所示的电极反应,下列说法正确的是
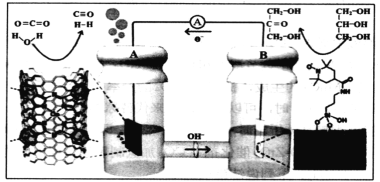
A.A为原电池的负极,失去电子,发生氧化反应
B.B上发生的电极反应为CH2OH(CHOH)CH2OH—2e-=CH2OHCOCH2OH+2H+
C.若通过交换膜的离子是HCO![]() ,则B上发生的电极反应为CH2OH(CHOH)CH2OH—2e-+2HCO
,则B上发生的电极反应为CH2OH(CHOH)CH2OH—2e-+2HCO![]() =CH2OHCOCH2OH+2H2O+2CO2
=CH2OHCOCH2OH+2H2O+2CO2
D.若A处产生的CO和H2的物质的量之比为1:3,则B处消耗丙三醇的物质的量为4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如下图所示装置探究钢铁的腐蚀与防护,烧杯内液体均为饱和食盐水。
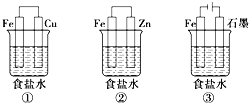
①在相同条件下,三组装置中铁电极腐蚀最快的是__(填装置序号),该装置中正极反应式为__。
②为防止金属Fe被腐蚀,可以采用上述___(填装置序号)装置原理进行防护。
(2)通信用磷酸铁锂电池有体积小、重量轻、高温性能突出、可高倍率充放电、绿色环保等众多优点。磷酸铁锂电池是以磷酸铁锂为正极材料的一种锂离子二次电池,放电时,正极反应式为M1-xFexPO4+e-+Li+=LiM1-xFexPO4,其原理如图所示。
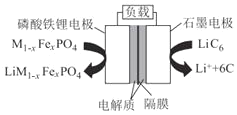
①放电时,电流由___电极经负载流向___电极;负极反应式为____。
②该电池工作时Li+移向___电极;充电时石墨电极接电源的____极。
③该电池的总反应方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在3个体积均为2.0L的恒容密闭容器中,反应CO2(g)+C(s)![]() 2CO(g) H>0分别在一定温度下达到化学平衡状态。下列说法正确的是( )
2CO(g) H>0分别在一定温度下达到化学平衡状态。下列说法正确的是( )
容器 | 温度/K | 起始时物质的量/mol | 平衡时物质的量/mol | ||
n(CO2) | n(C) | n(CO) | n(CO) | ||
Ⅰ | 977 | 0.28 | 0.56 | 0 | 0.4 |
Ⅱ | 977 | 0.56 | 0.56 | 0 | x |
Ⅲ | 1250 | 0 | 0 | 0.56 | y |
A.达到平衡时,向容器Ⅰ中增加C(s)的量,平衡正向移动
B.x=0.8,y>0.4
C.达到平衡时,容器Ⅲ中的CO的转化率小于![]()
D.若起始时向容器Ⅱ中充入0.1molCO2、0.2molCO和足量的C(s),则反应将向正反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2O能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备Cl2O的原理为HgO+2Cl2=HgCl2+Cl2O,装置如图所示。

已知:①Cl2O的熔点为-116℃、沸点为3.8℃,具有强烈刺激性气味、易溶于水;
②Cl2O与有机物、还原剂接触或加热时会发生燃烧并爆炸。
下列说法中正确的是( )
A.装置③中盛装的试剂是饱和食盐水
B.装置④与⑤之间可用橡胶管连接
C.从装置⑤中逸出气体的主要成分是Cl2O
D.通入干燥空气的目的是将生成的Cl2O稀释,减小爆炸危险
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com