
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.标准状况下,22.4 LSO2和SO3混合物中含有的硫原子数目为0.1NA
B.氢氧燃料电池负极消耗1.12L气体时,电路中转移的电子数为0.1NA
C.1mol NaHSO4在熔融状态下电离出的阳离子数为0.2NA
D.在1L 0.5mol/L的Na2CO3溶液中,阴离子总数大于0.5NA
科目:高中化学 来源: 题型:
【题目】从500mL1mol·L-1的CuSO4溶液中取出100mL,下列关于100mL溶液的叙述错误的是()
A.CuSO4的物质的量浓度为1mol·L-1
B.SO42-的物质的量浓度为1mol·L-1
C.含Cu2+的物质的量为0.1mol
D.含CuSO4的质量为80.0g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】借助太阳能将光解水制H2与脱硫结合起来,既能大幅度提高光解水制H2的效率,又能脱除SO2,工作原理如下图所示。下列说法不正确的是
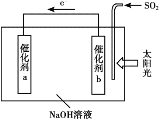
A. 该装置可将太阳能转化为化学能
B. 催化剂b附近的溶液pH增大
C. 吸收1mol SO2,理论上能产生1mol H2
D. 催化剂a表面发生的反应为:2H2O+2e-=H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个电化学过程的示意图,请按要求回答下列问题
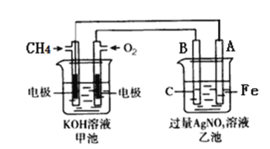
(1)甲池是_______装置(填“原电池”或“电解池”)
(2)写出电极反应式:通入CH4的电极________;A(Fe)电极_______。
(3)反应一段时间后,甲池中消耗1.6g甲烷,则乙池中某电极的质量增加_____g。
(4)反应一段时间后,乙池中溶液成分发生了变化,想要完全恢复到电解前可加入的物质是____
(5)某工厂烟气中主要含SO2,可用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如下图所示(电极材料为石墨)。
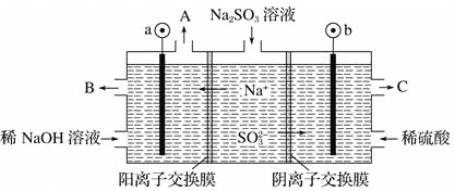
①图中a极要连接电源的______(填“正”或“负”)极,C口流出的物质是______。
②SO32-放电的电极反应式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】干冰、石墨、C60、氟化钙和金刚石的结构模型如下(石墨仅表示其中的一层结构):

回答下列问题:
(1)干冰晶胞中,每个CO2分子周围有________个与之紧邻且等距的CO2分子。
(2)由金刚石晶胞可知,每个金刚石晶胞占有________个碳原子。
(3)石墨层状结构中,平均每个正六边形占有的碳原子数是________。
(4)在CaF2晶体中,Ca2+的配位数是________,F-的配位数是________。
(5)固态时,C60属于________ (填“共价”或“分子”)晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W 均为常见的短周期主族元素,常温下,其最高价氧化物对应的水化物溶液(浓度均为0.01mol/L)的pH 和原子半径的关系如图所示,其中Y为碳元素。下列说法正确的是
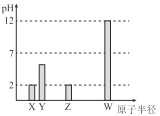
A.X是硫元素
B.Y的最高价氧化物的电子式为![]()
C.W 的最高价氧化物对应的水化物中仅含离子键
D.Z的最高价氧化物对应水化物的化学式为HZO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中是A、B、C、D、E五种短周期元素的某些性质,下列判断正确的是( )

A. C、D、E的氢化物的稳定性:C>D>E
B. 元素A的原子最外层轨道中无自旋状态相同的电子
C. 元素B、C之间不可能形成化合物
D. 与元素B同周期且第一电离能最小的元素的单质能与H2O发生置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的化工原料,工业上利用CO2和H2在一定条件下反应合成甲醇。
(1)已知:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1275.6kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH=-566.0 kJ·mol-1
③H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式_______________________。
(2)在容积为1L的密闭容器中,投入1molCO和2molH2,在不同条件下发生反应:CO(g)+2H2(g) ![]() CH3OH(g)。实验测得平衡时甲醇的物质的量随温度、压强变化如图1所示:
CH3OH(g)。实验测得平衡时甲醇的物质的量随温度、压强变化如图1所示:
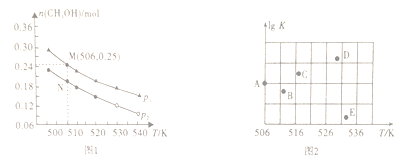
①该反应的△H_____0(填“>”、“<”或“=”),判断理由是_______________。
②M点时,CO的转化率为________。506K时该反应的平衡常数K=________(保留三位小数)。
③某同学绘制的压强为p时,不同温度下上述反应的平衡常数的对数值(lgK)如图2所示。A、B、C、D、E五点中能正确表示该反应的lgK与温度(T)的关系的点为____________。
④下列叙述能说明反应CO(g)+2H2(g) ![]() CH3OH(g)达到平衡状态的是________(填序号)。
CH3OH(g)达到平衡状态的是________(填序号)。
A.单位时间内生成2molH2的同时消耗1molCO
B.反应过程中c(CO):c(CH3OH)=1:1
C.恒温恒容时,混合气体的密度保持不变
D.绝热恒容时,反应的平衡常数不再变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com