
【题目】从500mL1mol·L-1的CuSO4溶液中取出100mL,下列关于100mL溶液的叙述错误的是()
A.CuSO4的物质的量浓度为1mol·L-1
B.SO42-的物质的量浓度为1mol·L-1
C.含Cu2+的物质的量为0.1mol
D.含CuSO4的质量为80.0g
 作业辅导系列答案
作业辅导系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,A、B、C的起始浓度分别是0.5mol/L、0.1 mol/L、1.6mol/L,可逆反应A(g)+B(g)![]() 2C(g)达到平衡时,下列数据合理的是
2C(g)达到平衡时,下列数据合理的是
A. c(A)=1.0mol/L c(B)=0.2mol/L B. c(B)=0.5mol/L c(C)=1.2mol/L
C. c(A)=0.4mol/L c(C)=1.8mol/L D. c(A )=0.9mol/L c(B)=0.5mo/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识,完成下列问题。
(1)用系统命名法给下列有机物命名:
①![]() _________________;②
_________________;②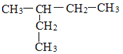 _______________。
_______________。
(2)写出下列有机物的结构简式:
①苯_____________;②丙三醇______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述不正确的是![]()
选项 | 已知 | 解释与结论 |
A | 活泼金属Al、不活泼金属Cu和浓硝酸可以形成原电池 | Al作正极,Cu作负极 |
B |
该反应在常温下能自发进行 | 该反应的 |
C | 常温下,
| 向 |
D | 向 | 氧化性: |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下实验测量mg铜银合金样品中铜的质量分数:

下列说法不正确的是![]()
A.收集到的VL气体都是NO
B.过滤用到的玻璃仪器是:烧杯、漏斗、玻璃棒
C.操作Ⅱ应是洗涤
D.根据题中已知条件不能求出合金中铜的质量分数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.利用甲烷催化还原NOx消除氮氧化物的污染
①CH4(g)+4NO2(g)![]() 4NO(g)+CO2(g)+2H2O(g) ΔH1=-574kJ·mol-1
4NO(g)+CO2(g)+2H2O(g) ΔH1=-574kJ·mol-1
②CH4(g)+4NO(g)![]() 2N2(g)+CO2(g)+2H2O(g) ΔH2=-1 160kJ·mol-1
2N2(g)+CO2(g)+2H2O(g) ΔH2=-1 160kJ·mol-1
③CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) ΔH3=-867kJ·mol-1
N2(g)+CO2(g)+2H2O(g) ΔH3=-867kJ·mol-1
(1)如果三个反应的平衡常数依次为K1、K2、K3,则K3=___(用K1、K2表示)。
(2)在2L恒容密闭容器中充入1molCH4和2molNO2进行反应③,CH4的平衡转化率α(CH4)与温度和压强的关系如图所示。
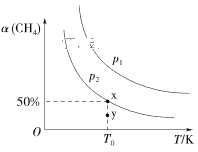
①若容器中的压强为p2,y点:v正____(填“大于”“等于”或“小于”)v逆。
②x点对应温度下反应的平衡常数K=___。
Ⅱ.甲烷蒸气转化法制H2的主要反应为:CH4(g)+H2O(g)![]() CO(g)+3H2(g)
CO(g)+3H2(g)
(3)在恒容密闭容器中充入2 mol CH4和H2O(g)的混合气体,且CH4和H2O(g)的物质的量之比为x,相同温度下达到平衡时测得H2的体积分数φ(H2)与x的关系如图所示。
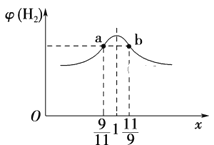
则CH4的转化率:a点____(填“>”“=”或“<”,下同)b点,CH4(g)的浓度:a点_____b点,氢气的产率:a点____b点。
Ⅲ.(4)根据以下三个热化学方程式:2H2S(g)+3O2(g)=SO2(g) +2H2O(l) ΔH=-Q1kJ·mol-1,2H2S(g)+O2(g)= S(s)+2H2O(l) ΔH=-Q2kJ·mol-1,2H2S(g)+O2(g)= S(s)+2H2O(g) ΔH=-Q3kJ·mol-1,判断Q1、Q2、Q3的大小关系是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将![]() 加入1L
加入1L![]() 溶液中,充分搅拌
溶液中,充分搅拌![]() 不考虑液体体积变化
不考虑液体体积变化![]() ,已知:
,已知:![]() ;
;![]() ,下列有关说法正确的是
,下列有关说法正确的是
A.相同温度下,AgCl的溶解性比![]() 弱
弱
B.沉淀转化反应![]() 的平衡常数为
的平衡常数为![]()
C.混合后溶液中的:![]()
![]()
![]()
![]()
D.混合后溶液中的:![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关甲、乙、丙、丁四个图示的叙述正确的是( )
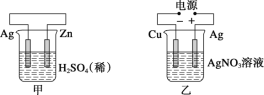
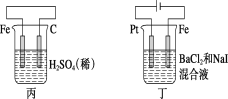
A.甲中负极反应式为2H++2e-=H2↑
B.乙中阳极反应式为Ag++e-=Ag
C.丙中H+向碳棒方向移动
D.丁中电解开始时阳极产生黄绿色气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.标准状况下,22.4 LSO2和SO3混合物中含有的硫原子数目为0.1NA
B.氢氧燃料电池负极消耗1.12L气体时,电路中转移的电子数为0.1NA
C.1mol NaHSO4在熔融状态下电离出的阳离子数为0.2NA
D.在1L 0.5mol/L的Na2CO3溶液中,阴离子总数大于0.5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com