
【题目】砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式_________________________。
(2)根据元素周期律,原子半径Ga________As,第一电离能Ga________As。(填“>”或“<”)
(3)AsCl3分子的立体构型为______________,其中As的杂化轨道类型为__________。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是_____________________。
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________,Ga与As以________键键合。Ga和As的摩尔质量分别为MGag·mol-1和MAsg·mol-1,原子半径分别为rGapm和rAspm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为_____________。(已知:晶胞内As原子之间彼此不相切)

【答案】 1s22s22p63s23p63d104s24p3 > < 三角锥形 sp3 GaF3为离子晶体,GaCl3为分子晶体,离子晶体的熔点高 原子晶体 共价键 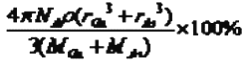
【解析】试题分析: (1)As为ⅤA族33号元素,电子排布式为:1s22s22p63s23p63d104s24p3;
(2)同一周期,原子序数越小半径越大,同周期第一电离能从左到右,逐渐增大;
(3)AsCl3中价层电子对个数=σ键个数+孤电子对个数=3+1 =4,所以原子杂化方式是sp3,由于有一对孤对电子对,分子空间构型为三角锥形;
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是GaF3为离子晶体,GaCl3为分子晶体,离子晶体的熔点高;
(5)GaAs的熔点为1238℃,熔点较高,以共价键结合形成属于原子晶体,密度为ρ g![]() cm﹣3,根据均摊法计算,As:
cm﹣3,根据均摊法计算,As: ![]() ,Ga:4×1=4,rGapm和rAspm,故其晶胞中原子所占的体积V1=
,Ga:4×1=4,rGapm和rAspm,故其晶胞中原子所占的体积V1=![]() ×10﹣30,1个晶胞的体积V2=
×10﹣30,1个晶胞的体积V2= ![]() ,将V1、V2带入计算 GaAs晶胞中原子的体积占晶胞体积的百分率。
,将V1、V2带入计算 GaAs晶胞中原子的体积占晶胞体积的百分率。
解析:根据以上分析,(1)As为ⅤA族33号元素,电子排布式为:1s22s22p63s23p63d104s24p3;
(2)根据元素周期律,Ga与As位于同一周期,Ga原子序数小于As,故半径Ga大于As,同周期第一电离能从左到右,逐渐增大,故第一电离能Ga小于As;
(3)AsCl3中价层电子对个数=σ键个数+孤电子对个数=3+1 =4,所以原子杂化方式是sp3,由于有一对孤对电子对,分子空间构型为三角锥形;
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是GaF3为离子晶体,GaCl3为分子晶体,离子晶体的熔点高;
(5)GaAs的熔点为1238℃,熔点较高,以共价键结合形成属于原子晶体,密度为ρ gcm﹣3,根据均摊法计算,As: ![]() ,Ga:4×1=4,故其晶胞中原子所占的体积V1=
,Ga:4×1=4,故其晶胞中原子所占的体积V1=![]() ×10﹣30,晶胞的体积V2=
×10﹣30,晶胞的体积V2= ![]() ,故GaAs晶胞中原子的体积占晶胞体积的百分率为 将V1、V2带入计算得百分率=
,故GaAs晶胞中原子的体积占晶胞体积的百分率为 将V1、V2带入计算得百分率= 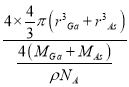 ×100%=
×100%=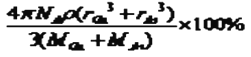 。
。


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】25℃时,向V mL pH=a的盐酸中,滴加10V mL pH=b的NaOH溶液,所得溶液中Cl-的物质的量恰好等于Na+的物质的量,则a+b的值是
A. 15 B. 14 C. 13 D. 不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.10mol/L的盐酸分别滴定20.00mL浓度均为0.10mol/L氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积的变化关系如图所示。下列说法不正确的是

A. 当滴定氨水消耗V(HCl)=10 mL时,有:2[c(OH-)-c(H+)]=c(NH4+)-c(NH3·H2O)
B. 当pH=7时,滴定氨水消耗的V(HCl)<20 mL,且溶液中c(NH4+)=c(Cl-)
C. 当滴定氨水消耗V(HCl)=20 mL时,有:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
D. 滴定氢氧化钠溶液,V(HCl)>20 mL时一定有:c(Cl-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】核电荷数由小到大顺序排列的五种短周期元素X、Y、Z、W、Q,其中在同周期中,Z的金属性最强,Q的非金属性最强;W的单质是淡黄色固体;X、Y、W在周期表中的相对位置关系如图所示
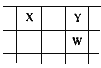
(1)五种元素形成的单质,其中固态时属于原子晶体的是________(填化学式);常用作强氧化剂的是________、________(填化学式)。
(2)这五种元素中,原子半径最大的是________(填化学式);由Z、W、Q形成的简单离子半径由大到小的顺序是________(用化学式表示);X、W、Q的最高价氧化物的水化物酸性从强到弱的顺序是________(用化学式表示)。
(3)Y和Z形成的一种化合物中含有离子键和共价键,请用电子书表示该化合物中化学键的形成过程___________________________________。
(4)Z与Q反应生成的化合物属于________化合物;电解该化合物的饱和溶液,阳极的电极反应式为________;电解一段时间后,将阳极产物和阴极溶液混合,反应的化学方程式是______________。
(5)由X、Y和氢三种元素组成的化合物X6H12Y6,已知:9 g该化合物燃烧放出140 kJ的热,写出该化合物燃烧热的热化学方程式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种将燃料电池与电解池组合制备KMnO4的装置如图所示(电极甲、乙、丙、丁均为惰性电极)。该装置工作时,下列说法不正确的是

A. 乙电极附近溶液的pH减小
B. 电极丁的反应式为:MnO42―― e- === MnO4-
C. KOH溶液的质量分数:c%>a%>b%
D. 导线中有2 mol电子通过时,理论上有2 mol K+移入阴极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色的酸性溶液中,下列离子组能大量共存的是( )
A.Ba2+、K+、Cl-、NO3-
B.Fe3+、Na+、Cl-、S2-
C.Al3+、Na+、CO32-、NO3-
D.Fe2+、Mg2+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
A. 0.1 mol CH4分子所含质子数为1.6 NA
B. 在0℃,101kPa时,22.4 L H2中含有NA个氢原子
C. 16 g氧气和16 g臭氧所含的原子数均为NA
D. NA个CO分子和11.2L CH4的质量比为7:4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com