
【题目】25℃时,进行下图所示滴定并得到对应曲线。下列说法错误的是( )
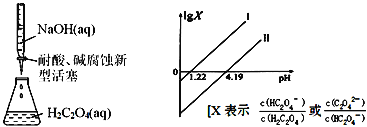
A.Ka2(H2C2O4)=10-4.19
B.直线Ⅰ中X=![]()
C.在NaHC2O4溶液中c(H2C2O4)+c(H+)=c(OH-)+c(C2O42-)
D.Ⅰ、Ⅱ两条直线的斜率均为1
【答案】B
【解析】
H2C2O4溶液中滴入NaOH溶液,先发生反应:H2C2O4+OH-=HC2O4-+H2O,随着碱的不断滴入,溶液的pH不断增大;当H2C2O4完全反应后,HC2O4-与NaOH发生反应HC2O4-+OH-=C2O42-+H2O,所以直线Ⅰ为X=![]() ,直线Ⅱ为X=
,直线Ⅱ为X=![]() 。
。
A. 在pH=4.19点,Ka2(H2C2O4)=![]() =10-4.19,A正确;
=10-4.19,A正确;
B. 由以上分析可知,直线Ⅱ中X=![]() ,B错误;
,B错误;
C. 在NaHC2O4溶液中,HC2O4-![]() C2O42-+H+,HC2O4-+H2O
C2O42-+H+,HC2O4-+H2O![]() H2C2O4+OH-,H2O
H2C2O4+OH-,H2O![]() H++OH-
H++OH-
由水电离出的c(OH-)=c(H+),则溶液中c(H+)-c(C2O42-)=c(OH-)-c(H2C2O4),从而得出c(H2C2O4)+c(H+)=c(OH-)+c(C2O42-),C正确;
D. 直线Ⅰ,lg X=0时,pH=1.22,pH=0时,lg X=1.22(由平衡常数进行计算),从而得出其斜率为1;采用同样的方法,可求出直线Ⅱ的斜率为1,D正确;
故选B。


科目:高中化学 来源: 题型:
【题目】现有以下几种有机物:
①![]() ②
②![]() ③
③ ④
④![]() ⑤
⑤![]()
⑥![]() ⑦
⑦ ⑧
⑧![]() ⑨
⑨![]()
请利用上述给出的物质按要求回答下列问题:
(1)③的系统命名是________。
(2)用“>”表示①③④⑧熔沸点高低顺序:________(填序号)。
(3)与③互为同系物的是________(填序号)。
(4)⑨的一氯代物同分异构体数目有________种。
(5)在120℃,![]() 条件下,某种气态烃与足量的
条件下,某种气态烃与足量的![]() 完全反应后,测得反应前后气体的体积没有发生改变,则该烃是________(填序号)。
完全反应后,测得反应前后气体的体积没有发生改变,则该烃是________(填序号)。
(6)写出⑥在铁作催化剂的条件下与液溴发生取代反应的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将3molA和1molB两种气体混合于固定容积2L的密闭容器中,发生如下反应:3A(g)+B(g)xC(g)+2D(g)。经2min该反应达到平衡状态,生成0.8molD,测得C的浓度为0.8mol/L。则下列判断错误的是
A.x=4
B.2min内B的反应速率为0.1mol·L-1·min-1
C.B的转化率为40%
D.该温度下平衡常数的值为1.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中属于加成反应的是
A.2CH3COOH+Na2CO3![]() 2CH3COONa+H2O+CO2↑
2CH3COONa+H2O+CO2↑
B.2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
C.CH3-CH=CH2+Br2![]() CH3-CHBr-CH2Br
CH3-CHBr-CH2Br
D.![]() +Br2
+Br2![]()
![]() +HBr
+HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用 0.1000mol/L NaOH溶液滴定 20.00mL0.1000mol/L某一元酸HA溶液,滴定曲线如图。下列说法正确的是
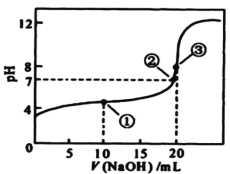
A.该滴定过程既能用甲基橙又能用酚酞作指示剂
B.点①所示溶液中:c(A-) >c(Na+)>c(H+) >c(OH-)
C.点②所示溶液中:c(Na+) =c(HA) +c(A-)
D.水的电离程度随着NaOH溶液的滴入不断增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3在现代工业生产中应用广泛。某化学研究性学习小组模拟工业生产流程制备无水FeCl3,实验装置如下图所示:
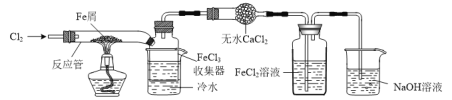
已知:无水FeCl3在空气中易潮解,加热易升华。
⑴通入Cl2和加热反应管这两步操作的先后顺序是_____,原因是______。
⑵实验后生成的FeCl3大部分进入收集器,少量沉积在反应管的右端。要使沉积得FeCl3进入收集器,可以进行的操作是________。
⑶洗气瓶中的FeCl2溶液用于吸收未反应的Cl2。向反应后的洗气瓶中滴加KSCN溶液,结果看到溶液先变红后褪色,溶液褪色的可能原因是_______。
⑷洗气瓶中生成的FeCl3溶液可用于吸收H2S气体生成S。写出吸收H2S气体的离子反应方程式:_______。为检测反应后溶液中是否存在Fe2+,甲同学提出可用酸性KMnO4溶液,乙同学提出酸性KMnO4溶液褪色不能证明存在Fe2+,理由是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素R、W、X、Y、Z的原子序数依次增大,R的简单氢化物可用作制冷剂,X是短周期中金属性最强的元素。Y的简单离子在同周期元素的简单离子中半径最小,由W、X和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀(Z的单质)析出,同时产生有刺激性气味的气体(Z的氧化物)。下列说法正确的是( )
A. 原子半径:Z>Y>X>W
B. Z的简单氢化物的热稳定性比W的强
C. Y的氧化物既可溶于R的最高价氧化物对应的水化物水溶液,也可溶于R的氢化物水溶液
D. X与W、Z形成的化合物不少于三种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M是一种医用高分子材料,可用于制造隐形眼镜;以下是M、有机玻璃的原料H及合成橡胶(N)的合成路线。
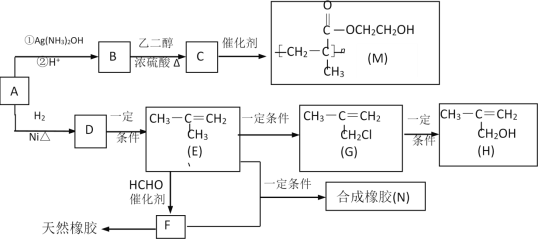
(1)A中含有的官能团是___(写名称)。
(2)写出反应类型:D→E___;写出反应条件:G→H___。
(3)写出B→C化学反应方程式:___;
(4)写出E+F→N化学反应方程式:___。
(5)H在一定条件下能被氧化为不饱和酸![]() ,该不饱和酸有多种同分异构体,属于酯类且含有碳碳双键的同分异构体共有___种。
,该不饱和酸有多种同分异构体,属于酯类且含有碳碳双键的同分异构体共有___种。
(6)已知:①RCHO![]()
![]()
②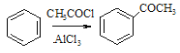
③![]() +SOCl2
+SOCl2![]() +SO2+HCl
+SO2+HCl
根据已有知识并结合相关信息,写出以 为原料制备
为原料制备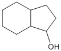 的合成路线流程图(无机试剂任用)___。合成路线流程图示例如下:H2C=CH2
的合成路线流程图(无机试剂任用)___。合成路线流程图示例如下:H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH。
CH3CH2OH。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]滴定法测定铬铁矿中铬含量的过程如下:
酸溶:准确称取0.1950 g铬铁矿试样放入锥形瓶中,加入适量磷酸和硫酸的混合酸,加热使试样完全溶解,冷却。
氧化:向上述溶液中滴加5滴1%的MnSO4溶液,再加入一定量的过硫酸铵[(NH4)2S2O8]溶液,摇匀,加热煮沸至出现紫红色,继续加热煮沸至紫红色褪去,冷却。[已知:①2Mn2+ + 5S2O82- + 8H2O = 10SO42- + 2MnO4- + 16H+;②继续加热煮沸后,溶液中过量(NH4)2S2O8和生成的HMnO4已分解除去]
滴定:用0.2050mol·L-1(NH4)2Fe(SO4)2标准溶液滴定上述溶液至终点,消耗19.50 mL标准溶液。(已知:Cr2O72-![]() Cr3+)
Cr3+)
(1)过硫酸铵保存在棕色试剂瓶中的原因是___________。
(2)①“氧化”的目的是将试样溶液中的Cr3+氧化成Cr2O72-,加入5滴MnSO4溶液的目的是________________(已知该条件下还原性:Cr3+ > Mn2+)。
②“氧化”过程中,如果继续加热煮沸时间不充足,会使铬含量的测定结果______(填“偏大”“不变”或“偏小”)。
(3)计算铬铁矿中铬的质量分数(写出计算过程)。___________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com