
����Ŀ��������M��һ��ҽ�ø߷��Ӳ��ϣ����������������۾���������M���л�������ԭ��H���ϳ���N���ĺϳ�·�ߡ�
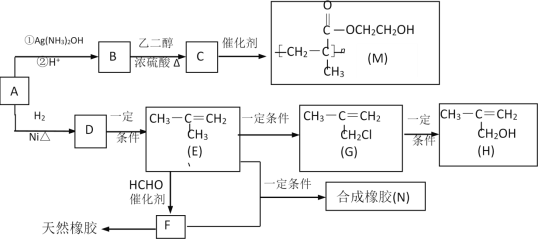
��1��A�к��еĹ�������___��д���ƣ���
��2��д����Ӧ���ͣ�D��E___��д����Ӧ������G��H___��
��3��д��B��C��ѧ��Ӧ����ʽ��___��
��4��д��E+F��N��ѧ��Ӧ����ʽ��___��
��5��H��һ���������ܱ�����Ϊ��������![]() ���ò��������ж���ͬ���칹�壬���������Һ���̼̼˫����ͬ���칹�干��___�֡�
���ò��������ж���ͬ���칹�壬���������Һ���̼̼˫����ͬ���칹�干��___�֡�
��6����֪����RCHO![]()
![]()
��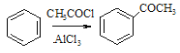
��![]() +SOCl2
+SOCl2![]() +SO2+HCl
+SO2+HCl
��������֪ʶ����������Ϣ��д���� Ϊԭ���Ʊ�
Ϊԭ���Ʊ�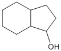 �ĺϳ�·������ͼ(���Լ�����)___���ϳ�·������ͼʾ�����£�H2C=CH2
�ĺϳ�·������ͼ(���Լ�����)___���ϳ�·������ͼʾ�����£�H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH��
CH3CH2OH��
���𰸡�ȩ����̼̼˫�� ������Ӧ ����������Һ������ ![]() +HOCH2CH2OH
+HOCH2CH2OH![]()
![]() +H2O
+H2O ![]() 5��
5�� 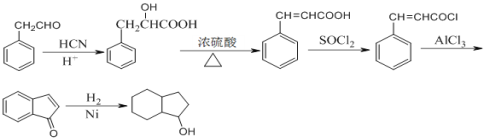
��������
����M�Ľṹ��ʽ��֪CΪ��![]() ��B���Ҷ�����Ӧ����C����B�Ľṹ��ʽΪ��
��B���Ҷ�����Ӧ����C����B�Ľṹ��ʽΪ��![]() ��Aͨ����������Ӧ������H+��Ӧ����B����A�Ľṹ��ʽΪ��
��Aͨ����������Ӧ������H+��Ӧ����B����A�Ľṹ��ʽΪ��![]() ��A�����������ӳɷ�Ӧ����D��A��̼̼˫����̼��˫�����ܹ������������ӳɷ�Ӧ������Dһ���������ܹ�����E��֪��DΪ
��A�����������ӳɷ�Ӧ����D��A��̼̼˫����̼��˫�����ܹ������������ӳɷ�Ӧ������Dһ���������ܹ�����E��֪��DΪ![]() ����F�ܹ�������Ȼ����F�Ľṹ��ʽΪ��
����F�ܹ�������Ȼ����F�Ľṹ��ʽΪ��![]() �����ݼӾ۷�Ӧԭ������д��E��F��Ӧ�ϳ�N�Ļ�ѧ����ʽΪ��
�����ݼӾ۷�Ӧԭ������д��E��F��Ӧ�ϳ�N�Ļ�ѧ����ʽΪ��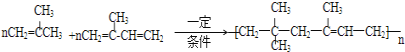 ��
��
��1�����ݷ�����֪AΪ![]() ���ʴ�Ϊ��ȩ����̼̼˫����
���ʴ�Ϊ��ȩ����̼̼˫����
��2��DΪ![]() ��Dͨ����ȥ��Ӧ����E��G��Hλ�ȴ�������ȥ��Ӧ����Ӧ����Ϊ�ʴ�Ϊ����������Һ�����ȣ���ȥ��Ӧ���Ӿ۷�Ӧ������������Һ�����ȣ�
��Dͨ����ȥ��Ӧ����E��G��Hλ�ȴ�������ȥ��Ӧ����Ӧ����Ϊ�ʴ�Ϊ����������Һ�����ȣ���ȥ��Ӧ���Ӿ۷�Ӧ������������Һ�����ȣ�
��3��BΪ![]() ��B���Ҷ�����Ӧ�Ļ�ѧ����ʽΪ��
��B���Ҷ�����Ӧ�Ļ�ѧ����ʽΪ��![]() ��
��
��4��E��F![]() ��Ӧ�Ļ�ѧ����ʽΪ��
��Ӧ�Ļ�ѧ����ʽΪ��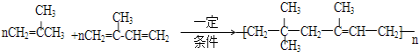 ��
��
��5��H��һ���������ܱ�����Ϊ��������![]() ���ò��������ж���ͬ���칹�壬���������Һ���̼̼˫����ͬ���칹��Ľṹ��ʽ�У�HCOOC��CH3��=CH2��HCOOCH2-CH=CH2��HCOOCH=CH-CH3��CH3COOCH=CH2��CH2=CH-COOCH3����5�֣��ʴ�Ϊ��5��
���ò��������ж���ͬ���칹�壬���������Һ���̼̼˫����ͬ���칹��Ľṹ��ʽ�У�HCOOC��CH3��=CH2��HCOOCH2-CH=CH2��HCOOCH=CH-CH3��CH3COOCH=CH2��CH2=CH-COOCH3����5�֣��ʴ�Ϊ��5��
��6����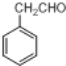 Ϊԭ���Ʊ�
Ϊԭ���Ʊ�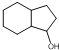 ��������и����ʵ�ת��������֪����������
��������и����ʵ�ת��������֪����������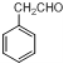 ��HCN�����ӳɷ�Ӧ����
��HCN�����ӳɷ�Ӧ����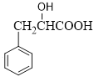 ��
��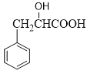 ������ȥ��Ӧ����
������ȥ��Ӧ����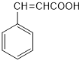 ��
�� ��SOCl2����ȡ����Ӧ����
��SOCl2����ȡ����Ӧ����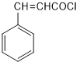 ��
��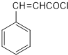 ��������ȥ�Ȼ����
��������ȥ�Ȼ����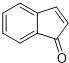 ��
�� �������ӳɵ�
�������ӳɵ�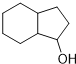 ���ϳ�·��Ϊ
���ϳ�·��Ϊ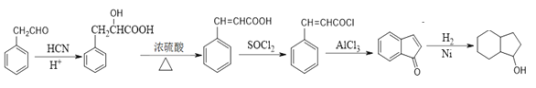 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�����ȿ���CO��CO2��Ӧ�öԹ�����̬������������Ҫ�����塣
(1)��֪7gCO��ȫȼ�շ���70.7kJ��д��COȼ�շ�Ӧ���Ȼ�ѧ����ʽ_________��
(2)CO��O2��Ƴ�ȼ�ϵ�أ���KOH��ҺΪ���Һ�����õ�صĸ�����ӦʽΪ_______���øõ�ص�⾫��ͭ����ͭ��ͨ��______һ��������CO������O2����������
(3)���ù��ܺ�������ɽ�CO2��H2O(g)ת��ΪCH4��O2�����������ʱ���ڲ�ͬ������I��II��III�������£�CH4���������ʱ��ı仯����ͼ����0��15Сʱ�ڣ�CH4��ƽ����������I��II��III��С�����˳��Ϊ___________������ţ���

(4)��TiO2��Cu2Al2O4Ϊ���������Խ�CO2��CH4ֱ��ת�������ᡣ�ڲ�ͬ�¶��´����Ĵ�Ч����������������ʵĹ�ϵ����ͼ��
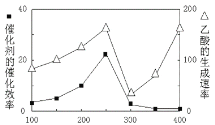
�ٵ��¶���________��Χʱ���¶��������������ʵ���ҪӰ�����ء�
��Cu2Al2O4������ϡ���ᣬϡ���ỹԭ����ΪNO��ͬʱ���������Σ�д���йص����ӷ���ʽ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��������ͼ��ʾ�ζ����õ���Ӧ���ߡ�����˵���������( )
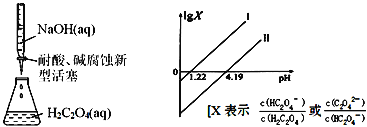
A.Ka2(H2C2O4)=10-4.19
B.ֱ�ߢ���X=![]()
C.��NaHC2O4��Һ��c(H2C2O4)+c(H+)=c(OH-)+c(C2O42-)
D.������ֱ�ߵ�б�ʾ�Ϊ1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Be��OH��2�����Եģ���ǿ�ᷴӦʱ����Be2+����ǿ�Ӧʱ����BeO22�����������ݵ����ʵ���Ũ�ȡ��������BeCl2��MgCl2��AlCl3��Һ������ʱ�������������ᣩ���ֽ�һ��Ũ�ȵ�NaOH��Һ�ֱ����������Һ����������NaOH��Һ�����x��mL�������ɳ��������ʵ���y��mol���Ĺ�ϵ��ͼ��ʾ������BeCl2��MgCl2��AlCl3������Һ��Ӧ��ͼ����ȷ���ǣ�������

A. �ݢۢ� B. �ڢۢ� C. �ۢݢ� D. �ۢڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Na2S�ֳƳ�����Ӧ�ù㷺�Ļ���ԭ�ϣ�Ҳ���������չ�ҵ�����е�SO2�����������գ�
��1�������ӷ���ʽ˵��Na2S�ֳƳ�����ԭ��___��
��2����AgCl����Һ�еμ�Na2S��Һ�����ɺ�ɫ������д����Ӧ�����ӷ���ʽ___���������ѧϰ�����������ӷ�Ӧ���������ӻ�����Ӧ���еķ�����___��
��Na2S��Һ�в���ͨ��SO2��ֱ�����������ա���俴����Һ����ǣ�ֹͣ��Ӧ����Һ�к�����Ϊ��S2O32-��HSO3-��H2SO3��HS-��
��3����Ӧ�����У���Һ��pH��___����������С���������ɵij�����___��
��4�����ڷ�Ӧ��õ�����Һ����������Ũ�ȹ�ϵ��ȷ����___��
a��c(Na+)=c(S2O32-) +2c(HSO3-)+2c(H2SO3) + 2c(HS-)
b��c(Na+)+c(H+)=2c(S2O32-)+c(HSO3-) +c(HS-) +c(OH-)
c��c(Na+)=2c(HS-)
d��c(Na+)=2c(HS-)+2c(S2O32-)+c(HSO3-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.6mol KCl��0.4mol Cu(NO3)2��0.2molAgNO3һ������ˮ�����100mL�����Һ���ö��Ե缫���һ��ʱ�������һ������19.2g Cu����ʱ����һ���ϲ���������������״���£�Ϊ
A.3.96LB.4.48LC.5.6LD.6.72L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�NO2��SO2 ��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
��1��һ�������£���2molNO��2molO2���ں����ܱ������з������·�Ӧ��2NO(g)+O2(g)![]() 2NO2(g)�����и�����˵����Ӧ�ﵽƽ��״̬����_____________��
2NO2(g)�����и�����˵����Ӧ�ﵽƽ��״̬����_____________��
A.��ϵѹǿ���ֲ���
B.���������ɫ���ֲ���
C.NO��O2�����ʵ���֮�ȱ��ֲ���
D.ÿ����1 molO2ͬʱ����2 molNO
��2��CO�����ںϳɼ״���һ���¶��£������Ϊ2L���ܱ������м���CO��H2��������ӦCO(g)+2H2(g)![]() CH3OH(g)����ƽ����ø����Ũ�ȣ�
CH3OH(g)����ƽ����ø����Ũ�ȣ�
���� | CO | H2 | CH3OH |
Ũ�ȣ�mol/L�� | 0.9 | 1.0 | 0.6 |
�ش��������⣺
�ٻ�������ƽ����Է�������=_________________��
��ƽ�ⳣ��K=__________________��
�������������ѹ��Ϊ1L���������㣬Ԥ����ƽ����c(H2)��ȡֵ��Χ��__________��
��������������䣬�ٳ���0.6molCO��0.4molCH3OH����ʱv��______v�������������������=������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ȼҵ�У����ӽ���Ĥ����ⱥ��ʳ��ˮʾ��ͼ���£�����˵������ȷ���ǣ� ��
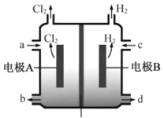
���ӽ���Ĥ
A.�缫AΪ����������������Ӧ��������
B.���ӽ���ĤΪ�����ӽ���Ĥ
C.����NaCl��a������NaOH��Һ��d����
D.OH-Ǩ�Ƶ��������ڵ�����ͨ�����ӵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NAΪ�����ӵ�������ֵ������˵��������ǣ� ��
A. 4.6g��NO2��N2O4��ɵĻ�������к��е�ԭ������Ϊ0.3NA
B. 0.2gD216O�к��е�������������������������Ϊ0.1NA
C. 6.2�˰����ӣ�P4���к�P��P��Ϊ0.05NA
D. ��������ϡ���ᷴӦʱ������0.1molNOת�Ƶĵ�����Ϊ0.3NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com