
【题目】Na2S又称臭碱、硫化碱,是应用广泛的化工原料,也常用于吸收工业废气中的SO2。完成下列填空:
(1)用离子方程式说明Na2S又称臭碱、硫化碱的原因___。
(2)向AgCl悬浊液中滴加Na2S溶液,生成黑色沉淀,写出反应的离子方程式___。结合你所学习过的其它离子反应分析,离子互换反应进行的方向是___。
向Na2S溶液中不断通入SO2,直至不再能吸收。其间看到溶液变浑浊,停止反应后溶液中含硫微粒为:S2O32-、HSO3-、H2SO3、HS-。
(3)反应过程中,溶液的pH逐渐___(填“变大”、“变小”),生成的沉淀是___;
(4)关于反应后得到的溶液,下列离子浓度关系正确的是___。
a.c(Na+)=c(S2O32-) +2c(HSO3-)+2c(H2SO3) + 2c(HS-)
b.c(Na+)+c(H+)=2c(S2O32-)+c(HSO3-) +c(HS-) +c(OH-)
c.c(Na+)=2c(HS-)
d.c(Na+)=2c(HS-)+2c(S2O32-)+c(HSO3-)
【答案】S2-+H2O![]() OH-+HS-,HS-+H2O
OH-+HS-,HS-+H2O![]() OH-+H2S 2AgCl+S2-=Ag2S+2Cl- 某些离子浓度减小的方向 变小 S b
OH-+H2S 2AgCl+S2-=Ag2S+2Cl- 某些离子浓度减小的方向 变小 S b
【解析】
(1)硫化钠是强碱弱酸盐,硫离子水解生成硫氢根离子和氢氧根离子,硫氢根离子水解生成具有臭味的硫化氢;
(2)Ag2S溶解度小于AgCl溶解度,溶解度大的物质能转化为溶解度小的物质;
(3)Na2S溶液中存在硫离子水解溶液显碱性,不断通入SO2, SO2溶于水显酸且SO2会与硫离子反应,硫离子水解程度远远大于硫氢根离子、亚硫酸氢根离子、硫代硫酸根离子;生成的沉淀是S;
(4)任何电解质溶液中都存在电荷守恒和物料守恒,根据电荷守恒和物料守恒判断。
:(1)硫化钠是强碱弱酸盐,硫离子水解生成硫氢根离子和氢氧根离子,硫氢根离子水解生成具有臭味的硫化氢, 故答案为:![]() 、
、![]() ;
;
(2)Ag2S溶解度小于AgCl溶解度,溶解度大的物质能转化为溶解度小的物质,离子方程式为![]() ,离子互换反应进行的方向是某些离子浓度减小的方向,故答案为:
,离子互换反应进行的方向是某些离子浓度减小的方向,故答案为:![]() ;某些离子浓度减小的方向;
;某些离子浓度减小的方向;
(3)Na2S溶液中存在硫离子水解溶液显碱性,不断通入SO2, SO2溶于水显酸且SO2会与硫离子反应,硫离子水解程度远远大于硫氢根离子、亚硫酸氢根离子、硫代硫酸根离子,所以溶液的pH变小;生成的沉淀是S,故答案为:变小;S;
(4)a.未通入SO2时,Na2S溶液中存在:c(Na+)=2c(S2-)+2c(HS-)+2c(H2S),通入SO2时后,融入SO2后会与水反应生成H2SO3,无法确定S原子和Na原子之间的数量关系,故a错误;
b.根据电荷守恒得c(Na+)+c(H+)=2c(S2O32-)+c(HSO3-)+c(HS-)+c(OH-),故b正确;
c.未通入SO2时,Na2S溶液中存在:c(Na+)=2c(S2-)+2c(HS-)+2c(H2S),c(Na+)>2c(HS-)通入SO2后-2价的硫元素会减小,所以c(Na+)>2c(HS-),故c错误;
d.若c(Na+)=2c(HS-)+2c(S2O32-)+c(HSO3-)再结合电荷守恒可得:c(H+)= c(OH-)- c(HS-)在未通入SO2时,Na2S溶液中存在质子守恒:c(H+)= c(OH-)- c(HS-)-2c(H2S),若在通入SO2时,只与该溶液中水解生成的H2S反应,则d正确,而实际上并非如此,故d错误。
故选b。


科目:高中化学 来源: 题型:
【题目】N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为________。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为
NO+NO2+2OH![]() 2
2![]() +H2O
+H2O
2NO2+2OH![]()
![]() +
+![]() +H2O
+H2O
①下列措施能提高尾气中NO和NO2去除率的有________(填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是________(填化学式);吸收后排放的尾气中含量较高的氮氧化物是________(填化学式)。
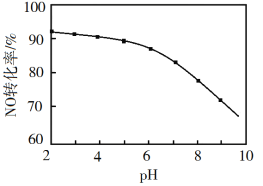
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为![]() 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
①在酸性NaClO溶液中,HClO氧化NO生成Cl和![]() ,其离子方程式为________。
,其离子方程式为________。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用 0.1000mol/L NaOH溶液滴定 20.00mL0.1000mol/L某一元酸HA溶液,滴定曲线如图。下列说法正确的是
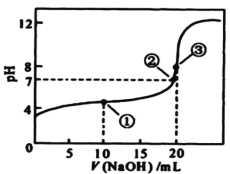
A.该滴定过程既能用甲基橙又能用酚酞作指示剂
B.点①所示溶液中:c(A-) >c(Na+)>c(H+) >c(OH-)
C.点②所示溶液中:c(Na+) =c(HA) +c(A-)
D.水的电离程度随着NaOH溶液的滴入不断增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素R、W、X、Y、Z的原子序数依次增大,R的简单氢化物可用作制冷剂,X是短周期中金属性最强的元素。Y的简单离子在同周期元素的简单离子中半径最小,由W、X和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀(Z的单质)析出,同时产生有刺激性气味的气体(Z的氧化物)。下列说法正确的是( )
A. 原子半径:Z>Y>X>W
B. Z的简单氢化物的热稳定性比W的强
C. Y的氧化物既可溶于R的最高价氧化物对应的水化物水溶液,也可溶于R的氢化物水溶液
D. X与W、Z形成的化合物不少于三种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘化锂(![]() )在能源、医药等领域有重要应用,某兴趣小组制备
)在能源、医药等领域有重要应用,某兴趣小组制备![]() 和
和![]() ,流程如下:
,流程如下:
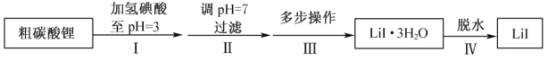
已知:![]() 在75~80℃转变成
在75~80℃转变成![]() ,80~120℃转变成
,80~120℃转变成![]() ,300℃以上转变成无水
,300℃以上转变成无水![]() 。
。
b.![]() 易溶于水,溶解度随温度升高而增大。
易溶于水,溶解度随温度升高而增大。
c.![]() 在空气中受热易被氧化。
在空气中受热易被氧化。
请回答:
(1)步骤II,调![]() ,为避免引入新的杂质,适宜加入的试剂为________。
,为避免引入新的杂质,适宜加入的试剂为________。
(2)步骤III,包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等多步操作。
下列说法正确的是________。
A.为得到较大的![]() 晶体颗粒,宜用冰水浴快速冷却结晶
晶体颗粒,宜用冰水浴快速冷却结晶
B.为加快过滤速度,得到较干燥的晶体,可进行抽滤
C.宜用热水洗涤
D.可在80℃鼓风干燥
(3)步骤IV,脱水方案为:将所得![]() 置入坩埚中,300℃加热,得
置入坩埚中,300℃加热,得![]() 样品。用沉淀滴定法分别测定所得
样品。用沉淀滴定法分别测定所得![]() 、
、![]() 样品纯度,测定过程如下:称取一定量样品,溶解,定容于容量瓶,将容量瓶中的溶液倒入烧杯,用移液管定量移取烧杯中的溶液加入锥形瓶,调
样品纯度,测定过程如下:称取一定量样品,溶解,定容于容量瓶,将容量瓶中的溶液倒入烧杯,用移液管定量移取烧杯中的溶液加入锥形瓶,调![]() ,用滴定管中的
,用滴定管中的![]() 标准溶液滴定至终点,根据消耗的
标准溶液滴定至终点,根据消耗的![]() 标准溶液体积计算,得
标准溶液体积计算,得![]() 、
、![]() 的纯度分别为99.96%,95.38%。
的纯度分别为99.96%,95.38%。![]() 纯度偏低。
纯度偏低。
①上述测定过程提及的下列仪器,在使用前一定不能润洗的是________。
A.容量瓶 B.烧杯 C.锥形瓶 D.滴定管
②测定过程中使用到移液管,选出其正确操作并按序列出字母:
蒸馏水洗涤→待转移溶液润洗→________→_______→_______→_______→洗净,放回管架。
a.移液管尖与锥形瓶内壁接触,边吹气边放液
b.放液完毕,停留数秒,取出移液管
c.移液管尖与锥形瓶内壁接触,松开食指放液设备
d.洗耳球吸溶液至移液管标线以上,食指堵住管口
e.放液完毕,抖动数下,取出移液管
f.放液至凹液面最低处与移液管标线相切,按紧管口
③![]() 纯度偏低,可能的主要杂质是________。
纯度偏低,可能的主要杂质是________。

(4)步骤IV,采用改进的实验方案(装置如图),可以提高![]() 纯度。
纯度。
①设备X的名称是________。
②请说明采用该方案可以提高![]() 纯度的理由________。
纯度的理由________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M是一种医用高分子材料,可用于制造隐形眼镜;以下是M、有机玻璃的原料H及合成橡胶(N)的合成路线。
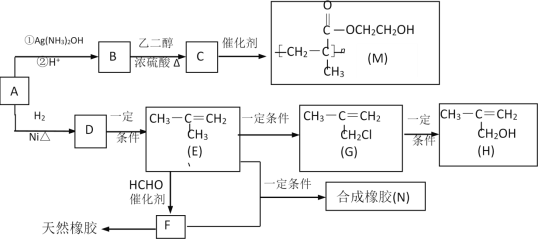
(1)A中含有的官能团是___(写名称)。
(2)写出反应类型:D→E___;写出反应条件:G→H___。
(3)写出B→C化学反应方程式:___;
(4)写出E+F→N化学反应方程式:___。
(5)H在一定条件下能被氧化为不饱和酸![]() ,该不饱和酸有多种同分异构体,属于酯类且含有碳碳双键的同分异构体共有___种。
,该不饱和酸有多种同分异构体,属于酯类且含有碳碳双键的同分异构体共有___种。
(6)已知:①RCHO![]()
![]()
②
③![]() +SOCl2
+SOCl2![]() +SO2+HCl
+SO2+HCl
根据已有知识并结合相关信息,写出以 为原料制备
为原料制备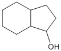 的合成路线流程图(无机试剂任用)___。合成路线流程图示例如下:H2C=CH2
的合成路线流程图(无机试剂任用)___。合成路线流程图示例如下:H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH。
CH3CH2OH。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究铜和浓硫酸的反应,下列装置或操作错误的是
甲 乙
乙  丙
丙
A.上下移动装置甲中的铜丝可控制SO2的生成
B.装置乙可用于收集SO2气体
C.为确认甲中有CuSO4生成,向甲中反应后的试管中直接加水稀释,观察溶液颜色
D.利用装置丙将硫酸铜溶液加热浓缩、冷却结晶,可析出CuSO4·5H2O晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的开关时,观察到电流表的指针发生了偏转。请根据如图所示,回答下列问题:
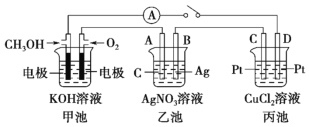
(1)甲池为_____(填“原电池”“电解池”或“电镀池”),通入 CH3OH 电极的电极反应为_____。
(2)乙池中 A(石墨)电极的名称为_____(填“正极”“负极”或“阴极”“阳极”),总反应化学方程式为__________。
(3)当乙池中 B 极质量增加 5.4 g 时,甲池中理论上消耗 O2 的体积为_____mL(标准状况),丙池中_____(填“C”或“D”)极析出_____g 铜。
(4)若丙中电极不变,将其溶液换成 NaCl 溶液,开关闭合一段时间后,甲中溶液的 pH将_____(填“增大”“减小”或“不变”,下同),丙中溶液的 pH 将______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明硅酸的酸性弱于碳酸酸性的实验事实是( )
A.CO2溶于水形成碳酸,SiO2难溶于水
B.CO2通入可溶性硅酸盐中析出硅酸沉淀
C.高温下SiO2与碳酸盐反应生成CO2
D.HCl通入可溶性碳酸盐溶液中放出气体,氯化氢通入可溶性硅酸盐溶液中生成沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com