
����Ŀ���о�NO2��SO2 ��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
��1��һ�������£���2molNO��2molO2���ں����ܱ������з������·�Ӧ��2NO(g)+O2(g)![]() 2NO2(g)�����и�����˵����Ӧ�ﵽƽ��״̬����_____________��
2NO2(g)�����и�����˵����Ӧ�ﵽƽ��״̬����_____________��
A.��ϵѹǿ���ֲ���
B.���������ɫ���ֲ���
C.NO��O2�����ʵ���֮�ȱ��ֲ���
D.ÿ����1 molO2ͬʱ����2 molNO
��2��CO�����ںϳɼ״���һ���¶��£������Ϊ2L���ܱ������м���CO��H2��������ӦCO(g)+2H2(g)![]() CH3OH(g)����ƽ����ø����Ũ�ȣ�
CH3OH(g)����ƽ����ø����Ũ�ȣ�
���� | CO | H2 | CH3OH |
Ũ�ȣ�mol/L�� | 0.9 | 1.0 | 0.6 |
�ش��������⣺
�ٻ�������ƽ����Է�������=_________________��
��ƽ�ⳣ��K=__________________��
�������������ѹ��Ϊ1L���������㣬Ԥ����ƽ����c(H2)��ȡֵ��Χ��__________��
��������������䣬�ٳ���0.6molCO��0.4molCH3OH����ʱv��______v�������������������=������
���𰸡�A��B��C��D 18.56 0.67 1mol/L��c(H2)��2mol/L =
��������
��1��A.�÷�Ӧ���ߵĻ�ѧ����������ȣ��ڷ�Ӧû�дﵽƽ��ʱ����������ʵ����ᷢ���ı䣬��ϵ��ѹǿҲҪ�ı䣬���ѹǿ����˵�����������������������ȣ���Ӧ�ﵽ��ƽ�⣬A����ȷ��
B.��Ӧ��NO2����ɫ���壬��ɫ����˵��NO2��Ũ�Ȳ��ٸı䣬��Ӧ�ﵽ��ƽ�⣬B����ȷ��
C.NO��O2����ʼ���ʵ�����ȣ�����ѧ��������ͬ���仯������ͬ�����û�дﵽƽ�⣬NO��O2�����ʵ���֮�Ȼᷢ���ı䣬�������ı�˵���ﵽ��ƽ�⣬C����ȷ��
D. ÿ����1 molO2ͬʱ����2 molNO�����淴Ӧ������ȣ�˵����Ӧ�ﵽ��ƽ�⣬D����ȷ��
��ѡABCD��
��2�����ɱ�������֪��CO��H2��CH3OH�����ʵ����ֱ���1.8mol��2mol��1.2mol�������ֱ�Ϊ1.8mol��28g/mol=50.4g��2mol��2g/mol=4g��1.2mol��32g/mol=38.4g�����������ƽ����Է�����������![]() =
=![]() =18.56g/mol�����ƽ����Է���������18.56��
=18.56g/mol�����ƽ����Է���������18.56��
��ƽ�ⳣ��K= ![]() =
=![]() ��0.67��
��0.67��
�������������ѹ��Ϊ1L����˲��H2��Ũ�ȱ�Ϊ2mol/L��ѹ������ʹ��ѹǿ����CO(g)+2H2(g)![]() CH3OH(g)�еĻ�ѧ������֪��ƽ�����ƣ�������Ũ�ȱ�С��������������ԭ��֪��ƽ��ʱ��������Ũ�ȷ�ΧΪ1mol/L��c(H2)��2mol/L��
CH3OH(g)�еĻ�ѧ������֪��ƽ�����ƣ�������Ũ�ȱ�С��������������ԭ��֪��ƽ��ʱ��������Ũ�ȷ�ΧΪ1mol/L��c(H2)��2mol/L��
�ܸ���������ݣ�����λmol/L��
CO | 2H2 | CH3OH | |
ԭƽ������Ũ�� | 0.9 | 1.0 | 0.6 |
�ٳ���Ũ�� | 0.3 | 0 | 0.2 |
���������Ũ�� | 1.2 | 1.0 | 0.8 |
Qc=![]() =
=![]() =0.67=K��˵����ʱ��ѧ��Ӧ�Դ�ƽ��״̬����v��=v����
=0.67=K��˵����ʱ��ѧ��Ӧ�Դ�ƽ��״̬����v��=v����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£���3molA��1molB�����������ڹ̶��ݻ�2L���ܱ������У��������·�Ӧ��3A(g)+B(g)xC(g)+2D(g)����2min�÷�Ӧ�ﵽƽ��״̬������0.8molD�����C��Ũ��Ϊ0.8mol/L���������жϴ������
A.x=4
B.2min��B�ķ�Ӧ����Ϊ0.1mol��L-1��min-1
C.B��ת����Ϊ40��
D.���¶���ƽ�ⳣ����ֵΪ1.2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��R��W��X��Y��Z��ԭ��������������R�ļ��⻯��������������X�Ƕ������н�������ǿ��Ԫ�ء�Y�ļ�������ͬ����Ԫ�صļ������а뾶��С����W��X��Z����Ԫ���γɵ�һ��������ˮ����ϡ���ᣬ�л�ɫ����(Z�ĵ���)������ͬʱ�����д̼�����ζ������(Z��������)������˵����ȷ����( )
A. ԭ�Ӱ뾶��Z>Y>X>W
B. Z�ļ��⻯������ȶ��Ա�W��ǿ
C. Y��������ȿ�����R������������Ӧ��ˮ����ˮ��Һ��Ҳ������R���⻯��ˮ��Һ
D. X��W��Z�γɵĻ����ﲻ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������M��һ��ҽ�ø߷��Ӳ��ϣ����������������۾���������M���л�������ԭ��H���ϳ���N���ĺϳ�·�ߡ�
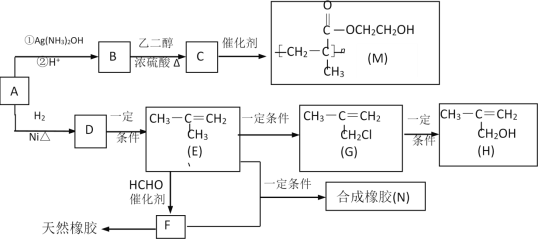
��1��A�к��еĹ�������___��д���ƣ���
��2��д����Ӧ���ͣ�D��E___��д����Ӧ������G��H___��
��3��д��B��C��ѧ��Ӧ����ʽ��___��
��4��д��E+F��N��ѧ��Ӧ����ʽ��___��
��5��H��һ���������ܱ�����Ϊ��������![]() ���ò��������ж���ͬ���칹�壬���������Һ���̼̼˫����ͬ���칹�干��___�֡�
���ò��������ж���ͬ���칹�壬���������Һ���̼̼˫����ͬ���칹�干��___�֡�
��6����֪����RCHO![]()
![]()
��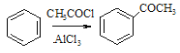
��![]() +SOCl2
+SOCl2![]() +SO2+HCl
+SO2+HCl
��������֪ʶ����������Ϣ��д���� Ϊԭ���Ʊ�
Ϊԭ���Ʊ�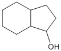 �ĺϳ�·������ͼ(���Լ�����)___���ϳ�·������ͼʾ�����£�H2C=CH2
�ĺϳ�·������ͼ(���Լ�����)___���ϳ�·������ͼʾ�����£�H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH��
CH3CH2OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̽��ͭ��Ũ����ķ�Ӧ������װ�û�����������
�� ��
��  ��
��
A.�����ƶ�װ�ü��е�ͭ˿�ɿ���SO2������
B.װ���ҿ������ռ�SO2����
C.Ϊȷ�ϼ�����CuSO4���ɣ�����з�Ӧ����Թ���ֱ�Ӽ�ˮϡ�ͣ��۲���Һ��ɫ
D.����װ�ñ�������ͭ��Һ����Ũ������ȴ�ᾧ��������CuSO4��5H2O����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���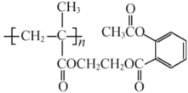 ��˵������ȷ���ǣ� ��
��˵������ȷ���ǣ� ��
A.�����ʿ���n���������ͨ�����۷�Ӧ����
B.![]() ��������ȫȼ�գ�����33.6 L����״������
��������ȫȼ�գ�����33.6 L����״������![]()
C.������������������ˮ�����֮һ���������������Ŀ�����
D.![]() ������������
������������![]() ��Һ��Ӧ����������
��Һ��Ӧ����������![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС���ͬѧ����ͼ��ʾװ���о��йص绯ѧ�����⡣���պϸ�װ�õĿ���ʱ���۲쵽��������ָ�뷢����ƫת���������ͼ��ʾ���ش��������⣺
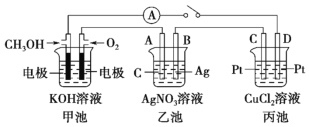
��1���׳�Ϊ_____(�ԭ��ء������ء���Ƴء�)��ͨ�� CH3OH �缫�ĵ缫��ӦΪ_____��
��2���ҳ��� A(ʯī)�缫������Ϊ_____(�������������������������������)���ܷ�Ӧ��ѧ����ʽΪ__________��
��3�����ҳ��� B ���������� 5.4 g ʱ���׳������������� O2 �����Ϊ_____mL(��״��)��������_____(�C����D��)������_____g ͭ��
��4�������е缫���䣬������Һ���� NaCl ��Һ�����رպ�һ��ʱ�������Һ�� pH��_____(�������С�����䡱����ͬ)��������Һ�� pH ��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���������������[(NH4)2Fe(SO4)2��6H2O]�ζ����ⶨ�������и������Ĺ������£�
����:ȷ��ȡ0.1950 g����������������ƿ�У������������������Ļ���ᣬ����ʹ������ȫ�ܽ⣬��ȴ��
����:��������Һ�еμ�5��1%��MnSO4��Һ���ټ���һ�����Ĺ������[(NH4)2S2O8]��Һ��ҡ�ȣ���������������Ϻ�ɫ����������������Ϻ�ɫ��ȥ����ȴ��[��֪����2Mn2+ + 5S2O82- + 8H2O = 10SO42- + 2MnO4- + 16H+��������������к���Һ�й���(NH4)2S2O8�����ɵ�HMnO4�ѷֽ��ȥ]
�ζ�:��0.2050mol��L-1(NH4)2Fe(SO4)2����Һ�ζ�������Һ���յ㣬����19.50 mL����Һ������֪��Cr2O72-![]() Cr3+��
Cr3+��
��1��������隣�������ɫ�Լ�ƿ�е�ԭ����___________��
��2���١���������Ŀ���ǽ�������Һ�е�Cr3+������Cr2O72-������5��MnSO4��Һ��Ŀ����________________����֪�������»�ԭ�ԣ�Cr3+ > Mn2+����
�ڡ������������У���������������ʱ�䲻���㣬��ʹ�������IJⶨ���______������ƫ����������������ƫС������
��3������������и�������������д��������̣���___________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��������Ϊ�����仯����֮����ת����

�Իش�
��1��д��D�Ļ�ѧʽ___��H�Ļ�ѧʽ___��
��2������G��Һ���Լ�Ϊ___��
��3��д����Eת���F�Ļ�ѧ����ʽ___��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com