
【题目】取一定质量NaHCO3和Na2O的固体混合物溶于适量的水,将所得溶液分成两等份,向其中一份水溶液中缓慢逐滴加入某物质的量浓度的盐酸,产生的气体体积与所加盐酸体积之间的关系如图所示;向另一份水溶液中加入过量Ba(OH)2溶液,得到白色沉淀39.4g。试回答下列问题:

(1)盐酸的物质的量浓度为___________;
(2)固体混合物中NaHCO3与Na2O物质的量之比_______。
【答案】1mol/L 4:1
【解析】
一定质量NaHCO3和Na2O的固体混合物溶于适量的水,发生反应Na2O+H2O=2NaOH、NaHCO3+NaOH=Na2CO3+H2O,将所得溶液分成两等份,向其中一份水溶液中缓慢逐滴加入某物质的量浓度的盐酸,由图象可知氢氧化钠不足,反应后溶液中的溶质是碳酸钠和碳酸氢钠;向另一份水溶液中加入过量Ba(OH)2溶液,得到白色沉淀为碳酸钡,根据原子守恒、反应的方程式结合图象数据来计算。
(1)一定质量NaHCO3和Na2O的固体混合物溶于适量的水,发生反应Na2O+H2O=2NaOH、NaHCO3+NaOH=Na2CO3+H2O,将所得溶液分成两等份,向其中一份水溶液中缓慢逐滴加入某物质的量浓度的盐酸,由图象可知氢氧化钠不足,反应后溶液中的溶质是碳酸钠和碳酸氢钠,先发生Na2CO3+HCl=NaHCO3+NaCl,后发生NaHCO3+HCl=CO2↑+NaCl+H2O。由于后一阶段消耗盐酸的体积是第一阶段消耗盐酸体积的2倍,所以碳酸钠和碳酸氢钠的物质的量相等;向另一份水溶液中加入过量Ba(OH)2溶液,得到白色沉淀39.4g,沉淀为碳酸钡,其物质的量为39.4g÷197g/mol=0.2mol,由碳元素守恒可知碳酸钠和碳酸氢钠均为0.1mol,这说明反应Na2CO3+HCl=NaHCO3+NaCl中消耗的盐酸为0.1mol,则HCl的物质的量浓度为0.1mol÷0.1L=1mol/L;
(2)由于生成的碳酸钠是0.1mol,根据反应Na2O+H2O=2NaOH、NaHCO3+NaOH=Na2CO3+H2O可知氧化钠是0.05mol,根据碳原子守恒可知碳酸氢钠的物质的量是0.2mol,所以固体混合物中NaHCO3与Na2O物质的量之比4:1。


科目:高中化学 来源: 题型:
【题目】有机物A只含有C、H、O三种元素,常用作有机合成的中间体。16.8 g该有机物燃烧生成44.0 g CO2和14.4 g H2O;质谱图表明其相对分子质量为84,红外光谱分析表明A分子中含有O—H键和位于分子端的C≡C键,核磁共振氢谱上有三个峰,峰面积之比为6∶1∶1。
(1)A的分子式是____________。
(2)下列物质中,一定条件下能与A发生反应的是_________________。
A.H2B.Na C.酸性KMnO4溶液 D.Br2
(3)A的结构简式是________________________。
(4)有机物B是A的同分异构体,1 mol B可与1 mol Br2加成。该有机物中所有碳原子在同一个平面上,没有顺反异构现象。B的结构简式是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验不合理的是
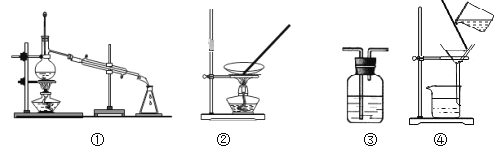
A. 用浓硫酸干燥SO2,选③
B. 从食盐溶液中获取NaCl,选②
C. 除去自来水中的Cl-,制纯净水,选④和①
D. 除去Fe(OH)3胶体中的难溶物,选④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素元素是非金属性很强的一类元素,能形成多种物质。
(1)氯气能氧化许多种还原剂,同时在适当条件下又可发生自身氧化还原反应。
①将足量的氯气通入到H2S溶液中,再向所得的溶液中加入用盐酸酸化的BaCl2溶液可得到白色沉淀,写出前一个反应的离子方程式:____________________________。
②将0.1molCl2缓慢通入到amL、浓度为2mol/L的KOH溶液中,二者恰好反应完,测得溶液c(ClO-)∶c(ClO3-)∶c(Cl-)=2∶1∶7,则a=______________。
(2)KClO3是一种重要的氧化剂,工业上制备KClO3的方法之一如下:
![]()
①写出电解时反应的化学方程式:_______________________________。
②相同温度下,两种氯酸盐的溶解度相对大小:NaClO3___________KClO3(填“>”或“<”)。
③KClO3在MnO2的催化作用下加热分解生成氧气的反应历程如下,请填写空白处:
2KClO3+2MnO2![]() 2KMnO4+Cl2↑+O2↑;
2KMnO4+Cl2↑+O2↑;
2KMnO4![]() K2MnO4+MnO2+O2↑,
K2MnO4+MnO2+O2↑,
K2MnO4+Cl2![]() O2↑+___________+___________。
O2↑+___________+___________。
反应结束后将固体混合物分离开的主要操作是__________________________。
(3)已知Cl2O是酸性氧化物,将Cl2O通入到水中可得到一种酸性溶液,请写出该溶液具有的除酸性外的一种化学性质______________。若将该气体通入到NaOH溶液中恰好完全反应,则溶液中各离子浓度由大到小的顺序为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某香料I的一种合成路线如下:

回答下列问题:
(1)C的名称为______________;H所含官能团名称是______________。
(2)B→C的反应类型是______________;写出I的结构简式:______________。
(3)G分子最多有______________个原子共平面。
(4)写出A→B的化学方程式:____________________________。
(5)J是I的同分异构体,同时满足下列条件的J的结构有_______种。其中,一种核磁共振氢谱有6个峰且峰的面积之比为1∶1∶1∶2∶2∶3的结构简式为______________。
①能使溴的四氯化碳溶液褪色
②能与碳酸氢钠溶液反应产生CO2
③属于芳香族化合物,且苯环上的一氯代物只有2种
(6)参照上述流程,以乙烯和OHC-CHO为原料合成HOOCCH=CHCOOH,设计合成路线:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型电池的开发与使用在现代社会中已很普遍,一种水煤气燃料电池的能量转化率可达90%以上。下列说法正确的是
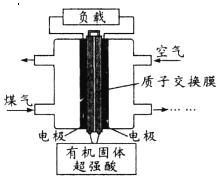
A. 总反应为2CO+O2==2CO2
B. 负极反应为H2-2e—==2H+、CO-2e—+H2O==CO2+2H+
C. 电路中通过4 mol电子,正极消耗22.4 L(标准状况)空气
D. 有机固体中的H+在放电时向正极移动,造成正极pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6.2 g有机物A与足量O2在密闭容器中充分燃烧,产物只有H2O和CO2,产物通过浓H2SO4后,质量增加5.4g,再通过碱石灰完全吸收,质量增加8.8g。用质谱法测得A的分子量为62;
(1)写出其分子式_____________________;
(2)若0.2mol的该有机物恰好与9.2g的金属钠完全反应,计算并推断出该有机物的结构简式____________。
(3)它在核磁共振氢谱中将会出现___________个信号.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)SiO2是玻璃的成分之一,SiO2与氢氧化钠溶液反应的化学方程式为______________________________,工艺师常用________(填物质名称)来雕刻玻璃。
(2)用Na2SiO3溶液浸泡过的棉花不易燃烧,体现Na2SiO3的用途可作________的原料。
(3)工业上常用2C+SiO2![]() Si+2CO↑制备硅单质,该反应中有元素化合价升高的物质是________(填化学式,下同),氧化剂是________。
Si+2CO↑制备硅单质,该反应中有元素化合价升高的物质是________(填化学式,下同),氧化剂是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是模拟电化学反应装置图。下列说法正确的是( )
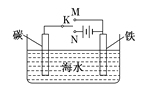
A. 开关K置于N处,则铁电极的电极反应式为:Fe-2e-=Fe2+
B. 开关K置于N处,可以减缓铁的腐蚀
C. 开关K置于M处,则铁电极的电极反应式为: 2Cl--2e-=Cl2↑
D. 开关K置于M处,电子从碳棒经开关K流向铁棒
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com