
【题目】(有机化学基础)胡椒乙酸是合成许多药用生物碱的重要中间体,以苯酚为原料制备胡椒乙酸的合成路线如图所示。
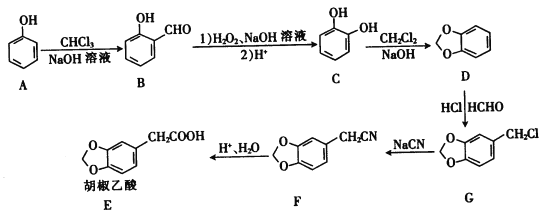
回答下列问题:
(1)下列关于有机物B的说法正确的是________(填字母)。
a.能与FeCl3溶液发生显色反应
b.核磁共振氢谱中只有3组峰
c.能发生银镜反应
d.能与溴水发生加成反应
(2)C的名称是__________,C→D的反应类型是__________。
(3)胡椒乙酸(E)中所含官能团的名称为______________。
(4)G生成F的化学方程式为____________。
(5)W是E的同分异构体,0.5molW与足量碳酸氢钠溶液反应生成1molCO2,已知W的苯环上只有2个取代基,则W的结构共有___________(不含立体异构)种,其中核磁共振氢谱有五组峰的结构简式为____________。
(6)参照上述合成路线,写出以一氯甲苯(![]() )为原料(无杌试剂任选)制备苯乙酸的合成路线:______________________。
)为原料(无杌试剂任选)制备苯乙酸的合成路线:______________________。
【答案】
(1)ac(2)邻苯二酚(或1,2-苯二酚);取代反应
(3)醚键和羧基(2分)
(4)![]()
(5)3(2分); (2分)
(2分)
(6)![]() (3分)
(3分)
【解析】
试题分析:
(1)有机物B中含有酚羟基和醛基,所以能与FeCl3溶液发生显色反应,能发生银镜反应;从结构看,分子中共有6中氢,则核磁共振氢谱中应有6组峰;结构在无碳碳双键或者碳碳三键,不能与溴水发生加成反应,故选ac。
(2)有机物C中含有两个相邻的酚羟基,所以名称是邻苯二酚或1,2-苯二酚。对比C、D的结构及反应条件可知,C→D的反应类型是取代反应。
(3)胡椒乙酸中所含官能团的名称为醚键和羧基。
(4)G生成F为取代反应,反应的化学方程式为![]() 。
。
(5)0.5molW与足量碳酸氢钠溶液反应生成1molCO2,说明W中含有2个羧基。W的苯环上只有2个取代基,即-COOH和-CH2COOH两个取代基,则W共有邻、间、对3种结构,其中核磁共振氢谱有五组峰的处于对位,结构简式为 。
。
(6)目标产物为苯乙酸(![]() ),对比原料一氯甲苯(
),对比原料一氯甲苯(![]() )的结构可知,根据图中G→F→E的合成路线,可以实现将-CH2Cl转化为-CH2COOH。则合成路线为:
)的结构可知,根据图中G→F→E的合成路线,可以实现将-CH2Cl转化为-CH2COOH。则合成路线为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】下列关于糖类、脂肪和蛋白质的叙述正确的是
A. 蛋白质溶液遇CuSO4后产生的沉淀能重新溶解 B. 淀粉水解的最终产物是葡萄糖
C. 葡萄糖能发生氧化反应和水解反应 D. 植物油不能使溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知阿伏伽德罗常数可表示为NA,则下列说法正确的是
A. 任何气体单质在标准状况下体积约为22.4L,则一定含有2NA个原子
B. 常温常压下,22g氧气和26g臭氧所含氧原子总数为3NA
C. 常温常压下,22.4LH2O中含有的氢原子数为2NA
D. 标准状况下,0.3molCO2中含有氧原子数0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 已知图一表示的是可逆反应CO(g)+H2(g) ![]() C(s)+H2O(g)△H>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)
C(s)+H2O(g)△H>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)![]() N2O4(g)△H<0的浓度(c)随时间(t)的变化情况。下列说法中正确的是( )
N2O4(g)△H<0的浓度(c)随时间(t)的变化情况。下列说法中正确的是( )
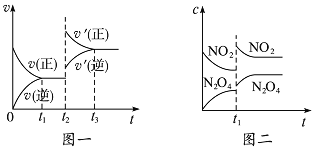
A.图一t2时改变的条件可能是升高了温度或增大了压强
B.图一t2时改变的条件是增大压强,则反应的△H增大
C.图二t1时改变的条件可能是升高了温度
D.若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C 均为短周期的元素,A、B同周期,A、C的最低价离子分别为A2-和C-,B2+和C-具有相同的电子层结构,下列说法中正确的是( )
A.离子半径:A2->C->B2+
B.C元素的最高正价一定为+7价
C.对应气态氢化物的稳定性:A>C
D.还原性:A2-<C-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素M、R形成的简单离子M2-与R+的核外电子数之和为20,下列说法正确的是( )
A.M原子的质子数一定大于R原子的质子数
B.M可能存在16M、18M两种核素
C.M2-与R+的电子层结构不可能相同
D.两种离子结合形成的化合物中可能含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了将混有K2SO4、MgSO4的KNO3固体提纯,并制得纯净的KNO3溶液E,某学生设计如下实验方案:
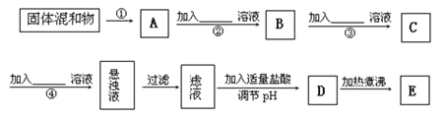
(1)操作①主要是将固体溶解,则所用的主要玻璃仪器是_____ __、____ ___。
(2)操作②~④加入的试剂依次可以为(写化学式):______________________________;
(3)如何判断SO42-已除尽?_________ ____ ___;
(4)写出加入适量盐酸调PH反应的离子方程式_____________________ ____;
(5)该同学的实验设计方案是否严密?请说明理由:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)NaHCO3溶液中存在多种平衡关系,写出相应平衡关系所对应的离子方程式:_ _ 。
NaHCO3溶液显碱性的原因: _ 。
NaHSO4溶液显酸性的原因: 。
(2)在101kPa时,H2在1.00molO2中完全燃烧生成2.00mol液态H2O。放出571.6kJ的热量,表示H2燃烧热的热化学方程式为____________ 。
(3)1.00L 1.00mol/L H2SO4溶液与2.00L 1.00mol/L NaOH溶液完全反应,放出114.6kJ的热量,表示其中和热的热化学方程式为______________ _ 。
(4)已知C(s)+O2(g)=CO2(g) △H1=-393.5kJ/mol,
2CO(g)+O2(g)=2CO2(g) △H2=-566.0kJ/mol,
C(s)+0.5O2(g)=CO(g) △H3=akJ/mol,则a=__________
(5)已知N2(g) +3H2(g) ![]() 2NH3(g)的平衡常数为K1,0.5 N2(g)+1.5H2(g)
2NH3(g)的平衡常数为K1,0.5 N2(g)+1.5H2(g) ![]() NH3(g) 的平衡常数为K2,NH3(g)
NH3(g) 的平衡常数为K2,NH3(g) ![]() 0.5 N2(g)+1.5H2(g) 的平衡常数为K3,写出K1和K2的关系式__________,写出K2和K3的关系式____________,写出K1和K3的关系式_____________
0.5 N2(g)+1.5H2(g) 的平衡常数为K3,写出K1和K2的关系式__________,写出K2和K3的关系式____________,写出K1和K3的关系式_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种短周期元素,A、B同主族,C、D同周期,B、E同周期。气体A2与气体C2混合后点燃能够发生爆炸,且产物在常温常压下是一种无色无味的液体。B、C、E简单离子的核外电子排布相同。E的最高价氧化物可与B的最高价氧化物的水化物反应生成一种易溶于水的的盐,D能形成自然界硬度最大的单质。请根据上述所提供的信息回答下列问题。
(1)写出A、B两种元素的元素名称:A________、B________写出D的最高价氧化物的电子式 。
(2)写出由B和C两元素形成的原子个数比为1:1的化合物F的电子式 ,其存在的化学键是
(3)写出F和A2C反应的离子方程式:____________________。
(4)用电子式表示B2C形成的过程:______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com