
【题目】实验室制备溴苯的反应装置如图所示,下列叙述错误的是( )

A. FeBr3 的作用是催化剂,若没有 FeBr3 可用铁屑代替
B. 实验中装置b中的作用是吸收挥发的苯和溴
C. 装置c中石蕊试液由紫色变为红色,可证明苯与溴发生的是取代反应
D. 反应后的混合液经NaOH溶液洗涤、蒸馏,得到溴苯
【答案】D
【解析】
A. FeBr3 的作用是催化剂,若没有 FeBr3,可向其中加入铁粉,利用Br2与Fe反应产生FeBr3获得,因此也可用铁屑代替,A正确;
B.苯与液溴反应产生溴苯,由于液溴、苯都具有挥发性,为防止它们的干扰,常根据苯、液溴容易溶于有机物四氯化碳的性质,用盛有四氯化碳的洗气瓶吸收挥发的苯和溴,B正确;
C.用液溴与苯在催化剂作用下制取溴苯,挥发的溴、苯被四氯化碳吸收,若装置c中石蕊试液由紫色变为红色,可证明苯与溴反应产生了HBr,HBr溶于水得到氢溴酸,石蕊遇酸变红,故可以证明苯与溴发生的是取代反应,C正确;
D.反应后的混合液中含有溴苯及溶于其中的溴、苯等物质,经水洗、NaOH 溶液洗涤、再水洗,除去未反应的溴单质,分液、干燥、蒸馏,可以得到溴苯,D错误;
故合理选项是D。


科目:高中化学 来源: 题型:
【题目】用固体NaOH配制一定物质的量浓度的溶液时,下列操作会导致溶液浓度偏高的是
A.在烧杯中溶解时,有少量液体溅出B.样品中含有少量Na2O杂质
C.容量瓶使用前未干D.定容时仰视液面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在试管a中先加入2mL 95%的乙醇,边摇动边缓缓加入5mL浓H2SO4并充分摇匀,冷却后再加入2g无水醋酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液。连接好装置,用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验。
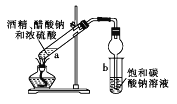
(1)写出a试管中的主要化学反应的方程式________________.
(2)加入浓H2SO4的目的是______________________________.
(3)试管b中观察到的现象是_______________________.
(4)在实验中球形干燥管除了起冷凝作用外,另一个重要作用是______________,其原因_____________.
(5)饱和Na2CO3溶液的作用是______________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将pH均为3,体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随1g![]() 的变化如右图所示。下列说法正确的是
的变化如右图所示。下列说法正确的是
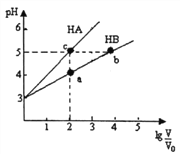
A. 稀释相同倍数时:c(Aˉ)>c(Bˉ-)
B. 水的电离程度:b=c>a
C. 溶液中离子总物质的量:b>c>a
D. 溶液中离子总浓度:a>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.根据下表所示化学反应与数据关系,回答下列问题:
化学反应 | 平衡常数 | 温度 | |
973 K | 1173 K | ||
①Fe(s)+CO2(g)FeO(s)+CO(g) | K1 | 1.50 | 2.15 |
②Fe(s)+H2O(g)FeO(s)+H2(g) | K2 | 2.40 | 1.67 |
③CO(g)+H2O(g)CO2(g)+H2(g) | K3 | ? | ? |
(1)反应①是________(填“吸热”或“放热”)反应。
(2)在973K时,K3=_________。
(3)要使反应③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有______(填写字母序号)。
A.缩小反应容器的容积 B.扩大反应容器的容积 C.升高温度
D.使用合适的催化剂 E.设法减小平衡体系中的CO浓度
Ⅱ.无机和有机氰化物在工农业生产中应用广泛,尤其是冶金工业常用的氰化物,含氰废水的处理显得尤为重要。含氰废水中的氰化物常以[Fe(CN)6]3-和CN-的形式存在,工业上有多种废水处理方法。
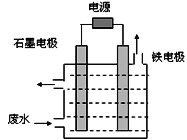
(1)电解处理法:
用如图所示装置处理含CN-废水时,控制溶液pH为9~10并加入NaCl,一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去。铁电极为__________(填“阴极” 或“阳极”),阳极产生ClO-的电极反应为__________________________,阳极产生的ClO-将CN-氧化为无害物质而除去的离子方程式为__________________________。
(2)UV(紫外光线的简称)—H2O2氧化法。
实验过程:取一定量含氰废水,调节pH,加入一定物质的量的H2O2,置于UV工艺装置中,
光照一定时间后取样分析。
【查阅资料】
①在强碱性溶液中4[Fe(CN)6]3-+4OH-===4[Fe(CN)6]4-+O2↑+2H2O,[Fe(CN)6]4-更稳定;
②[Fe(CN)6]3-转化为CN-容易被H2O2除去;
③HCN是有毒的弱酸,易挥发。
【问题设计】
①请写出HCN的电子式________________。
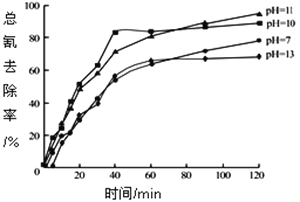
②含氰废水在不同pH下的除氰效果如图所示,pH选择的最佳范围应为________________(选填编号:![]() .7~10;
.7~10;![]() .10~11;
.10~11;![]() .11~13),解释该pH不宜太大的原因___________________。
.11~13),解释该pH不宜太大的原因___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学化学中有很多物质可以实现下图中物质之间的转化。其中反应条件和部分反应的产物已略去。液体B和C可能是单一溶质的溶液,也可能是纯净物。

(1)若A是一种红色金属,气体D能使品红溶液褪色,加热时又恢复原色。写出反应①的化学方程式_______________________________________________。
(2)若A是金属单质,D是一种无色气体,遇到空气变为红棕色,液体C呈浅绿色。
写出反应①的离子方程式________________________________________; 写出反应②的任意一个离子方程式____________________________________________。
(3)若A是一种金属单质,D是最轻的气体,B能否是NaOH溶液________(填“能”或“否”),若能,写出相应的离子方程式 (若否,则不用填此空)__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铅酸蓄电池的工作原理如图所示,其总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。下列判断不正确的是( )
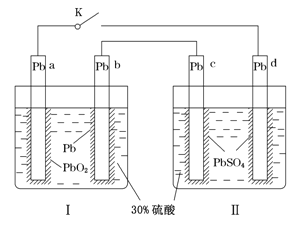
A. 闭合K时,d电极的反应式为PbSO4+2H2O-2e-=PbO2+4H++SO42—
B. 当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2 mol
C. 闭合K时,Ⅱ中SO42—向c电极迁移
D. 闭合K一段时间后,Ⅱ可单独作为原电池,d电极为正极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com