
≥£Œ¬œ¬£¨≈®∂»æ˘Œ™0.1 mol/L µƒœ¬¡–Àƒ÷÷—Œ»Ð“∫£¨∆‰pH≤‚∂®»Áœ¬±ÌÀ˘ æ£∫
| –Ú∫≈ | ¢Ÿ | ¢⁄ | ¢€ | ¢Ð |
| »Ð“∫ | CH3COONa | NaHCO3 | Na2CO3 | NaClO |
| pH | 8.8 | 9.7 | 11.6 | 10.3 |
 ø⁄À„–ƒÀ„ÀŸÀ„”¶”√Âœµ¡–¥∞∏
ø⁄À„–ƒÀ„ÀŸÀ„”¶”√Âœµ¡–¥∞∏ Õ¨≤ΩÕÿ’π‘ƒ∂¡œµ¡–¥∞∏
Õ¨≤ΩÕÿ’π‘ƒ∂¡œµ¡–¥∞∏
| ƒÍº∂ | ∏þ÷–øŒ≥à | ƒÍº∂ | ≥ı÷–øŒ≥à |
| ∏þ“ª | ∏þ“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı“ª | ≥ı“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ∂˛ | ∏þ∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı∂˛ | ≥ı∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ»˝ | ∏þ»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı»˝ | ≥ı»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫µ•—°Ã‚
‘⁄25°Ê ±Ω´pH£Ω11 µƒNaOH »Ð“∫”ÎpH£Ω3 µƒCH3COOH»Ð“¥µ»Ãª˝ªÏ∫œ∫Û£¨œ¬¡–πÿœµ Ω÷–’˝»∑µƒ «
| A£Æc (Na+)=c(CH3COO£≠)+c(CH3COOH) |
| B£Æc(H+)=c(CH3COO£≠)+c(OH“ª) |
| C£Æc (Na+) > c (CH3COO£≠)>c(OH£≠)>c(H+) |
| D£Æc (CH3COO£≠)>c(Na+)>c(H+)>c(OH£≠) |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫µ•—°Ã‚
≥£Œ¬ ±£¨œ¬¡–– ˆ’˝»∑µƒ «
| A£ÆpH=9µƒNH4Cl”ÎNH3°§H2OªÏ∫œ»Ð“∫÷–c(Cl-)>c(NH4+) |
| B£ÆpH=2.5µƒø…¿÷÷–c£®H+£© «pH=3.5µƒƒ˚√ ÀÆ÷–c£®H+£©µƒ1 0±∂ |
| C£ÆAgCl‘⁄0.1 mol£ØL CaCl2»Ð“∫∫Õ0.l mol£ØL NaCl»Ð“∫÷–µƒ»ÐΩ‚∂»œýÕ¨ |
| D£Æ1 mL l mol l L Na2CO3»Ð“∫º”ÀÆœ° Õ÷¡100 mL£¨pH∫ÕKwæ˘ºı–° |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫µ•—°Ã‚
“Œ¬œ¬£¨Ω´0£Æ100 0 mol°§L£≠1—ŒÀ·µŒ»Î20£Æ00 mL Œ¥÷™≈®∂»µƒƒ≥“ª‘™ºÓMOH»Ð“∫÷–£¨»Ð“∫pHÀʺ”»Î—ŒÀ·Ã ª˝±‰ªØ«˙œþ»ÁÕºÀ˘ æ°£œ¬¡–”–πÿÀµ∑®≤ª’˝»∑µƒ «£® £©
| A£Æbµ„£∫c(M+)+c(MOH)£Ωc(Cl°•) |
| B£ÆaµΩbµ„µƒÀƻГ∫µºµÁ–‘“¿¥Œ‘ˆ«ø |
| C£Æ∏√“ª‘™ºÓ»Ð“∫≈®∂»Œ™0£Æ100 0 mol°§L£≠1 |
| D£Æ “Œ¬œ¬£¨MOHµƒµÁ¿Î≥£ ˝Kb£Ω1°¡10£≠5 |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫µ•—°Ã‚
25°Ê ±£¨ƒ≥≈®∂»µƒNH4Cl»Ð“∫pH = 4£¨œ¬¡–– ˆ’˝»∑µƒ «
| A£Æ»Ð“∫÷–µƒ c(OH£≠) = 1°¡10£≠10 mol°§L£≠1 |
| B£Æ»Ð“∫÷–µƒc(NH4+)£æc(Cl£≠)£æc(H+)£æc(OH£≠) |
| C£Æ»Ð“∫÷–µƒc(H+) + c(NH4+) = c(Cl£≠) + c(OH£≠) |
| D£Æ»Ð“∫÷–µƒc(NH3°§H2O) = c(NH4+) |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫µ•—°Ã‚
25°Ê ±£¨”–c(CH3COOH)£´c(CH3COO£≠)£Ω0.1 mol°§L£≠1µƒ“ª◊È¥◊À·°¢¥◊À·ƒ∆ªÏ∫œ»Ð“∫£¨»Ð“∫÷–c(CH3COOH)°¢c(CH3COO£≠)”ÎpH µƒπÿœµ»ÁÕºÀ˘ æ°£œ¬¡–”–πÿ»Ð“∫÷–¿Î◊”≈®∂»πÿœµµƒ– ˆ’˝»∑µƒ «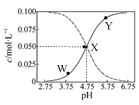
| A£ÆYµ„À˘±Ì 浃»Ð“∫÷–£∫c(CH3COO£≠)£æc(CH3COOH)£æc(H£´)£æc(OH£≠) |
| B£ÆWµ„À˘±Ì 浃»Ð“∫÷–£∫c(Na£´)£´c(H£´)£´c(OH£≠)£´c(CH3COOH)£Ω0.1mol°§L£≠1 |
| C£Æ∏√Œ¬∂»œ¬¥◊À·µƒµÁ¿Î∆Ω∫‚≥£ ˝Œ™10°™4.75 mol°§L£≠1 |
| D£ÆœÚXµ„À˘±Ì 浃»Ð“∫÷–º”»Îµ»Ãª˝µƒ0.05 mol°§L£≠1 NaOH»Ð“∫ £∫c(H£´)£Ωc(CH3COOH)£´c(OH£≠) |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫µ•—°Ã‚
250C ±£¨”–c(CH3COOH)+c(CH3COO£≠)=0.1mol°§L-1µƒ“ª◊È¥◊À·°¢¥◊À·ƒ∆ªÏ∫œ»Ð“∫£¨»Ð“∫÷–c(CH3COOH)°¢c(CH3COO£≠)”ÎpH µƒπÿœµ»ÁÕº7 À˘ æ°£œ¬¡–”–πÿ»Ð“∫÷–¿Î◊”≈®∂»πÿœµµƒ– ˆ’˝»∑µƒ «
| A£ÆpH="5." 5 µƒ»Ð“∫÷–£∫ c(CH3COOH)>c(CH3COO£≠)>c(H£´)>c(OH£≠) |
| B£ÆW µ„À˘±Ì 浃»Ð“∫÷–£∫ c(Na£´)+c(H£´)= c(CH3COOH)+c(OH£≠) |
| C£ÆpH =" 3." 5 µƒ»Ð“∫÷–£∫ c(Na£´) +c(H£´) -c(OH£≠) +c(CH3COOH)=0.1mol°§L-1 |
| D£ÆœÚW µ„À˘±Ì 浃1.0L »Ð“∫÷–Õ®»Î0.05mol HCl ∆¯ÃÂ(»Ð“∫ê˝±‰ªØø…∫ˆ¬‘)£∫ c(H£´)= c(CH3COOH)+c(OH£≠) |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫µ•—°Ã‚
œ¬¡–∏˘æð µ—È≤Ÿ◊˜∫Õœ÷œÛÀ˘µ√≥ˆµƒΩ·¬€’˝»∑µƒ «
| —°œÓ | µ—È≤Ÿ◊˜ | µ—Èœ÷œÛ | Ω· ¬€ |
| A | Ω´…Ÿ¡øFe(NO3)2 ‘—˘º”ÀÆ»ÐΩ‚£¨µŒº”œ°H2SO4À·ªØ£¨‘ŸµŒº”KSCN»Ð“∫ | »Ð“∫±‰≥…∫Ï…´ | Fe(NO3)2 ‘—˘“—±‰÷ |
| B | Ω´…Ÿ¡øƒ≥ŒÞ…´∆¯ÃÂÕ®»Î≥Œ«Â ت“ÀÆ | ≥ˆœ÷∞◊…´≥¡µÌ | ∏√∆¯Ã“ª∂® «CO2 |
| C | ∑÷±≤‚∂®≥£Œ¬œ¬0.1 mol°§L£≠1 Na2SiO3»Ð“∫∫ÕNa2CO3»Ð“∫µƒpH | pH£∫Na2SiO3£æ Na2CO3 | ∑«Ω Ù–‘£∫Si£æC |
| D | œÚ≈®∂»æ˘Œ™0.1 mol°§L£≠1 NaCl∫ÕNaIªÏ∫œ»Ð“∫÷–£¨µŒº”…Ÿ¡øAgNO3»Ð“∫ | ≥ˆœ÷ª∆…´≥¡µÌ | Ksp(AgCl)£æKsp(AgI) |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫µ•—°Ã‚
0.1mol/LHF»Ð“∫µƒpH=2£¨‘Ú∏√»Ð“∫÷–”–πÿ≈®∂»πÿœµ Ω≤ª’˝»∑µƒ «
| A£Æc(H+)£æc(F-) | B£Æc(H+)£æc(HF) |
| C£Æc(HF)£æc(OH-) | D£Æc(HF)£æc(F-) |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com