
【题目】下列溶液中物质的量浓度为1mol·L-1的是
A.将20gNaOH溶解在500mL水中
B.将22.4L HCl气体溶于水配成1 L溶液
C.将1 L 10 mol·L-1浓盐酸加入9L水中
D.将10gNaOH溶解在少量水中,恢复至室温,再加蒸馏水直到溶液体积为250ml
科目:高中化学 来源: 题型:
【题目】已知一个可逆反应,若正反应为自发过程,则其逆反应为非自发过程,反之亦然。
(1)已知2CO(g)![]() CO2(g)+C(s),T=980 K时ΔH-TΔS=0。当体系温度低于980 K时,估计ΔH-TΔS________0(填“大于”、“小于”或“等于”,下同);当体系温度高于980 K时,估计ΔH-TΔS________0。
CO2(g)+C(s),T=980 K时ΔH-TΔS=0。当体系温度低于980 K时,估计ΔH-TΔS________0(填“大于”、“小于”或“等于”,下同);当体系温度高于980 K时,估计ΔH-TΔS________0。
(2)电子工业中清洗硅片上的SiO2(s)的反应为SiO2(s)+4HF(g)===SiF4(g)+2H2O(g) ΔH(298.15 K)=-94.0 kJ/mol,ΔS(298.15 K)=-75.8 J/(mol·K),设ΔH和ΔS不随温度而变化,则此反应自发进行的温度是________。
(3)化学反应2NO(g)+2CO(g)===N2(g)+2CO2(g)在298 K、100 kPa下:ΔH=-113.0 kJ/mol,ΔS=-145.3 J/(mol·K),反应在常温下________(填“能”或“不能”)自发进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)磷是生物体中不可缺少的元素之一,在自然界中磷总是以磷酸盐的形式出现的,例如磷酸钙矿Ca3(PO4)2、磷灰石Ca5F(PO4)3等.
(1)磷的某种核素中,中子数比质子数多1,则表示该核素的原子符号为 .
(2)白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在电炉中(约1550℃)下通过下面两个反应共熔得到.
①2Ca3(PO4)2(s)+5C(s)═6CaO(s)+P4(s)+5CO2(g)△H1=+Q1kJmol﹣1
②CaO(s)+SiO2(s)═CaSiO3(s)△H2=﹣Q2kJmol﹣1
写出电炉中发生总反应的热化学方程式 .
(3)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:2Ca3(PO4)2+6SiO2=6CaSiO3+P4O10;10C+P4O10=P4↑+10CO↑,上述反应中的各种物质,属于酸性氧化物的有 .
(Ⅱ)离子交换膜是一类具有离子交换功能的高分子材料.一容器被离子交换膜分成左右两部分,如右图所示.若该交换膜为阳离子交换膜(只允许阳离子自由通过),左边充满盐酸酸化的H2O2溶液,右边充满滴有KSCN溶液的FeCl2溶液(足量),一段时间后右边可观察到的现象: ,若该交换膜为阴离子交换膜(只允许阴离子自由通过),左边充满含2mol NH4Al(SO4)2的溶液,右边充满含3mol Ba(OH)2的溶液,当有2mol SO42﹣通过交换膜时(若反应迅速完全),则左右两室沉淀的物质的量之比为 .
![]()
(Ⅲ)某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质,利用相关工艺可进行提纯与综合利用.通入一定量的N2后,在1500℃下与Cl2充分反应得到纯化石墨与气体混合物,然后降温至80℃,分别得到不同状态的两类物质a和b.(注:石墨中氧化物杂质均转变为相应的氯化物,SiCl4的沸点为57.6℃,金属氯化物的沸点均高于150℃.)
(1)若a与过量的NaOH溶液反应,可得两种盐,其中一种盐的水溶液具有粘合性,化学反应方程式为 .
(2)若b与过量的NaOH溶液充分反应后,过滤,所得滤液中阴离子有 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知阿伏伽德罗常数可表示为NA,则下列说法正确的是( )
A.17gNH3所含中子数目为10 NA
B.常温常压下,22 g氧气和26 g臭氧所含的氧原子总数为3NA
C.常温常压下,18g H2O含有的电子总数为8NA
D.常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铁铵[aFe2(SO4)3·b(NH4)2SO4·cH2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。某化工厂以硫酸亚铁(含少量硝酸钙)和硫酸铵为原料,设计了如下工艺流程制取硫酸铁铵。
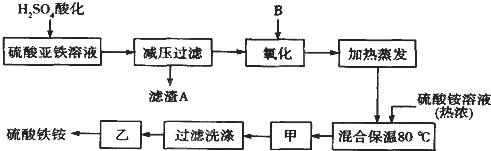
请回答下列问题:
(1)硫酸亚铁溶液加H2SO4酸化的主要目的是 。
(2)下列物质中最适合的氧化剂B是 。
a.NaClO b.H2O2 c.KMnO4 d.K2Cr2O7
(3)操作甲的名称是:甲 。
(4)上述流程中,氧化之后和加热蒸发之前,需取少量 (填试剂的化学式)检验Fe2+是否已全部被氧化;
(5)称取14.00 g所得样品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14 g沉淀;向另一份溶液中加入0.05 mol Ba (NO3)2溶液,恰好完全反应。则该硫酸铁铵的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2.8g Fe全部溶于一定浓度、200mL的HNO3溶液中,得到标准状况下的气体1.12L,测得反应后溶液的pH为1。若反应前后溶液体积变化忽略不计,下列有关判断正确的是
A.反应后溶液中c(NO3-)=0.85mol/L
B.反应后的溶液最多还能溶解1.4gFe
C.反应后溶液中铁元素可能以Fe2+形式存在
D.1.12L气体可能是NO、NO2的混合气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“化学多米诺实验”即利用反应中气体产生的压力和虹吸作用原理,使若干化学实验依次发生,整个过程只须控制第一个反应,就好像多米诺骨牌游戏一样。右图就是一个“化学多米诺实验”。

各装置中试剂或物质:
A.2mol/L H2SO4
B.Zn
C.2mol/LH2SO4+CuSO4
D.Zn
E.CuSO4溶液
F.NH3H2O
G.30%H2O2
H.H2S溶液
I.NaOH溶液
已知:Cu2++4NH3H2O=[Cu(NH3)4]2+ +4H2O 该反应产物可作为H2O2分解的催化剂。请回答下列问题:
(1)进行实验前必须进行的操作 ;
(2)B与D两容器中反应速率比较B________D(填>、<、=)原因是 ;
(3)H中的现象是 ;
(4)I的作用是(用化学方程式表示) ;
(5)A和B之间导管a的作用是 ;
(6)在该实验中不涉及的反应类型是(填序号) 。
①分解反应 ②化合反应 ③置换反应 ④复分解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com