
【题目】常温下,在25mL0.1mol/LNaOH 溶液中逐滴加入0.2mol/LCH3COOH 溶液,下图曲线所示的有关粒子浓度关系错误的是
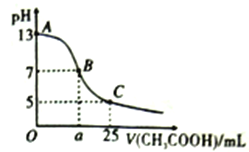
A. 任一点一定都有c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
B. B点:a=12.5,c(Na+ ) =c(CH3COO-)>c(OH-)= c(H+)
C. C点:c(CH3COO-)+ c(CH3COOH)=2 c(Na+ )=0.1mol/L
D. C点:c(CH3COO-):c(CH3COOH))=3:2,则CH3COOH的Ka=1.5×10-5
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】同温同压下,由N2O和CO2组成的混合气体的密度是C2H4、N2和H2组成的混合气体密度的 2倍,则C2H4、N2和H2组成的混合气体中H2的质量分数为
A. 3/13 B. 10/13 C. 大于3/13,小于10/13 D. 3/143
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图转化关系判断下列说法不正确的是(反应条件已略去)
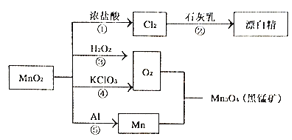
A. 反应①②③④⑤均属于氧化还原反应
B. 生成黑锰矿的反应中,3molMn参加反应转移4mol电子
C. 生成等量的O2,反应③和④转移的电子数之比为1:2
D. 反应⑤为铝热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】⑴若某原子的摩尔质量是M g /mol,则一个该原子的真实质量是__________g。
⑵483g Na2SO4·10H2O中所含的Na+的物质的量是________SO42—的物质的量是_________,所含H2O分子的数目是_______________个。
⑶标准状况下,4 g H2、11.2LO2、1 mLH2O中,所含分子数最多的是______________,
含原子数最多的是_________,质量最小的是___________,体积最小的是__________。
⑷相同状况下,相同质量的某气体物质与氢气的体积比为1︰8,则该气体的摩尔质量为______________。
⑸等质量的O2和O3,它们物质的量之比为__________,所含分子个数比为___________,所含氧原子个数比为__________,相同状况下的体积比为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
IVA 族元素及其化合物在材料等方面有重要用途。回答下列问题:
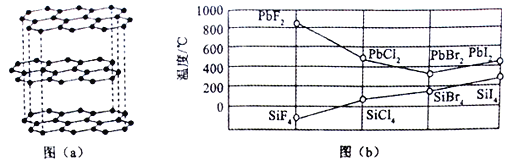
(1)碳的一种单质的结构如图(a)所示。该单质的晶体类型为________________,依据电子云的重叠方式,原子间存在的共价键类型有_____________,碳原子的杂化轨道类型为_________。
(2)石墨烯是从石墨材料中剥离出来的、由单层碳原子组成的二维晶体。将氢气加入到石墨烯中可制得一种新材料石墨烷。下列判断错误的是___________。
A.石墨烯是一种强度很高的材料
B.石墨烯是电的良导体而石墨烷则为绝缘体
C.石墨烯与石墨烷均为高分子化合物
D.石墨烯与H2 制得石墨烷的反应属于加成反应
(3)四卤化硅SiX4的沸点和二卤化铅PbX2 的熔点如图(b)所示。
①SiX4的沸点依F、Cl、Br、I 次序升高的原因是_________________________________。
②结合SiX4的沸点和PbX2的熔点的变化规律,可推断: 依F、Cl、Br、I 次序,PbX2 中的化学键的离子性___________、共价性______________。(填 “增 强”“不变”或“减 弱 ”)
(4)碳的另一种单质C60,晶胞结构与金属铜晶胞相似,其晶胞参数为a nm,晶体密度为_______g·cm-3(只列计算式,不需化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验室以一种工业上的废渣(废渣主要含有MgCO3、MgSiO3和少量Fe、Al的氧化物)为原料,制备MgCO3·3H2O。实验流程如下图所示:

(1)为了加快废渣的酸溶速率,可采取的办法有_________(任写一点),酸溶时废渣中主要成分发生反应的离子方程式为___________________________________。
(2)加入30%H2O2的目的是__________________________________。
(3)用萃取分液的方法除去溶液中的Fe3+
萃取分液完成后,检验水相中是否含有Fe3+的最佳试剂是__________________________。
(4)室温下,除去MgSO4溶液中的A13+(使Al3+浓度小于1×10-6mol/L)而不引入其它杂质,应加入的试剂X为__________,应调节pH的范围为_________________。
已知:①Ksp[Al(OH)3]=1.0×10-33 ②pH=8.5 时,Mg(OH)2开始沉淀
(5)下图为不同反应温度下所得水合碳酸镁的X射线衍射谱图。由图可知,干燥时需控制温度范围为___________________,温度较高时MgCO3·3H2O发生转化的化学方程式为_______________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.1mol由两种气态烃组成的混合气体完全燃烧后,得到0.16mol CO2和3.6克水,则混合气体中( )
A. 一定有甲烷
B. 一定是甲烷和乙烯
C. 可能有乙烷
D. 一定有乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个容积相同的容器中,一个盛有HCl气体,另—个盛有H2和Cl2的混合气体。在同温同压下, 两容器内的气体一定具有相同的( )
A. 原子数 B. 密度 C. 质量 D. 质子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应N2(g)+3H2(g) ![]() 2NH3(g)ΔH<0,下列研究目的和示意图相符的是( )
2NH3(g)ΔH<0,下列研究目的和示意图相符的是( )
A | B | C | D | |
研究目的 | 压强对反应的影响(p2>p1) | 温度对反应的影响 | 平衡体系中增加N2浓度对反应的影响 | 催化剂对反应的影响 |
示意图 |
|
|
|
|
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com