
| A、原子半径:A>B>C |
| B、单质的氧化性:B>A>C |
| C、气态氢化物的稳定性:A<B<C |
| D、原子序数:A>B>C |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
A、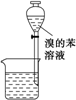 装置①为放出萃取溴水后的苯层 |
B、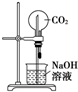 装置②为喷泉实验 |
C、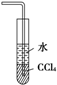 装置③不能用来吸收HCl气体 |
D、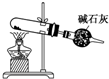 以NH4Cl为原料,装置④可用于制备少量NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 酸 | 碱 | 盐 | 酸性氧化物 | |
| A | 硝酸 | 纯碱 | 烧碱 | 二氧化硫 |
| B | 硫酸 | 烧碱 | 食盐 | 一氧化碳 |
| C | 醋酸 | 苛性钠 | 石灰石 | 水 |
| D | 碳酸 | 苛性钾 | 硫酸钡 | 三氧化硫 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、431 kJ |
| B、945.6 kJ |
| C、649 kJ |
| D、869 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH3?H2O |
| B、MgO |
| C、Mg(OH)2 |
| D、MgCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、放电时正极反应为:Zn-2e-+2OH-═Zn(OH)2 |
| B、该原电池,Zn作正极,可用石墨等作负极 |
| C、放电时每转移3mol电子,正极有1mol K2FeO4被氧化 |
| D、放电时正极附近溶液的碱性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
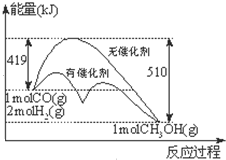 反应CO(g)+2H2(g)?CH3OH(g)过程中能量的变化如图示.下列判断不正确的是( )
反应CO(g)+2H2(g)?CH3OH(g)过程中能量的变化如图示.下列判断不正确的是( )| A、达到平衡时,升高温度,CO的转化率减小 |
| B、1mol CO(g)和2mol H2(g)在密闭容器中反应,达平衡时,放出的热量为91KJ |
| C、相同条件下,1mol CO(g)和2mol H2(g)完全反应生成1mol液态CH3OH放出的热量大于91KJ |
| D、反应热取决于反应物总能量与生成物总能量的相对大小,与反应发生的条件无关 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com