
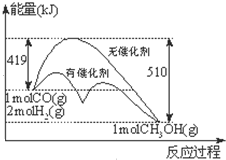
 反应CO(g)+2H2(g)?CH3OH(g)过程中能量的变化如图示.下列判断不正确的是( )
反应CO(g)+2H2(g)?CH3OH(g)过程中能量的变化如图示.下列判断不正确的是( )| A、达到平衡时,升高温度,CO的转化率减小 |
| B、1mol CO(g)和2mol H2(g)在密闭容器中反应,达平衡时,放出的热量为91KJ |
| C、相同条件下,1mol CO(g)和2mol H2(g)完全反应生成1mol液态CH3OH放出的热量大于91KJ |
| D、反应热取决于反应物总能量与生成物总能量的相对大小,与反应发生的条件无关 |


科目:高中化学 来源: 题型:
| A、原子半径:A>B>C |
| B、单质的氧化性:B>A>C |
| C、气态氢化物的稳定性:A<B<C |
| D、原子序数:A>B>C |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、9 | B、12 | C、16 | D、20 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨气通入稀硫酸:NH3+H+=NH4+ |
| B、稀氢氧化钠溶液和氯化铵溶液混合:NH4++OH-=NH3?H2O |
| C、碳酸氢铵和少量浓氢氧化钠溶液混合:NH4++OH-=NH3↑+H2O |
| D、Cl2和水反应:Cl2+H2O?H++Cl-+HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4+ |
| B、N2O |
| C、NO |
| D、NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 元素 | 结构及性质 |
| ① | A | A单质是生活中常见金属,它有两种氯化物,相对分子质量相差35.5 |
| ② | B | B原子最外层电子数是内层电子总数的1/5 |
| ③ | C | C是常见化肥的主要元素,单质常温下呈气态 |
| ④ | D | D单质被誉为“信息革命的催化剂”,是常用的半导体材料 |
| ⑤ | E | 通常情况下,E没有最高正化合价,A、B、C、D、F都能与E形成化合物 |
| ⑥ | F | F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com