
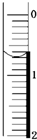
 化工试剂草酸钠常用于制革、烟火、整理织物等.纯Na2C2O4为白色晶体,溶于水,不溶于乙醇,有还原性.实验室可用标准KMnO4溶液测定市售草酸钠中Na2C2O4的质量分数(假设杂质不与KMnO4反应).
化工试剂草酸钠常用于制革、烟火、整理织物等.纯Na2C2O4为白色晶体,溶于水,不溶于乙醇,有还原性.实验室可用标准KMnO4溶液测定市售草酸钠中Na2C2O4的质量分数(假设杂质不与KMnO4反应).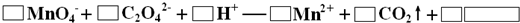
| 滴定终点 | 第一次终点 | 第二次终点 | 第三次终点 | 第四次终点 |
| 滴定管液面刻度 | 20.72mL | 21.70mL | 20.68mL | 20.70mL |
| (20.72+20.68+20.70-0.70×3)mL |
| 3 |
| (20.72+20.68+20.70-0.70×3)mL |
| 3 |
| 0.06mol/L |
| 2 |
| 2.010g |
| 2.680g |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、12C、13C、14C 为碳元素的三种核素.元素周期表中碳的相对原子质量为12.01,说明自然界中的碳主要以12C的核素形式存在.14C为放射性核素,可用于同位素示踪 |
| B、汽车尾气催化转化装置可将尾气中的NO和CO等有害气体转化为N2和CO2,该装置中的催化剂可降低NO和CO反应的活化能,有利于提高该反应的平衡转化率 |
| C、能量是可以互相转化的.植物的光合作用可将太阳能转变成化学能,单晶硅可将光能转变成电能.原电池和电解池可实现化学能和电能的相互转化 |
| D、乳酸分子中既有羟基又有羧基,因此可在一定条件下缩聚得到聚乳酸(PLA).该高分子化合物是一种可降解的环保材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
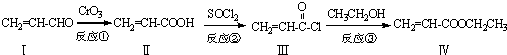
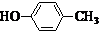 也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为
也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
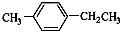 )是一种重要的有机原料,用该物质可合成其他物质.
)是一种重要的有机原料,用该物质可合成其他物质.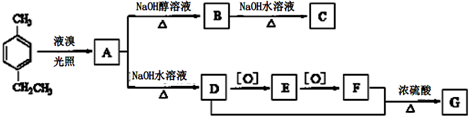
查看答案和解析>>
科目:高中化学 来源: 题型:
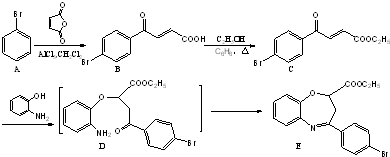
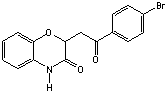 和一种常见的有机物F,F的结构简式为
和一种常见的有机物F,F的结构简式为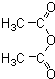
| H2O |
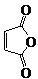 俗名“马莱酐”,它是马莱酸(顺丁烯二酸:)的酸酐.
俗名“马莱酐”,它是马莱酸(顺丁烯二酸:)的酸酐.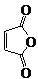 为原料制备化合物
为原料制备化合物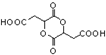 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:| 浓H2SO4 |
| 170℃ |
| Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
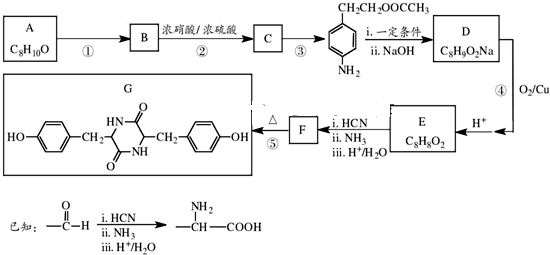
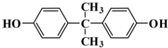 )与光气(
)与光气(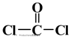 )聚合得到,请写出该聚碳酸酯的结构简式
)聚合得到,请写出该聚碳酸酯的结构简式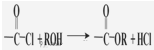 )
)查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
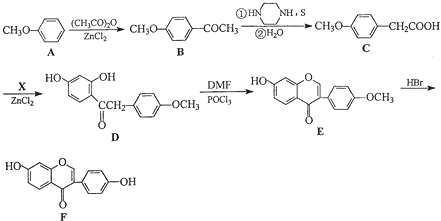
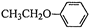 和(CH3CO)2O为原料制备药物中间体
和(CH3CO)2O为原料制备药物中间体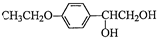 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C=CH2
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C=CH2| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
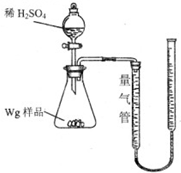 用如图所示装置测定Fe和Fe2O3的混合物中单质铁的质量分数(夹持部分已略去).称取Wg样品置于锥形瓶中,通过分液漏斗加入足量稀硫酸使样品完全溶解.实验前量气管起始读数为amL,实验后量气管的最终读数为bmL.
用如图所示装置测定Fe和Fe2O3的混合物中单质铁的质量分数(夹持部分已略去).称取Wg样品置于锥形瓶中,通过分液漏斗加入足量稀硫酸使样品完全溶解.实验前量气管起始读数为amL,实验后量气管的最终读数为bmL.| 序号 | 溶液中可能存在 的金属离子 | 选择最少种数的试剂,验证该 假设(填字母) |
| ① | ||
| ② | ||
| ③ |
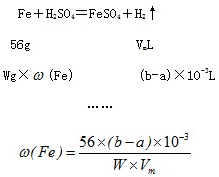
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com