
【题目】下列说法正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.吸热反应不加热一定不能发生
C.放热的反应在常温下一定很容易发生
D.反应是放热还是吸热须看反应物和生成物所具有的总能量的相对大小
【答案】D
【解析】解:A、需要加热才能发生的反应不一定是吸热反应,如铝热反应需要在高温下发生,但是放热反应,故A错误;B、有的吸热反应比一定需要加热,如氯化铵和氢氧化钡晶体的反应就是吸热反应,故B错误;
C、放热的反应在常温下不一定很容易发生,如:铝热反应2 Al+Fe2O3 ![]() Al2O3+2Fe是放热反应,但需在高热条件下以保证足够的热量引发氧化铁和铝粉反应,故C错误;
Al2O3+2Fe是放热反应,但需在高热条件下以保证足够的热量引发氧化铁和铝粉反应,故C错误;
D、放热反应是指:反应物所具有的总能量高于生成的总能量,在反应中会有一部分能量转变为热能的形式释放,反之,就是吸热反应,故D正确.
故选D.
【考点精析】解答此题的关键在于理解吸热反应和放热反应的相关知识,掌握化学上把吸收热量的化学反应称为吸热反应;化学上把放出热量的化学反应称为放热反应.


科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)0.5molH2SO4的质量是;
(2)标准状况下,1.92g某气体的体积为672mL,则该气体的摩尔质量为;
(3)等质量的SO2和SO3的物质的量之比;氧原子个数比为;
(4)11.1gCaCl2固体溶于水配成500mL溶液,其浓度为molL﹣1 , 从中取出100mL溶液,其中Cl﹣的物质的量为mol;再把取出的溶液加水稀释成500mL,则此时CaCl2溶液的浓度为molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 溴水中有下列平衡Br2+H2O![]() HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅
B. 合成氨反应,为提高氨的产率,理论上应采取降低温度的措施
C. 反应CO(g)+NO2(g) ![]() CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深
CO2(g)+NO(g)(正反应为放热反应),达平衡后,升高温度体系颜色变深
D. 对于反应2HI(g) ![]() H2(g)+I2 (g),达平衡后,缩小容器体积可使体系颜色变深
H2(g)+I2 (g),达平衡后,缩小容器体积可使体系颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T°C时,在一固定容积的密闭容器中发生反应:A(g)+B(g)C(s)△H<0,按照不同配比充入A,B,达到平衡时容器中A,B浓度变化如图中曲线(实线)所示,下列判断正确的是( ) 
A.T°C时,该反应的平衡常数值为4
B.c点没有达到平衡,此时反应向逆向进行
C.若c点为平衡点,则此时容器内的温度高于T°C
D.T°C时,直线cd上的点均为平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对16O叙述正确的是
A. 16O原子的核外电子数为8 B. 16O与 18O 互为同素异形体
C. 16O的中子数为16 D. 氧元素的近似相对原子质量是16
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
2CO(g)+O2(g)=2CO2(g)△H=﹣566kJ/mol;
Na2O2(s)+CO2(g)=Na2CO3(s)+ ![]() O2(g)△H=﹣226kJ/mol
O2(g)△H=﹣226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
A.CO的燃烧热为283 kJ
B.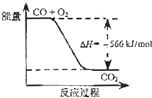
如图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)△H>﹣452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把一定量的Na2O2和NaHCO3的混合粉末分为两等份,将其中一份加入到100mL稀盐酸中恰好完全反应,生成的气体干燥后体积为2.24L(标况);再将此气体通入另一份混合物中,恰好完全反应后,得到O2 2.016L(标况),则加入稀盐酸的物质的量浓度是( )
A.3.4mol/L
B.0.2mol/L
C.1.8mol/L
D.3.6mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学学习中使用数轴的表示方法可起到直观、形象的效果,下列表达中不正确的是( )
A.常温下溶液的pH与酸碱性的关系: ![]()
B.硫的化合物中化合价与其氧化性、还原性的关系: ![]()
C.Fe在Cl2中的燃烧产物: ![]()
D.氨水与SO2反应后溶液中的铵盐: ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com