
【题目】把一定量的Na2O2和NaHCO3的混合粉末分为两等份,将其中一份加入到100mL稀盐酸中恰好完全反应,生成的气体干燥后体积为2.24L(标况);再将此气体通入另一份混合物中,恰好完全反应后,得到O2 2.016L(标况),则加入稀盐酸的物质的量浓度是( )
A.3.4mol/L
B.0.2mol/L
C.1.8mol/L
D.3.6mol/L
【答案】A
【解析】解:标况下2.24L混合气体的物质的量为: ![]() =0.1mol,
=0.1mol,
2.016LO2的物质的量为:n(O2)= ![]() =0.09mol,则:
=0.09mol,则:
2Na2O2+ | 2CO2 | =2Na2CO3+O2 | 气体物质的量减小△n |
2 | 2 | 2 | |
n(CO2) | 0.1mol﹣0.09mol=0.01mol |
所以:n(CO2)= ![]() =0.02mol,
=0.02mol,
由于恰好完全反应,则第一份生成的CO2与混合物中含有的过氧化钠反应,第一份生成CO2的为0.02mol,生成的O2为:0.1mol﹣0.02mol=0.08mol,则:
2Na2O2+ | 4HCl= | =4NaCl+2H2O+ | O2↑ |
0.32mol | 0.08mol | ||
NaHCO3+ | 4HCl= | =NaCl+H2O+ | CO2↑ |
0.02mol | 0.02mol |
所以消耗的HCl的物质的量为:0.32mol+0.02mol=0.34mol,其物质的量浓度为: ![]() =3.4mol/L,
=3.4mol/L,
故选A.


科目:高中化学 来源: 题型:
【题目】已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体.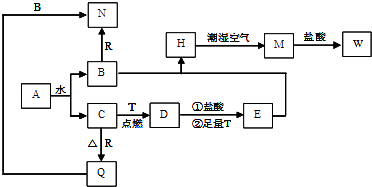
(1)写出下列物质的化学式:
A: D: R: .
(2)按要求写下列反应方程式:
H在潮湿空气中变成M的化学方程式:;
D与盐酸反应的离子方程式: .
(3)检验气体C的方法: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼和铝位于同一主族,它们可以形成许多组成和性质类似的化合物.一种用硼镁矿(Mg2B2O5H2O)制取单质硼的工艺流程图如下: 
回答下列问题:
(1)Mg2B2O5H2O中B的化合价为 .
(2)溶液b中溶质的化学式为 .
(3)用pH试纸测溶液pH的操作方法是 .
(4)写出Mg2B2O5H2O与盐酸反应的化学方程式:
(5)制得的粗硼在一定条件下生成BI3 , BI3加热分解可以得到纯净的单质硼.现将0.0200g粗硼制成的BI3完全分解,生成的I2用0.3000mo1.L﹣1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液15.00mL.(已知:I2+2S2O32﹣=2I﹣+S4O62﹣)
①滴定操作中指示剂通常为
②该粗硼样品的纯度为 .
③若滴定管在使用前未用Na2S2O3标准溶液润洗,测得样品的纯度将(填“偏高”、“偏低”或“无影响”).
(6)请仿照如图形式设计从沉淀a中获得单质Mg的流程图(提示:在箭头上方或下方标出所用试剂或实验操作). ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子的组合为无色溶液且可以大量共存的是
A. Na+ 、NH4+ 、NO3-、MnO4- B. K + 、Ag+ 、Cl-、Br-
C. K +、SO42-、OH-、AlO2- D. Ba2+ 、Na+ 、OH-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)0.5molH2SO4的质量是;
(2)标准状况下,1.92g某气体的体积为672mL,则该气体的摩尔质量为;
(3)等质量的SO2和SO3的物质的量之比;氧原子个数比为;
(4)11.1gCaCl2固体溶于水配成500mL溶液,其浓度为molL﹣1 , 从中取出100mL溶液,其中Cl﹣的物质的量为mol;再把取出的溶液加水稀释成500mL,则此时CaCl2溶液的浓度为molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物命名正确的是( )
A.CH3(CH2)4CH3 1,4﹣二甲基丁烷
B.CH3CH(CH3)CH=CH2 甲基丁烯
C.CH3CH2CH(CH3)2 2﹣甲基丁烷
D.CH2ClCH2Cl 二氯乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤的气化是高效、清洁的利用煤炭的重要途径之一.
(1)焦炭与水蒸气反应是将固体煤变为气体燃料的方法.已知:
①C(s)+O2 (g)=CO2 (g)△H=﹣393.5kJmol﹣1
②CO(g)+ ![]() O2 (g)=CO2 (g)△H=﹣283.0kJmol﹣1
O2 (g)=CO2 (g)△H=﹣283.0kJmol﹣1
③H2(g)+ ![]() O2 (g)=H2O (g)△H=﹣241.8kJmol﹣1
O2 (g)=H2O (g)△H=﹣241.8kJmol﹣1
则碳与水蒸气反应生成一氧化碳和氢气的热化学方程式是 , 该反应的化学平衡常数K随温度的升高将(填“增大”、“减小”或“不变”).
(2)CO可以与H2O(g)进一步发生反应CO(g)+H2O(g)CO2(g)+H2(g)△H<0.在甲、乙两个恒容密闭容器中,起始时按照表数据进行投料,在800℃时达到平衡状态,K=1.0.
H2O | CO | CO2 | H2 | |
甲 n/mol | 0.10 | 0.30 | 0.10 | 0.50 |
乙 n/mol | 0.20 | 0.20 | 0 | 0 |
起始时,甲容器中反应向(填“正反应”或“逆反应”)方向进行;平衡时,乙容器中CO的转化率为 .
(3)以CO为燃料制作燃料电池,电池的正极通入O2和CO2 , 负极通入CO,电解质是熔融碳酸钠,写出工作时正极的电极反应式: , 若使用该电池电解熔融Al2O3制取10.8g Al,则理论上需要氧气的体积为(标准状况下)L.
(4)将(2)中生成的混合气用过量的NaOH溶液吸收,得到的溶液中有一种溶质可以水解,请写出其水解的离子方程式: , .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅的说法不正确的是( )
A.硅是非金属元素,但它的单质是灰黑色有金属光泽的固体
B.硅的导电性能介于金属和绝缘体之间,是良好的半导体材料
C.在常温下,硅的化学性质活泼
D.硅是人类将太阳能转换为电能的常用材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
2CO(g)+O2(g)=2CO2(g)△H=﹣566kJ/mol;
Na2O2(s)+CO2(g)=Na2CO3(s)+ ![]() O2(g)△H=﹣226kJ/mol
O2(g)△H=﹣226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
A.CO的燃烧热为283 kJ
B.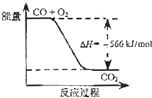
如图可表示由CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)△H>﹣452 kJ/mol
D.CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com