
【题目】硼和铝位于同一主族,它们可以形成许多组成和性质类似的化合物.一种用硼镁矿(Mg2B2O5H2O)制取单质硼的工艺流程图如下: 
回答下列问题:
(1)Mg2B2O5H2O中B的化合价为 .
(2)溶液b中溶质的化学式为 .
(3)用pH试纸测溶液pH的操作方法是 .
(4)写出Mg2B2O5H2O与盐酸反应的化学方程式:
(5)制得的粗硼在一定条件下生成BI3 , BI3加热分解可以得到纯净的单质硼.现将0.0200g粗硼制成的BI3完全分解,生成的I2用0.3000mo1.L﹣1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液15.00mL.(已知:I2+2S2O32﹣=2I﹣+S4O62﹣)
①滴定操作中指示剂通常为
②该粗硼样品的纯度为 .
③若滴定管在使用前未用Na2S2O3标准溶液润洗,测得样品的纯度将(填“偏高”、“偏低”或“无影响”).
(6)请仿照如图形式设计从沉淀a中获得单质Mg的流程图(提示:在箭头上方或下方标出所用试剂或实验操作). ![]()
【答案】
(1)+3
(2)NaHCO3
(3)把一小块pH试纸放在表面皿(或玻璃片)上,用蘸有待测溶液的玻璃棒点在试纸的中部,试纸变色后与标准比色卡比较
(4)Na2B4O7?10H2O+2HCl=2NaCl+5H2O+4H3BO3
(5)淀粉溶液;82.5%;偏高
(6)![]()
【解析】解:(1)根据化合价代数和为0,可知Mg2B2O5H2O中B的化合价为+3,所以答案是:+3;(2)由上述分析可知,通入过量二氧化碳,则得溶液b为NaHCO3 , 所以答案是:NaHCO3;(3)用pH试纸测溶液pH的操作方法是把一小块pH试纸放在表面皿(或玻璃片)上,用蘸有待测溶液的玻璃棒点在试纸的中部,试纸变色后与标准比色卡比较;所以答案是:把一小块pH试纸放在表面皿(或玻璃片)上,用蘸有待测溶液的玻璃棒点在试纸的中部,试纸变色后与标准比色卡比较;(4)Na2B4O710H2O与盐酸反应根据强酸制弱酸的原理生成氯化钠、水和硼酸,反应方程式为:Na2B4O710H2O+2HCl=2NaCl+5H2O+4H3BO3 ,
所以答案是:Na2B4O710H2O+2HCl=2NaCl+5H2O+4H3BO3;(5)①滴定过程中有碘单质参与,可以使用淀粉溶液作为指示剂;所以答案是:淀粉溶液;
②硫代硫酸钠的物质的量为:0.3mol/L×0.015L=0.0045mol,根据关系式:B~BI3~ ![]() I2~3S2O32﹣ , n(B)=
I2~3S2O32﹣ , n(B)= ![]() n(S2O32﹣)=0.0015mol,
n(S2O32﹣)=0.0015mol,
硼的质量为:11g/mol×0.0015mol=0.0165g,粗硼中硼的含量为: ![]() ×100%=82.5%,
×100%=82.5%,
所以答案是:82.5%;
③若滴定管在使用前未用Na2S2O3标准溶液润洗,则测得Na2S2O3标准溶液体积偏大,所以根据B~BI3~ ![]() I2~3S2O32﹣ , 样品的纯度将偏高,所以答案是:偏高;(6)沉淀a为Mg(OH)2固体,加浓盐酸蒸发结晶得MgCl26H2O晶体,因为MgCl26H2O受热易水解生成氢氧化镁,所以在HCl的气流中加热得到MgCl2固体,最后再电解熔融MgCl2固体得到镁,所以从沉淀a中获得单质Mg的流程图为
I2~3S2O32﹣ , 样品的纯度将偏高,所以答案是:偏高;(6)沉淀a为Mg(OH)2固体,加浓盐酸蒸发结晶得MgCl26H2O晶体,因为MgCl26H2O受热易水解生成氢氧化镁,所以在HCl的气流中加热得到MgCl2固体,最后再电解熔融MgCl2固体得到镁,所以从沉淀a中获得单质Mg的流程图为 ![]() ,
,
所以答案是: ![]() .
.


 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 稀硫酸与铁粉反应:2Fe+6H+=2Fe3++3H2↑
B. CaCO3与稀盐酸反应:CO32–+2H+=CO2↑+H2O
C. FeCl3溶液与Fe反应:Fe3++Fe=2Fe2+
D. 钠与水反应:2Na+2H2O=2Na++2OH–+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从南方往北方长途运输水果时,常常将浸泡有酸性高锰酸钾溶液的硅藻土放置在盛放水果的容器中,其目的是
A. 利用酸性高锰酸钾溶液杀死水果周围的细菌,防止水果霉变
B. 利用酸性高锰酸钾溶液吸收水果周围的氧气,防止水果腐烂
C. 利用酸性高锰酸钾溶液吸收水果产生的乙烯,防止水果早熟
D. 利用睃性髙锰酸钾溶液的氧化性,催熟水果
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.5L某NaCl溶液中含有0.5molNa+ , 对该溶液的说法不正确的是( )
A.配制100mL该溶液需用5.85g NaCl
B.该溶液的物质的量浓度为1molL ﹣1
C.该溶液中含有58.5g NaCl
D.量取100mL该溶液,其中Na+的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T°C时,在一固定容积的密闭容器中发生反应:A(g)+B(g)C(s)△H<0,按照不同配比充入A,B,达到平衡时容器中A,B浓度变化如图中曲线(实线)所示,下列判断正确的是( ) 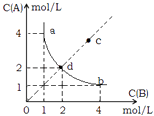
A.T°C时,该反应的平衡常数值为4
B.c点没有达到平衡,此时反应向逆向进行
C.若c点为平衡点,则此时容器内的温度高于T°C
D.T°C时,直线cd上的点均为平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把一定量的Na2O2和NaHCO3的混合粉末分为两等份,将其中一份加入到100mL稀盐酸中恰好完全反应,生成的气体干燥后体积为2.24L(标况);再将此气体通入另一份混合物中,恰好完全反应后,得到O2 2.016L(标况),则加入稀盐酸的物质的量浓度是( )
A.3.4mol/L
B.0.2mol/L
C.1.8mol/L
D.3.6mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com