
【题目】铜及其化合物具有广泛的应用,间接碘量法可以测定铜合金中的铜,回答下列问题:
(1)铜合金的种类较多,主要有黄铜和各种青铜等。试样可以用HNO3分解,还需要用到浓H2SO4.CuSO4和Cu(NO3)2中阳离子的基态核外电子排布式为______;S、O、N三种元素的第一电离能由大到小的顺序为______;
(2)Cu(NO3)2溶液中通入足量NH3能生成配合物[Cu(NH3)4](NO3)2,其中NH3中心原子的杂化轨道类型为______,[Cu(NH3)4](NO3)2属于______晶体。
(3)CuSO4溶液中加入过量KCN能生成配离子[Cu(CN)4]2-,1 mol CN-中含有的π键数目为______,与CN-互为等电子体的离子有______(写出一种即可);
(4)CuSO4的熔点为560℃,Cu(NO3)2的熔点为115℃,CuSO4熔点更高的原因可能是______;
(5)在弱酸性溶液中,Cu2+与过量KI作用,生成CuI沉淀,同时析出定量的I2;如图为碘晶体晶胞结构。下列有关说法中正确的是______;
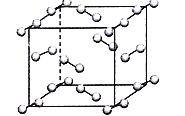
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子,以4配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中的碘原子间存在非极性键和范德华力
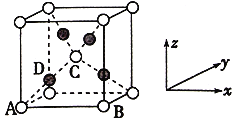
(6)已知Cu2O晶胞结构如图所示,该晶胞原子坐标参数A为(0,0,0),B为(1,0,0),C为(![]() )。则D原子的坐标参致为______,它代表______原子(填元素符号);已知金属铜的堆积方式是面心立方最密堆积,则晶体中铜原子的配位数是12,Cu原子的空间利用率是______。
)。则D原子的坐标参致为______,它代表______原子(填元素符号);已知金属铜的堆积方式是面心立方最密堆积,则晶体中铜原子的配位数是12,Cu原子的空间利用率是______。
【答案】1s22s22p63s23p63d9 N>O>S sp3 离子 2NA ![]() CuSO4和Cu(NO3)2均为离子晶体,SO42-所带电荷比NO3-大,故CuSO4晶格能较大,熔点较高 A (
CuSO4和Cu(NO3)2均为离子晶体,SO42-所带电荷比NO3-大,故CuSO4晶格能较大,熔点较高 A (![]() ,
,![]() ,
,![]() ) Cu 74%
) Cu 74%
【解析】
(1)阳离子为Cu 2+,Cu原子核外电子数为29,原子形成阳离子时,先失去高能层中电子,同一能层先失去高能级中电子;同主族自上而下元素第一电离能减小,N元素原子2p轨道为半充满稳定状态,第一电离能高于同周期相邻元素的;
(2)NH3中N原子形成3个N-H,含有1对孤对电子,VSEPR模型为四面体;[Cu(NH3)4](NO3)2由[Cu(NH3)4]2+ 与NO3-构成,是离子化合物;
(3)CN-与N2互为等电子体,CN-中C、N之间形成C≡N三键,三键含有1个σ键、2个π键;将N原子用碳原子与1个单位负电荷替换可得到与CN-互为等电子体的一种离子;
(4)离子电荷越多,晶格能越大,物质的熔点越高;
(5)同种非金属元素之间形成非极性共价键,碘为分子晶体,碘晶体中的碘原子间存在非极性键和范德华力,晶胞中占据顶点和面心,碘分子的排列有2种不同的取向;
(6)晶胞原子坐标参数A为(0,0,0)、B为(1,0,0)、C为(![]() ,
,![]() ,
,![]() ),如图坐标系中,A为处于坐标系中的原点(定义为O),则C处于晶胞体心位置,A、D、C的连线处于体对角线线上,且D处于A、C连线的中点位置,D到晶胞左侧面距离为参数x,D到晶胞前面的距离为参数y,D到晶胞下底面距离为参数z;计算晶胞中白色球、黑色球数目,结合化学式确定代表的元素;金属铜是面心立方最密堆积方式,Cu原子处于顶点与面心,顶点Cu原子与面心Cu原子相邻,每个顶点为8个晶胞共用,每个面为2个晶胞共用;设Cu原子半径为r,则晶胞棱长为2
),如图坐标系中,A为处于坐标系中的原点(定义为O),则C处于晶胞体心位置,A、D、C的连线处于体对角线线上,且D处于A、C连线的中点位置,D到晶胞左侧面距离为参数x,D到晶胞前面的距离为参数y,D到晶胞下底面距离为参数z;计算晶胞中白色球、黑色球数目,结合化学式确定代表的元素;金属铜是面心立方最密堆积方式,Cu原子处于顶点与面心,顶点Cu原子与面心Cu原子相邻,每个顶点为8个晶胞共用,每个面为2个晶胞共用;设Cu原子半径为r,则晶胞棱长为2![]() r,计算晶胞中Cu原子总体积,该晶胞中Cu原子的空间利用率。
r,计算晶胞中Cu原子总体积,该晶胞中Cu原子的空间利用率。
(1)阳离子为Cu 2+,Cu原子核外电子数为29,阳离子的基态核外电子排布式为:1s22s22p63s23p63d9;由元素周期律可知,同主族自上而下元素第一电离能减小,N元素原子2p轨道为半充满稳定状态,第一电离能高于同周期相邻元素的,故第一电离能为:N>O>S;
(2)NH3中N原子形成3个N-H,含有1对孤对电子,杂化轨道数目为4,VSEPR模型为四面体,中心N原子采取sp3杂化;[Cu(NH3)4]2+ 与NO3-形成离子化合物,则[Cu(NH3)4](NO3)2属于离子晶体;
(3)CN-与N2互为等电子体,CN-中C、N之间形成C≡N三键,三键含有1个σ键、2个π键,1mol CN中含有的2molπ键,1mol CN中含有的π键数目为:2NA;将N原子用碳原子与1个单位负电荷替换可得到与CN-互为等电子体的一种离子:![]() ;
;
(4)CuSO4和Cu(NO3)2均为离子晶体,SO42-所带电荷比NO3-大,故CuSO4晶格能较大,熔点较高;
(5)A.碘分子的排列有2种不同的取向,在顶点和面心不同,2种取向不同的碘分子以4配位数交替配位形成层结构,故A正确;
B.用均摊法计算:顶点碘分子个数加面心碘分子个数=8×![]() +6×
+6×![]() =4,因此平均每个晶胞中有4个碘分子,即有8个碘原子,故B错误;
=4,因此平均每个晶胞中有4个碘分子,即有8个碘原子,故B错误;
C.碘晶体为无限延伸的空间结构,构成微粒为分子,是分子晶体,故C错误;
D.碘晶体中的碘原子间存在I-I非极性键,而晶体中碘分子之间存在范德华力,故D错误;
故答案为:A;
(6)晶胞原子坐标参数A为(0,0,0)、B为(1,0,0)、C为(![]() ,
,![]() ,
,![]() ),如图坐标系中,A为处于坐标系中的原点(定义为O),则C处于晶胞体心位置,A、D、C的连线处于体对角线线上,且D处于A、C连线的中点位置,故D到晶胞左侧面距离为
),如图坐标系中,A为处于坐标系中的原点(定义为O),则C处于晶胞体心位置,A、D、C的连线处于体对角线线上,且D处于A、C连线的中点位置,故D到晶胞左侧面距离为![]() 、到晶胞前面的距离为
、到晶胞前面的距离为![]() ,到晶胞下底面距离为
,到晶胞下底面距离为![]() ,故D的参数为(
,故D的参数为(![]() ,
,![]() ,
,![]() );晶胞中白色球数目=1+8×
);晶胞中白色球数目=1+8×![]() =2,黑色球数目=4,二者数目之比为1:2,而化学式为Cu2O,故黑色球为Cu原子、白色球为O原子,即D表示Cu原子;金属铜是面心立方最密堆积方式,Cu原子处于顶点与面心,顶点Cu原子与面心Cu原子相邻,每个顶点为8个晶胞共用,每个面为2个晶胞共用,设Cu原子半径为r,则晶胞棱长为2
=2,黑色球数目=4,二者数目之比为1:2,而化学式为Cu2O,故黑色球为Cu原子、白色球为O原子,即D表示Cu原子;金属铜是面心立方最密堆积方式,Cu原子处于顶点与面心,顶点Cu原子与面心Cu原子相邻,每个顶点为8个晶胞共用,每个面为2个晶胞共用,设Cu原子半径为r,则晶胞棱长为2![]() r,晶胞体积=(2
r,晶胞体积=(2![]() r)3,晶胞中Cu原子数目=8×
r)3,晶胞中Cu原子数目=8×![]() +6×
+6×![]() =4,晶胞中Cu原子总体积=4×
=4,晶胞中Cu原子总体积=4×![]() πr3,该晶胞中Cu原子的空间利用率是=
πr3,该晶胞中Cu原子的空间利用率是=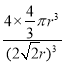 ×100%=74%。
×100%=74%。


科目:高中化学 来源: 题型:
【题目】氮的化合物应用广泛,但氮氧化物是重要的空气污染物,应降低其排放。
(1)用CO2和NH3可合成氮肥尿素
已知:①2NH3(g)+CO2(g)===NH2CO2NH4(s) △H=-159.5kJ·mol-1
②NH2CO2NH4(s)===CO(NH2)2(s)+H2O(g) △H=+116.5kJ·mol-1
③H2O(1)===H2O(g) △H=+44kJ·mol-1
用CO2和NH3合成尿素(副产物是液态水)的热化学方程式为___________。
(2)工业上常用如下反应消除氮氧化物的污染:
CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) △H
N2(g)+CO2(g)+2H2O(g) △H
在温度为T1和T2时,分别将0.40 mol CH4和1.0 mol NO2充入体积为1L的密闭容器中,n(CH4)随反应时间的变化如图所示:

①根据如图判断该反应的△H___________0(填“>”“<”或“=”),理由是___________。
②温度为T1时,0~10min内NO2的平均反应速率v(NO)2=___________,反应的平衡常数K=______(保留三位小数)
③该反应达到平衡后,为再提高反应速率同时提高NO2的转化率,可采取的措施有______(填编号)。
A.改用高效催化剂 B.升高温度
C.缩小容器的体积 D.增加CH4的浓度
(3)利用原电池反应可实现NO2的无害化,总反应为6NO2+8NH3===7N2+12H2O,电解质溶液为NaOH溶液,工作一段时间后,该电池正极区附近溶液pH___________(填“增大”“减小”或“不变”),负极的电极反应式为___________。
(4)氮的一种氢化物HN3,其水溶液酸性与醋酸相似,则NaN3溶液中各离子浓度由大到小的顺序为___________;常温下将 a mol·L-1的HN3与b mol·L-1的Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(N3-),则该混合物溶液呈___________(填“酸”“碱”或“中”)性,溶液中c(HN3)=___________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用煤油作溶剂,二(2-乙基己基)磷酸酯作流动载体,H2SO4 作内相酸处理含铜废水。 在其他条件相同时,Cu2+萃取率[萃取率= ×100% ]与初始 Cu2+浓度关系如图 1 所示;在其他条件相同时,处理前初始 Cu2+浓度为 200 mg·L-1,Cu2+萃取率与废水 pH 的关系如图 2 所示。下列说法错误的是
×100% ]与初始 Cu2+浓度关系如图 1 所示;在其他条件相同时,处理前初始 Cu2+浓度为 200 mg·L-1,Cu2+萃取率与废水 pH 的关系如图 2 所示。下列说法错误的是
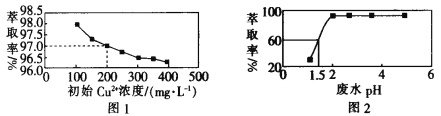
A.根据图 1 可知,废水中初始 Cu2+浓度越大,Cu2+的萃取效果越好
B.根据图 2 可知,废水初始 pH>2 时,去除 Cu2+的效果较好
C.根据图 1 可知,Cu2+初始浓度为 200 mg·L-1 时,Cu2+的萃取率为 97.0%
D.根据图 2 可知,若取 800 mL 初始 Cu2+浓度为 200 mg·L-1 的废水,在 pH=1.5 时处理废水,则处理后的废水中剩余 Cu2+的物质的量为 1.5×10-3mol(假设体积不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍及其化合物在工业生产和科研领域有重要的用途。请回答下列问题:
(1)基态 Ni 原子中,电子填充的能量最高的能级符号为_________,价层电子的轨道表达式为_________。
(2)Ni的两种配合物结构如图所示:
A B
①A 的熔、沸点高于B的原因为_________。
②A晶体含有化学键的类型为___________(填选项字母)。
A.σ键 B.π键 C.配位键 D.金属键
③A晶体中N原子的杂化形式是_________。
(3) 人工合成的砷化镍常存在各种缺陷,某缺陷砷化镍的组成为Ni1.2As, 其中 Ni 元素只有+2 和+3 两种价态, 两种价态的镍离子数目之比为_________。
(4) NiAs的晶胞结构如图所示:

①镍离子的配位数为_________。
②若阿伏加德罗常数的值为NA,晶体密度为 ρ g·cm-3,则该晶胞中最近的砷离子之间的距离为_________pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.天然弱碱水呈碱性的原因是其中含有较多的Mg2+、Ca2+等离子
B.生活中用电解食盐水的方法制取消毒液,运用了盐类水解的原理
C.向CuCl2溶液中加入CaCO3,调节pH可除去溶液中混有的Fe3+
D.焊接时用NH4Cl溶液除锈与盐类水解有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,HNO2的电离常数Ka=7.1×10-4,NH3·H2O的电离常数Kb=1.7×10-5。0.1 mol·L-1 NH4NO2溶液中,离子浓度由大到小的顺序是__________,常温下NO2-水解反应的平衡常数Kh=_______(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷酸(H3AsO4)分步电离的平衡常数(25℃)为:K1=5.6×10-3,K2=1.7×10-7,K3=4.0×10-12,第三步电离的平衡常数的表达式为K3=________;Na3AsO4的第一步水解的离子方程式为:AsO43-+H2O![]() HAsO42-+OH-,该步水解的平衡常数(25℃)为_________________。
HAsO42-+OH-,该步水解的平衡常数(25℃)为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学采用工业大理石(含有少量SiO2、Al2O3、Fe2O3等杂质)制取CaCl2·6H2O,设计了如下流程:
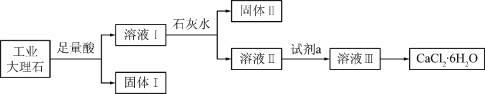
下列说法不正确的是
A. 固体I中含有SiO2,固体II中含有Fe(OH)3
B. 使用石灰水时,要控制pH,防止固体II中Al(OH)3转化为AlO2-
C. 试剂a选用盐酸,从溶液III得到CaCl2·6H2O产品的过程中,须控制条件防止其分解
D. 若改变实验方案,在溶液I中直接加氨水至沉淀完全,滤去沉淀,其溶液经蒸发浓缩、冷却结晶也可得到纯净CaCl2·6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中a、b、c表示相应仪器中加入的试剂,可用如图装置制取、净化、收集的气体是( )
编号 | 气体 | a | b | c |
|
A | NH3 | 浓氨水 | 生石灰 | 碱石灰 | |
B | CO2 | 盐酸 | 碳酸钙 | 饱和NaHCO3溶液 | |
C | NO | 稀硝酸 | 铜屑 | H2O | |
D | NO2 | 浓硝酸 | 铜屑 | NaOH溶液 |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com