
����Ŀ���ݱ�����һ���������ɶ�����̼�������ϳ��Ҵ��ѳ�Ϊ��ʵ��
��֪����CH3CH2OH��l��+3O2��g���T2CO2��g��+3H2O��l����H=��1366.8kJ/mol
��2H2��g��+O2��g���T2H2O��l����H=��571.6kJ/mol
��1��д����CO2��H2��Ӧ�ϳ�CH3CH2OH��l����H2O��l�����Ȼ�ѧ����ʽ
��2�������Ҵ�ȼ�ϵ���״��棬���ƹ㣬�Ի�����ȾС�����зdz������ķ�չǰ������ȼ�ϵ���У�ʹ�ò����缫��KOH��Һ���������Һ��ͨ���Ҵ�ȼ����һ��Ϊ�����ü��ϵĵ缫��ӦʽΪ ��
��3�����Ҵ�ȼ�ϵ�ص��400mL ����ʳ��ˮװ�ÿɼ�ʾ��ͼ����װ���з�����ⷴӦ�ķ���ʽΪ�������������۲쵽��������������������448mL���壨����ڱ�״���²�ã�ʱ��ֹͣ��⣬���������Һ��Ͼ��ȣ���Һ��pHΪ �� ��������������ܽ⼰��Һ����ı仯�� 
���𰸡�
��1��2CO2��g��+6H2��g��=CH3CH2OH��l��+3H2O��l����H=��348kJ/mol
��2������C2H6O+16OH����12e��=2CO32��+11H2O
��3��2NaCl+2H2O ![]() Cl2��+H2��+2NaOH����Һ��죻13
Cl2��+H2��+2NaOH����Һ��죻13
���������⣺��1����CH3CH2OH��l��+3O2��g��=2CO2��g��+3H2O��l����H=��1366.8kJ/mol����2H2��g��+O2��g��=2H2O��l����H=��571.6kJ/mol��
���ݸ�˹���ɣ��ڡ�3���ٿɵã�2CO2��g��+6H2��g��=CH3CH2OH��l��+3H2O��l����H=����571.6kJ/mol����3������1366.8kJ/mol��=��348kJ/mol��
���Դ��ǣ�2CO2��g��+6H2��g��=CH3CH2OH��l��+3H2O��l����H=��348kJ/mol����2�����Ҵ�ȼ�ϵ���У���������ȼ���Ҵ�����ʧ���ӵ�������Ӧ���ڼ��Ի����µĵ缫��ӦΪ��C2H6O+16OH����12e��=2CO32��+11H2O��
���Դ��ǣ�����C2H6O+16OH����12e��=2CO32��+11H2O����3������ͼʾ��֪�����ĵ缫���ӵ�Դ�ĸ�����Ϊ���ص�����������������ԭ��Ӧ�����������Ҳ�����ԭ��ص�ֱ�ӣ����Ե��ص��Ҳ�Ϊ��������������������Ӧ�����������缫����ʳ��ˮ�ķ���ʽΪ��2NaCl+2H2O ![]() Cl2��+H2��+2NaOH��
Cl2��+H2��+2NaOH��
������ˮ����������ӷŵ磬ʹˮ�ĵ���ƽ�������ƶ�������������Ũ���������Դ��з�̪����Һ��죻
�������ɱ���µ�448mL���壬������Ϊ�����������448mL���������ʵ���Ϊ0.02mol�����ݷ�Ӧ����ʽ2NaCl+2H2O ![]() Cl2��+H2��+2NaOH��֪������0.02mol����������0.04mol�������ƣ������Һ������������Ũ��Ϊ��c��OH����=c��NaOH��=
Cl2��+H2��+2NaOH��֪������0.02mol����������0.04mol�������ƣ������Һ������������Ũ��Ϊ��c��OH����=c��NaOH��= ![]() =0.1mol/L����Һ��������Ũ��Ϊ��1��10��13mol/L����Һ��pH=13��
=0.1mol/L����Һ��������Ũ��Ϊ��1��10��13mol/L����Һ��pH=13��
���Դ��ǣ�2NaCl+2H2O ![]() Cl2��+H2��+2NaOH����Һ��죻13��
Cl2��+H2��+2NaOH����Һ��죻13��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����Ʊ���������泥�NH2COONH4���ķ�Ӧ���£�2NH3��g��+CO2��g��NH2COONH4��s��
�÷�Ӧ�ڸ��������½����ɰ�������泥�����ˮ����������̼��炙�̼����泥�
��1���÷�Ӧ��һ���������ܹ��Է����У���Ӧ�ġ�H0��������ڡ�С�ڻ���ڣ�
��2��д������̼����淋Ļ�ѧ����ʽ ��
��3��ʵ�鲽�����£�
����1����ͼ��ʾ��װ���������װ�������ԣ�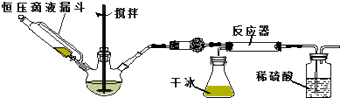
����2������Ӧ������װ��ҩƷ��������������ƿ�м����������ƹ��壬��ѹ��Һ©����װ��Ũ��ˮ��
����3���μ�Ũ��ˮ�����裬���ڷ�Ӧ���ʣ��ڷ�Ӧ���еõ���Ʒ��
�ٸ������ʢ�ŵ�ҩƷ�� ��
�ڶԱ�̼���κ��ᷴӦ��CO2 �� ��ʵ�����øɱ���������CO2������ŵ��� �� ��
���Ժ�ѹ��Һ©�������Һ©����Ŀ���� ��
�ܷ�Ӧ����CO2�������½�ʱ���ɲ�ȡ����Ӧ��ʩ�� ��
��4����ʵ��װ�ÿ������ٵİ�ȫ������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������Һ���ϲ�ȡһЩ��Һ���ⶨ�����ܶ�Ϊa g��cm��3���ٴ��²�ȡһЩ��Һ���ⶨ�����ܶ���ֵӦΪ
A.����aB.С��aC.����aD.��ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҿ���NaNO2+NH4Cl=NaCl+N2��+2H2O�Ʊ�N2������˵����ȷ���ǣ� ��
A. NaNO2����������Ӧ
B. NH4Cl�еĵ�Ԫ�ر���ԭ
C. N2��������������ǻ�ԭ����
D. ÿ����1mol N2ת�Ƶ��ӵ����ʵ���Ϊ6mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѡ��ij��Ӧ�ķ�Ӧ�����������仯��ͼ��ʾ��ͼ��E1��ʾ����Ӧ�Ļ�ܣ�E2��ʾ�淴Ӧ�Ļ�ܣ��������й�������ȷ���ǣ� �� 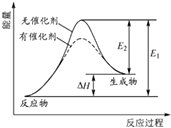
A.�÷�ӦΪ���ȷ�Ӧ
B.�����ܸı䷴Ӧ���ʱ�
C.�����ܽ��ͷ�Ӧ�Ļ��
D.�淴Ӧ�Ļ�ܴ�������Ӧ�Ļ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ƣ�Na2S2O3������Ϊ���ȼ�����֪25 mL 0.1 mol/L Na2S2O3��Һǡ�ð�224 mL����״���£�Cl2��ȫת��ΪCl������S2O32-��ת��Ϊ��������
A. SO42-B. SO32-C. SD. S2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2.3g��Ͷ�뵽97.8gˮ�У���Ӧ��Ϻõ�100mL����Һ����
��1�����������ڱ���µ���� ��
��2����������������Һ�������������� ��
��3����������������Һ�����ʵ���Ũ�� ��
��4����K2Cr2O7+14HCl�T2KCl+3Cl2��+7H2O+2CrCl3�ķ�Ӧ�У���0.3mol����ת��ʱ����Cl2�����Ϊ����״��������������HCl�����ʵ���Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����PH��14����Һ�У��ܴ����������ɫ��Һ�ǣ� ��
A.Na����Cu2����Cl����SO42��B.Mg2����Ba2����NO3����Cl��
C.K����Na����SO42����CO32��D.K����Ag����HCO3����Br��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��D��E��F��G�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵����������������A��B��C��D��EΪ��ͬ�����Ԫ�أ�A��C��������������������Ӳ�����2����B�ĵ縺�Դ���C������ɫ�ܲ����۲�E����ɫ��ӦΪ��ɫ��F�Ļ�̬ԭ������4��δ�ɶԵ��ӣ�G��+1�����������ó���K��L��M�������Ӳ㣮�ش��������⣺
��1��A��B��C��D��E��F��G����Ԫ���е�һ��������С��������Ԫ�ط��ţ���DԪ�ص�ԭ�Ӻ������ֲ�ͬ�˶�״̬�ĵ��ӣ����ֲ�ͬ�ܼ��ĵ��ӣ���̬��F3+��������Ų�ʽ�� ��
��2��B����̬�⻯����ˮ�е��ܽ��Զ����A��C����̬�⻯�ԭ���� ��
��3��������AC2�ĵ���ʽ�� ��
��4��FD3��ECAB��Һ��ϣ��õ�������������Ѫ��ɫ��Һ��������λ��Ϊ5�������Ļ�ѧʽ�� ��
��5��������EF[F��AB��6]��һ����ɫ���壬��ͼ1��ʾ�侧���� ![]() ��E+δ������������ɫ�����һ��������E+�ĸ���Ϊ ��
��E+δ������������ɫ�����һ��������E+�ĸ���Ϊ �� 
��6��G�Ķ��������������Ҷ�����H2N��CH2һCH2һNH2���γ������ӣ���ͼ2�������������к��еĻ�ѧ�������� �� ������ĸ�� 
a����λ�� b�����Լ� c�����Ӽ� d���Ǽ��Լ�
������CAB���е�Aԭ�����Ҷ�����H2N��CH2һCH2һNH2����Cԭ�ӵ��ӻ���ʽ�ֱ�Ϊ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com