
【题目】Ⅰ.已知:反应aA(g)+bB(g)cC(g),某温度下,在 2 L 的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。

(1)经测定前4 s内v(C)=0.05 mol·L1·s1,则该反应的化学方程式为______________。
(2)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:v(A)=0.3 mol·L1·s1;乙:v(B)=0.12 mol·L1·s1;丙:v(C)=9.6 mol·L1·min1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为___________(用甲、乙、丙表示)。
Ⅱ.为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题。
编号 | 操作 | 实验现象 |
① | 分别在试管A、B中加入5 mL 5% H2O2溶液,各滴入1~2 滴1 mol/L FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5 ℃左右冷水的烧杯中;将试管B放入盛有40 ℃左右热水的烧杯中 | 试管A中不再产生气泡试管B中产生的气泡量增大 |
② | 另取两支试管分别加入5 mL 5% H2O2溶液和5 mL 10% H2O2溶液 | 试管A、B中均未见气泡产生 |
(3)实验①的目的是_______________________________,实验中滴加FeCl3溶液的目的是____________________________。
(4)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是______________________________________________________________(用实验中所提供的几种试剂)。

(5)某同学在50 mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如右图所示,则A、B、C三点所表示的即时反应速率最慢的是______。
【答案】3A(g)+B(g) 2C(g) 乙>甲>丙 研究温度对H2O2分解速率的影响 加快H2O2分解速率,使实验现象易于观察 将两支试管同时放入盛有热水的烧杯中,或向两支试管中同时滴入2滴1 mol/L FeCl3溶液,观察产生气泡的速率 C点
【解析】
I(1)反应中各物质浓度的改变量之比等于化学计量数之比,前4s时,A、B分别为0.3mol/L、0.1mol/L,C的改变量为v(C)×t=0.05mol/(Ls)×4s=0.2mol/L,计量数之比为3:1:2,则方程式为:3A(g)+ B(g)2C(g);
(2)转化为同一物质的反应速率分别为:甲:v(A)=0.3 mol·L1·s1;乙:v(A)=0.36 mol·L1·s1;丙:v(C)=0.24 mol·L1·s1,反应由快到慢的顺序为乙>甲>丙;
II(3)实验①过氧化氢的浓度、催化剂相同,而温度不同,则目的探究温度对H2O2分解速率的影响;滴加FeCl3溶液的目的加快H2O2分解速率,使实验现象易于观察;
(4)常温下,过氧化氢不易分解,为提高分解速率可使用催化剂或升高温度的方法;
(5)反应开始时,过氧化氢的浓度最大,催化剂参与反应,反应前后量不变,则浓度越大反应速率越快,反应速率最慢的为C点。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某强酸性溶液中可以大量共存的离子组是
A.K+、NO3﹣、OH﹣、Cl﹣
B.SO42﹣、Mg2+、Cl﹣、Na+
C.SO42﹣、Na+、Mg2+、SO32﹣
D.Cl﹣、SCN﹣、K+、Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室制取乙酸乙酯的主要步骤如下:

①在甲试管(如图)中加入2mL浓硫酸、3mL乙醇和2mL乙酸的混合溶液。
②按如图连接好装置(装置气密性良好)并加入混合液,小火均匀地加热3—5min。
③待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层、洗涤、干燥。
(1) 写出该反应的化学方程式是:_______________________;
(2) 与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是____________。
(3)甲试管中,混合溶液的正确加入顺序:________________________;
(4)步骤②中需要用小火均匀加热,其主要原因是____________________________________;
(5)上述实验中饱和碳酸钠溶液的作用是____________(填字母代号)。
A. 反应掉乙酸和乙醇 B. 反应掉乙酸并吸收乙醇
C. 析出乙酸乙酯 D. 加速酯的生成,提高其产率
(6)欲将乙试管中的物质分离开以得到乙酸乙酯,必须使用的仪器是____________;分离时,乙酸乙酯应该从仪器____________(填:“下口放”或“上口倒”)出。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液的pH=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是
A. 1∶9 B. 1∶1 C. 1∶2 D. 1∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A. 由图甲可以判断:对于反应A(g)+B(g) ![]() 2C(g),若T1>T2,则ΔH<0
2C(g),若T1>T2,则ΔH<0
B. 图乙表示可逆反应CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH>0
CO2(g)+H2(g) ΔH>0
C. 图丙表示CO2通入饱和Na2CO3溶液中,溶液导电性变化
D. 图丁表示0.1 mol·L-1的盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液pH随加入盐酸体积的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.如图为原电池装置示意图。

(1)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4===2PbSO4+2H2O,写出B电极反应式:__________。该电池在工作时,A电极的质量将_______(填“增加”“减小”或“不变”),若该电池反应消耗了0.1 mol H2SO4,则转移电子的数目为________。
(2)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出A电极反应式:_____________________________。该电池在工作一段时间后,溶液的碱性将________(填“增强”“减弱”或“不变”)。
Ⅱ.现用图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量。量筒的规格为1000 mL,供选择的电极材料有纯铜片和纯锌片。

(3)b电极材料为________,其电极反应式为_________________________。
(4)当量筒中收集到672 mL(标准状况下)气体时,通过导线的电子的物质的量为________mol,此时a电极质量________(填“增加”或“减少”)________g。
(5)如果将a、b两电极的电极材料对调,U形管中将出现的现象是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。

(1)实验过程中铜网出现黑色和红色交替的现象,请写出相应的化学方程式______________________________、________________________________。
(2)甲水浴的作用是_________________________________________;乙水浴的作用是_________________________________________。
(3)反应进行一段时间后,干试管a中能收集到不同的物质,它们是________。集气瓶中收集到的气体的主要成分是________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有______。要除去该物质,可在混合液中加入____________(填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生设计氨催化氧化实验,并将制得NO进一步氧化为NO2用水吸收NO2,并检验HNO3的生成。
可供选择的固体药品有:NH4Cl、Ca(OH)2、KClO3、MnO2、CaO
可供选择的液体药品有:浓氨水、过氧化氢、浓盐酸、水
可供选择的仪器有:如图
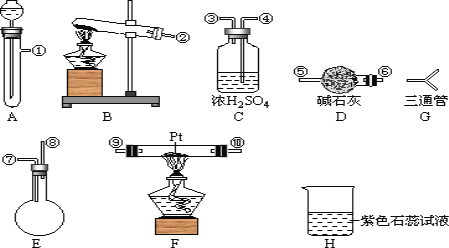
另有铁架台、铁夹、铁圈、乳胶管若干,可供选择。设计实验时,A和B两个制气装置允许使用两次,其余装置只能使用一次。
(1)氨氧化制NO的化学反应为__________________________,该反应应在装置____中进行。
(2)为快速制NH3和O2,制取NH3的装置最好选择_______,其化学反应方程式为______________;制取O2的装置最好选择_______。
(3)装置C的作用是___________________。
(4)装置H中溶液变红,其原因是(用化学方程式表示)______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com